����ժ Ҫ����GATA���������һ�ຬ��пָ�ṹ���ת¼���ӣ��������Եؽ�Ϲ�ͬ�ĺ���������A/T(GATA)A/G���������ü����ڶ����㷺�ֲ����书����Ҫ�漰�߲�ֻ������ٷ�������ά�ֵȷ��档�ֶ�GATA����Ļ�����Ϣ���ṹ�ͷ�����м�飬����������GATA�����Ա���������е��о���չ������δ�����о��������չ����
�����ؼ��� : GATA����;����ѧ����;������:����;
����Abstract����The GATA family are transcription factors containing one or two zinc-finger DNA-binding domains. They are so-called because they bind to the consensus DNA sequence A/T(GATA)A/G. They have been found throughout the animal kingdom, and have been shown to play critical roles in germ layer differentiation, organ development and function maintenance. This article briefly introduces the basic information, structure and classification of the GATA family, summarizes the recent research progress of GATA family members in invertebrate, and finally looks forward to the future research directions.
����Keyword����GATA family; biological function; invertebrate; evolution;
����GATA������һ����б���IV��пָ�ṹ���ת¼���ӣ��������Ե���л��������ӵ�A/T(GATA)A/G���н�϶�����[1,2]��1988�꣬��˳ʽԪ��A/T(GATA)A/G�����״��ڼ��鵰������������ϱ�����[3]��֮�����˳ʽԪ����ϵ�ת¼���ӱ���¡��������ΪGata1[4]��Ŀǰ��GATA�����ڼ����������й㷺��������о�����������һ����6��GATA�����Ա(GATA1��6)���������ǵ�ϵͳ������ϵ����֯����������GATA�����ΪGATA1/2/3��GATA4/5/6�����Ǽ���[5]��GATA1/2/3�Ǽ�������Ѫϵͳ��������ϵͳ�ֻ��ͷ���������ģ�GATA4/5/6�Ǽ������С����߲�������б�������ࡢ���ࡢ�κ���ֳ�ٵȣ�����֯�����Ի���ı�����ؼ��Եĵ�������[6,7,8]����������GATA���廹�������ڰ�ϸ�����쳣��ֳ�Լ�ϸ���ر���յ��ȷ��淢������[9,10,11]������������ࡢ���ַḻ����̽��GATA�����Ա���ܺͽ�������Ҫ������Դ�����ȣ�GATA�������������е��о���Ҫ������ģʽ����ڸ���Ӭ(Drosophila melanogaster)�����������߳�(Caenorhabditis elegans)�У�������������������Ҳ��չ��������ȱ��ȫ����ܽᱨ��������������GATA�����Ա���������е��о���չ������Ϊ���GATA������о��ṩ�ο���

����1 ��GATA����Ľṹ������
����GATA�����Աͨ�����������߶ȱ��ص�пָ�ṹ��(ͼ1)������ʽΪCys-X2-Cys-X17-Cys-X2-Cys (X��ʾ�ɱ䰱���ᣬ���ֱ�ʾ����)��C��пָ�ṹ��������������A/T(GATA)A/G��ϣ�N��пָ�ṹ��Ĺ������ȶ����ض����еĽ�ϻ�����������ϡ��������GATAת¼���Ӷ���������пָ�ṹ�����������У�����GATAת¼���ӽ�����C�˸�����DNA��ϵ�пָ�ṹ��[5,12]��
������ͬ������GATA�����Ա����Ŀ��ͬ�����������ձ����6����Ա�����У�Ӳ�������GATA2�ֵ���������һ���γ�GATA2a��GATA2b[13]����������GATA�����Ա��Ŀ���̶����ڵ͵ȵĶ�����źʹ̰��������н�����һ����Ա[14,15,16]���ӱ��ζ����ŵ���֫������GATA�������Ŀ���̶�[17,18,19,20,21,22,23,24]����Ƥ���β�������ͷ��������һ���������GATA�����Ա[25,26]��
����ͼ1 GATA�����Աпָ�ṹ������бȶ�

�����»��߱�ʾпָ�ṹ��CΪ��GATA�����б��صİ��װ���л���
����2 ��������GATA�������
����2.1�� �����ʹ̰�����
�����������Ŀǰ���־���GATA�����Ա����͵ȵ�������ڱ�������(Amphimedon queenslandica)��˫���ͺ���(Sycon raphanus)�н�������һ��GATA�����ԱGata��������������ʾ��GATAλ��GATA1/2/3��GATA4/5/6�Ǽ���֮�䣬˵��GATA������Ŀ�����ŷ����ڶ������֮��[14,15]����������Gata�Ķ�λ������ʾ����������̥������û���ֻ���ڲ�ϸ���б������������Գƶ����Gata4/5/6�����߲�ı��˵�����ද����Ȼ���������ĺ������������ϸ����������������߲����ͬԴ�ԣ���ʾGATA��������ϸ����ֻ������ÿ��������߲����Դ[15]��
�����ڴ̰�������״����(Nematostella vectensis)�н�������Nv Gata���������������ڱ�����������Χ�ĵ���ϸ���������ɢ������ǻ������ԭ���ߺ�ɺ����ʱ�ڣ�����Ҫ������θ��Ƥϸ�����̰������Ƕ����߲�ֻ��Ŀ�ʼ��Nv Gata��Ҫ�����߲���ﰵʾ���������߲�ֻ���������[16]��
����2.2 �������
�����ڵ��к�Բͷ�г�(Schmidtea mediterranea)��������GATA�����Ա���ֱ�����GATA1/2/3��GATA4/5/6�Ǽ��塣Gata4/5/6��Ҫ�ֲ��ڳ������ڸ�ϸ����Ҳ���������Gata4/5/6�ý������³���ȱ�ݣ������¸�ϸ����ֳ����������Gata1/2/3���ý������Ա��ͱ仯��˵��Gata4/5/6���г�ij����ֻ������Źؼ�����[19]�������г�(Schmidtea polychroa)����4��GATA�����Ա��GATA123a��b����GATA1/2/3�Ǽ��壻GATA456a��b����GATA-4/5/6�Ǽ��塣�ڷ��������У�Gata456a������ä������Gata456b��λ�ڱ�����ʵ��ϸ��[20]�������о����������ζ����GATA4/5/6�Ǽ����Ա�����߲���Դ�����ٷֻ��ͷ����й��ܱ��ء�
����2.3 ���߳涯��
�����߳涯����GATA�����о������������������߳�(C.elegans)���������й���11��GATA�����Ա(ELT-1��7��END-1��END-3��MED-1��MED-2)���ڽṹ�ϣ���ELT-1��������пָ�ṹ�������Աֻ����C�˵�пָ�ṹ������������ʾELT-1����GATA1/2/3�Ǽ��壬������Ա����GATA4/5/6�Ǽ���[18]��
�������������߳�(C.elegans)�ı�Ƥ�ɸ����Ƥϸ�����ӷ�ϸ��(��ϸ������Ƥĸϸ��)�ͽ����Ƥϸ��(�ڡ�ֱ��������)��ɡ��ڱ�Ƥ�����У���ҪELT-1��ELT-3��ELT-5��ELT-6�Ĺ�ͬ���á�elt-1��C��������������PAL-1�ļ����´ٽ���Ƥǰ�������[27]��ELT-1�ɼ���elt-3�ڽӷ�ϸ������ı�Ƥϸ���б���Ӷ��ٽ���Ƥ�ֻ�[28,29]���ڽӷ�ϸ���У�elt-5��elt-6��ͬԴ���͵���CEH-16�����ͬ����elt-3�ڽӷ�ϸ���еı���[30]�����׳淢���У�elt-5��elt-6��ΪWnt�ź�ͨ·�����λ���ά�ֽӷ�ϸ����ϸ���������ȶ�[31,32]�����������������У�elt-5��elt-6��ΪHox����LIN-39�����λ���������ԭ��ϸ�������˺�ϸ���ں�[33]��Liu��[34]����ELT-6Ҳ���Դٽ�Lin-39�ı����ʾELT-5/ELT-6��LIN-39�����γ�һ��������������������ԭ��ϸ���ķֻ���
����ELT-2��ELT-7��END-1��END-3��MED-1��MED-2�ڳ���(���߲��Eϸ��ϵ)�ķֻ�����������ά�����DZ���ġ�������ʱ�ڣ�ĸԴ�Ե�SKN-1����med-1��med-2�ı���ٽ�EMSϸ�����ѳ�Eϸ��(�ֻ�Ϊ�������߲�)��MSϸ��(�γ��ʲ�����ڼ��⡢��ǻ����ֳ��)[35]��MED-1��MED-2�ɼ�������end-1��end-3�Ķ��ݱ���(1��3��ϸ����������ʧ)[36,37]����END-1��END-3ֱ�Ӽ���elt-2��elt-7�ı��ELT-2��ELT-7��һ������ges-1��ifb-2��pha-4�ȳ����ֻ�����ı���[38]�������о�������ELT-2�ܹ������������߲�GATAת¼���ӵ������߲��ػ��ͳ����ֻ���ά�֣���һ��֤����ELT-2�����߲㷢���еĹؼ�����[39,40,41]��elt-4����ĵ�����ELT-2�Ľض̵��ף�Ҳ�ڳ����б����Ŀǰ��δ��������幦��[42]���ڳɳ泦�������������У�ELT-2�ɱ����߳����ܲ�ԭ��ĸ�Ⱦ���ڶ���ϸ����ԭ��(��ͭ�̼ٵ�����Pseudomonas aeru-ginosa�����˺�ɳ���Ͼ�Salmonella typhimurium��)�����(�����������Cryptococcus neoformans)�ĸ�Ⱦ�����У��ó���elt-2��ʹ�߳�Ŀ��Խ���[43]��������Ⱦ��ͬ��ԭ���������߳�ת¼��͵������飬������ELT-2�����������ػ������Ÿ���[44]�����⣬elt-2�ڳ���ɳ���Ͼ�(Salmonella enterica)��Ⱦ��ָ����߳�ת¼���б����Ը�������elt-2���ý�ʹ�ָ���ػ���ı��オ��[45]����ͭ�̼ٵ�����(P.aeruginosa)��Ⱦ�ָ����ý�elt-2��ʾ��elt-2�ڸ�Ⱦ�ָ����ڵ����ø�����[46]�������о�������ELT-2���������������߳�(C.elegans)��������Ҫ�������ӣ�Ҳ�Ǽ�������߷�����Ӧ����Ҫ���ӡ�
����GATAת¼����Ҳ�����߳��Ӧ����Ӧ�ͷ������������ڡ�ELT-2��ELT-3�ڶ��ֻ���в����ͨ���ϵ������������������λ����ת¼��Ӧ�Ի����仯[47,48,49,50,51]��ELT-1ͨ���ٽ���ʱ���ػ���let-7����micro RNAs (mir-48��mir-84��mir-241)�ı����������߳�ķ���ʱ��[52]��Mann��[53]���֣�������(�ɳ��6��)��ʼ��ELT-2�ĺ�������˥�����٣���������л���ı����½������յ����߳�˥�ϡ�ELT-2������ͨ������N-��������ת��ø����(O-Glc NAc transferase,ogt)����˥�Ϲؼ�����DAF-16Эͬ�ӻ��߳��˥��[54,55]��
�������������߳�GATA�������Ա���书���ܽ����1��
����2.4 �����ڶ���
����2007�꣬Gillis��[21]�״μ�����ɳ��(Platynereis dumerilli)�е�GATAת¼���ӣ�������������ڷ����еĶ�λ�������ʾ��Gata123��Ҫ����̥�ĸ����ǰ������߲��������ڵ����׳��У�Gata123�����ڱ������߲��ϸ�����������������׳�ķ��������������ڸ������ںϣ�������Ԥ���γ������߲�ĸ����ڲ������ǿ��������16h,Gata456��ֲ�K�������߲���ϸ���ĺ���б��������24 h���������չ����ǰ��ë�֣�������48 h�������ݸ�ë�ҵ�λ�÷ֶα��������߲㣬���ڸ�ë�Ҹ����ı�������ߣ����׳��У��������ë����ص����ɼ����м���������[21]����ɳ��(P.dumerilli)���������У�Gata123��λ�����߲㣬Gata456���������߲��б������ë����(Chaetopterus variopedatus)(Gata-123a��Gata456a)[17]�������̹ܳ�(Hydroides elegans)(Gata1/2/3a��Gata1/2/3b��Gata4/5/6)[22]��Сͷ��(Capitella sp.I)(Gata A1��Gata B1��Gata B2��Gata B3)[60]��������ֳ���֦���dz�(Themiste lageniformis)(Gata456a��Gata456b)[17]�У�GATA��Ա�Ķ�λ�о����֣�����������GATA�����Ա����Ŀ��������𣬵��ڷ����еĶ�λ����ɳ��(P.dumerilli) GATA�Ǽ����Ա���߲�ֲ��ص���ͬ����ʾGATA�������߲�ֻ��о��б��ص����á�
����2.5 �����嶯��
����2014�꣬Yue��[23]��¡���ο��ȱ�(Chlamys farreri)��Gata���������ڳ���ĸ����ࡢѪϸ���������и߱�����ý�Gata��Ѫϸ���ĸ����ʺ���Ѫϸ���������½���Ϊ̽���ο��ȱ�(C.farreri)��Ѫϸ���ķ������������GATA�����ڷ��������еı���������ڵ����׳�Ŀ�ǰ��ë������ĶԳ�ϸ������ͬʱ���D���׳�ʱ�����ڱ�����״�ṹ�еı�������׳�ʱ�����״�ṹ�б����ϸ��������Gata�ڵ����׳桢D���׳�������׳��е�m RNA���������ߣ���ʾ���׳淢���п�����������Ѫϸ���ķ������ֱ��ڵ����׳������Գ�ϸ���Ż��״�ṹ��[61]��Salazar��[62]������(Euprymna tasmanica)����Ѫ��������(white body)�м�Gata2�ı��Song��[63]�ڳ�ĵ��(Crassostrea gigas)���ý�Gata2/3����ʹѪϸ�������Ի������Ѫת¼���ӵ�m RNA�����������½�����Ѫ�ܰͺ�������Ѫϸ�������ʾ��½�������۾�ĵ��(C.hongkongensis)�У�Gata4��������������ݿ˵���Hsp70�ı������Ѫϸ�����ý�Gata4,Hsp70�ı��������ߣ�˵��GATA4��Hsp70��ת¼��������[64]����Щ�о�������GATAת¼���������嶯��Ѫϸ�����ɺ�ά���о�����Ҫ���á�
������1 ���������߳��GATA�����Ա���书��
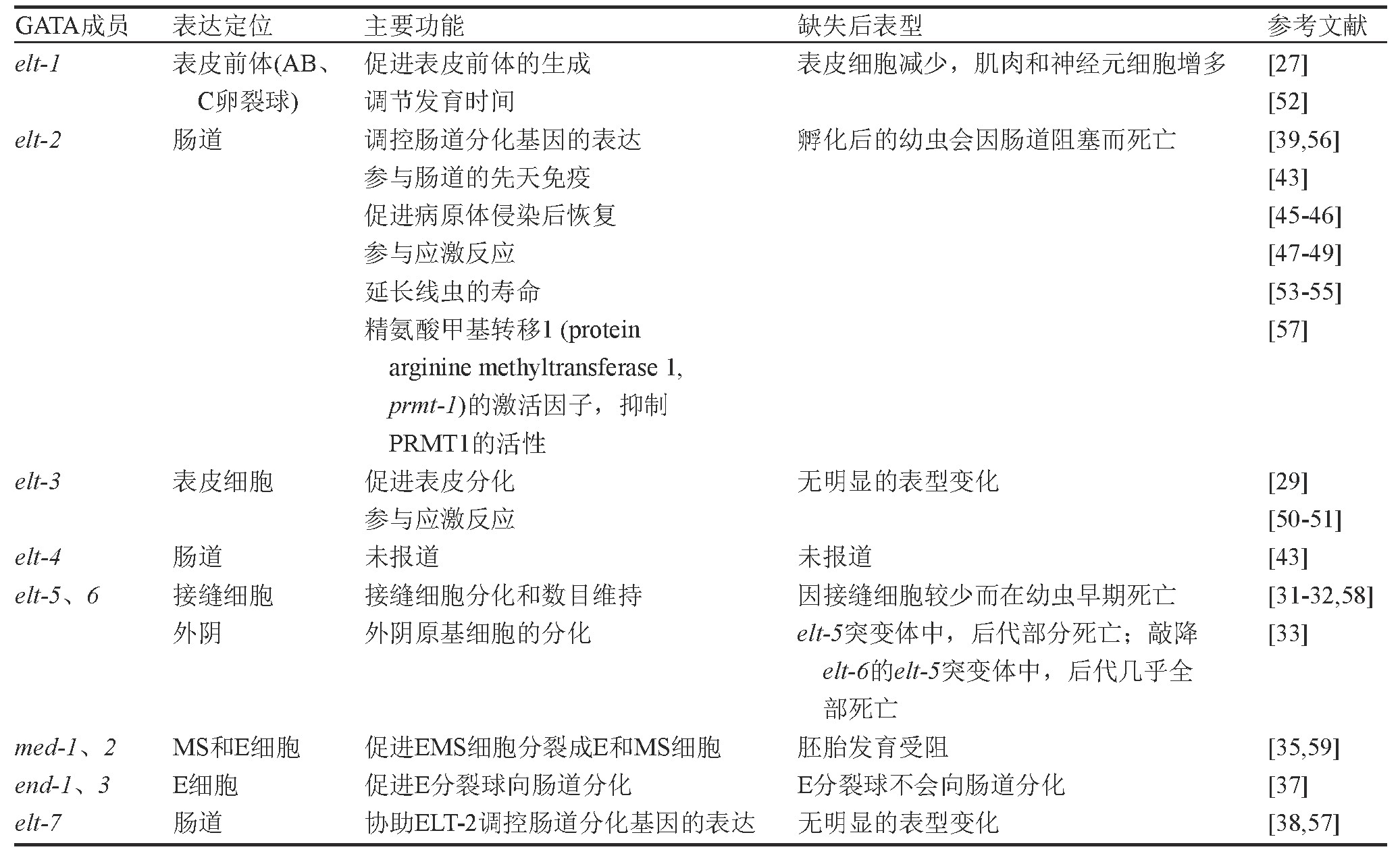
�����ڳ�ĵ��(C.gigas)�У��о���Ա����Gata2/3�ڷ��������еĶ�λ�������о�����������D���׳�α����ڱ��DZ�Ե���׳渹��[65];Gata2/3�ڱ����ᷢ���еĶ�λ��ʾ�����ڷ�����7.5 h���׳汳�����[66]����������������Ʋ⣬GATA2/3���˲�����Ѫ�����⣬�����ܲ����˳�ĵ��(C.gigas)�ı�����Ϳǵ��γɡ�
����2.6�� ��֫����
������Ӭ(D.melanogaster)��Ŀǰ������5��GATA�����Ա���ֱ�ΪGATAa (pannier,pnr)��GATAb (serpent,srp)��GATAc (grain,grn)��GATAd��GATAe[24]��������������ʾ��Grn����GATA1/2/3�Ǽ��壬��������GATA4/5/6�Ǽ���[18]���ṹ������ʾ��GATAd��GATAe������һ��C�˵�пָ�ṹ��[5]��GATA�����Ա��Ҫ�ڹ�Ӭ�����ٷ����ͷֻ��з������á�
����pnr����̥���ڱ����ڱ���Ƥ�ͽ�������Ϊ��Ĥ������[67]��ԭ����ʱ�ڣ�pnr���ý����¹�Ӭ�ı������ܱպ�[68,69]���ڸ�ë���������У�Fromental-Ramain��[70]������Pnr����������(Pnr-α��Pnr-β)��Pnr-β�ڳ�ԭ�������Ĵ���������������벿λԭ����achaete/scute�ı������������Ӻϱ���pnr-βʱ����ë�������ᷢ���仯[70]����Pnr-α�ı������쵽Pnr-β�������࣬���ܼ���Wingless�ı���[71]��
��������̥�Σ�pnr��ȱʧ�ᵼ���ļ�ϸ�����İ�ϸ���ֻ�ȱ�ݣ����ڷ����߲�(pan-mesodermal)������pnr���յ���λ������ϸ���IJ�����˵������������ϸ���γɵ���Ҫ��������[72,73]����pnr�Ӻ�ͻ��ijɳ��У��������ѹ�����и��ߵ������ԣ�����pnr�ļ�������ά�ֳɳ��������������������Ҫ[74]��
����Srp��Ҫ��ѪҺ(��Ѫ)�����������߲�֬�����з������á���Ӭ(D.melanogaster)��ԭѪϸ���������β�����һ����̥���ڵ�ͷ�����߲��У�Ѫϸ��ԭ���ֻ��ɽ�ĸϸ���;���ϸ������ʱ��srp�ı��ﱻ������ͷ�����߲�[75]����srpͻ�����У�Ѫϸ�������ɴ���ȼ��٣�������ȫ��ʧ��˵��Srp��Ѫϸ��ԭ���γɵı�������[75,76]����Ѫϸ��ԭ���ֻ�Ϊ��ĸϸ���;���ϸ���Ĺ����У�Srp�ֱ���Ϊ����ϸ����ʧ���ӻ���(glial cell missing,gcm)�������ۻ���(lozenge,lz)�ļ�������������ά�ֽ�ĸϸ���;���ϸ���ķֻ�[77,78]���׳���ܰ�����ԭѪϸ�����ɵĵڶ��Σ�������̥Ѫϸ���ֻ��е��������ƣ�Srp����lz/gcm������Ѫϸ���ֻ�[79]�����⣬pnr��ΪSTAT�����ΰл�������ܰ����н�ĸϸ���ķֻ�[80]��
�������GATAת¼���Ӳ����г�����̬�����ͷ���������̥ʱ�ڣ�GATAe��SrpЭͬ�����г��ķֻ���srpͻ�����У��г���ǰ��������ǰ���������ɺ�[81];GATAe�Ļ����Ĭ��ʹ�г��ֻ���־����ı�������[82]���׳�ͳ����srp���г��ı�����ʧ����GATAe�ı��������������ڳ����г��У�GATAeά���г���Ƥϸ������̬���������ܡ���������ı����Լ���ϸ������ֳ�ͷֻ�[82]��GATAe��������С�ܵķ�����GATAe���ý�ʹ��С��ϸ����ֳʧ�أ�������������°��ؼ�����������ӣ�������������[83]��˵��GATAe����С���������ƺ�ϸ���������������ӡ�grn����̥������11��(�ܾ���7 h)���ڳ����б��һֱ��������̥������ȫ������δ�й����о�[84]��
������֬���巢�������У�srp��ͻ��ʹ֬����ǰ��ϸ�����������ֻ�Ϊ֬����ϸ��[85]�������߲������srp���յ���λ֬����ϸ��������[86]��˵��Srp��֬����ϸ���ֻ���ϸ�����˾���������Ҫ���á����⣬SrpҲ��Ϊ֬������������Cecropin A1��ת¼�������Ӳ������߷�Ӧ[87]��
����GATA1/2/3�Ǽ����grnҲ������һЩ��Ӭ(D.melanogaster)�ķ������̡�grnͨ�����ƾֲ�ϸ��������Ӱ��������״������grnͻ�����У���Ӭ(D.melanogaster)���ȱ�̣�������Բ���α�ɱ���[88]��Grn��Even-skippedЭͬ����Unc-5���壬���ر����˶���Ԫ����ͻ����[89]��
�����ڸ���ӬGATA�����Ա�ı��P�����ܽ����2��
������������֫�����У�Ҳ������һЩGATA����Ĺ����о�����GATA��������ѻƵ���ԭ����(vitellogenin,vg)�ĵ��ء�������Ѫ��(Haemaphysalis longicornis)��GATA���Ҳ�(Bombyx mori)��GATAβ4�Ͱ�������(Aedes aegypti)��GATAa���ý�ʱ��vg�ı��ﱻ�������ƣ�˵��������vg��ת¼��������[94,95,96]���ڰ�������(A.aegypti)�л�����GATAr��������vg��ת¼[97]����ijЩ������GATA��Ա������Ѫϸ������ֳ�ͷֻ���������ˮ����(Anopheles aquasalis)�У�srp���ý�ʹѪϸ������ֳ�ͷֻ�����[98]�����л�����з(Eriocheir sinensis)�м�����һ��GATA-likeת¼����(Es GLP)�����ý�������Ѫϸ����Ŀ������Ѫϸ��������������[99]���Ҳ�(B.mori)��GATAβ������GATAβ1��3�������ͣ�GATAβ1��λ����ֳ�٣��������ѻ�ǰ�ڵ����ɡ�����ϸ���ĺ��ڷ�������ëĤ������GATAβ2���׳��Ӽ�ڱ��GATAβ3ֻ��Ӽ�ڱ���[100,101]��
����2.7 ����Ƥ���β�������ͷ������
�����ڼ�Ƥ������ɫ��(Strongylocentrotus purpuratus)����GATAc��GATAe����GATA�����Ա���ֱ��뼹�����GATA1/2/3��GATA4/5/6�Ǽ���ͬԴ[25,26]��GATAc���������������ͣ�GATAc��������Ҫ����������ϸ��ǰ��ͳ�����ǻϸ���У������������׳�����߲��б���[102,103]����ԭ�����������У�Gatac���ý���Ӱ����ǻϸ��(blastocoelar cell)Ǩ�ƺ�����ЧӦ����ı���[103]��Gatae�������ڱ���������ֲ�K��ԭ����ʱ�����߿״�����⾵�׳�ʱ�����г������Լ����������˵����߲�������ĩ����Ҫ���г�����ǻ���б���[25]��Gatae�������߲����ı�������׳�����ϸ���ֻ��Ļ�������У�Gcm����Gatae��ɫ��ϸ��ϵ�б��������������ý�������������׳�[104,105]�����⣬��ȱ��в���£�Gatae�ı����������Ž��ͣ�˵���������Ϊ����(S.purpuratus)ȱ��в�ȵ���������ָ��[106]���ڷ´̲��з��֣�GATA1����Ѫ��֯ˮ�Ρ��������Һ�ϸ�����б���[107]��
�����ڼ������ﺣ��(Ciona intestinalis)��ֻ���������Gataa���ڷ�������Gataa��ĸ��ת¼������̥�о��ȱ��64ϸ��������[108]��Western blot�����ʾ��GATAa�ĺ������ܾ��ѵ�4ϸ�����������ߣ�������ĸϵm RNA��������Ľ��[109];16ϸ���ڣ�Gataa�ĺ���ת¼����ʼת¼����32ϸ���ڣ�GATAa����K��Zic L�ı��ָ�����K�ֻ�Ϊ���߲㡣GATAa��β-catenin (ָ��ֲ�K�ֻ�Ϊ���߲�)�����ʹ������̥���߲�˳���ֻ�[110]��Ȼ�������ý�Gataaʱ�����K����������ܱ������GATAa����β-catenin�е������������ϣ����ٽ���Щ������ֲ�Kϸ���еļ��˵��GATAa�Ĺ��ܲ�����������16ϸ���εĶ����ֲ�K�м����ض�����ı������������ĺ��ӻ������ת¼��Ҳ����Ҫ����[111]���ڰ����IJ���(Branchiostoma belcheri)��ԭ���ߺ������У�Gata123�����������߲㣻���������ѵ�����ʱ�ڣ��������Ҫ���������Ѻ�βѿ�������ݺ��������в�Ҳ�����ı���[112]��
������2 �ڸ���Ӭ��GATA��Ա�ı��P����
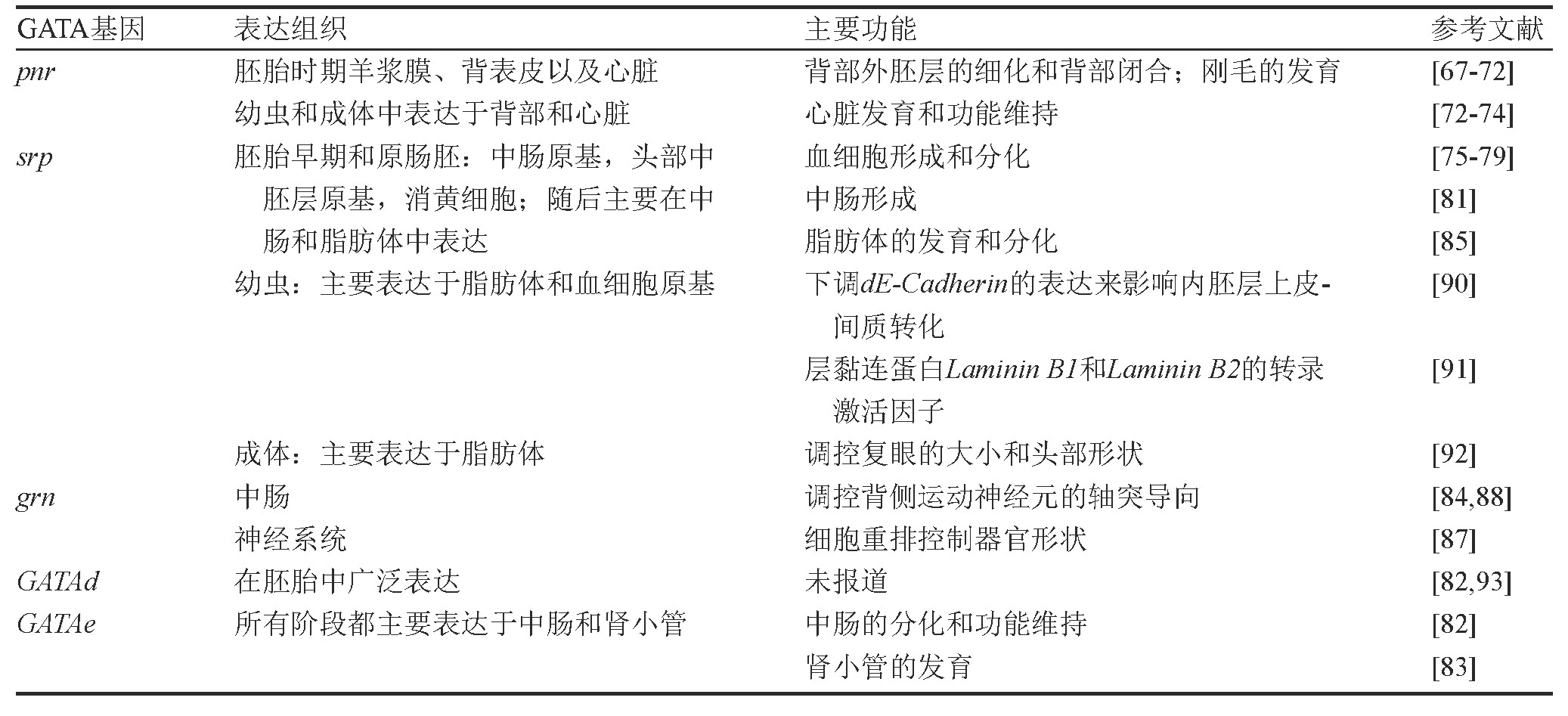
����3 ��������GATA����Ľ���
�������������У�GATA����Ľ����о���Ҫ������ԭ�ڶ����֫�����ź��߳涯�����Լ���ڶ��LƤ�����š�β���������ź�ͷ���������š��̰������н���һ��GATAת¼���ӣ���������Գƶ����У�GATAת¼���ӵ������������������ҷ�����GATA1/2/3��GATA4/5/6�Ǽ��塣��ѧ���Ʋ⣬�ڴ̰�����������Գƶ�������Ĺ����У���һ��GATA����ת¼���Ӱ������߲�ֻ��������ƣ�����������Գƶ�������“urbilaterian”�г���������ͬ��GATAת¼����[16,21,25]����֫�����о��ж��GATA4/5/6�Ǽ����Ա����ֻ��GATA4/5/6�Ǽ��巢�������š�ͨ��ϵͳ�����ͻ�������������ȷ��GATA4/5/6���ų�ba�͡�a�ͺ�bb��(���������ַ�Ϊbba��bbb��)���࣬����ba�͡�a�ͺ�bb��(�����е�bba)��ͬһȾɫ���ϴ������У�����о���Ա��������Ǵ������ƽ�������������ṹ������ʾ��bbb��GATA��Ա��������������ж�ʧ�˵�һ�����ӣ����а�������N��пָ�ṹ������У�˵��������GATA��������Ż��Ƹ�����[18]�����߳���ֶ�����������У�GATA4/5/6�Ǽ����Ա���֫�������ƣ�Ҳ�д�����������������������ʾ����֮���GATA4/5/6�Ǽ����Ա������Ϊһ֧��˵����֫����߳���ֶ���֮�����Ե��ϵ��Զ����Ƥ���β�������ͷ�������е�GATA��������뼹�����Ϊһ�࣬��Ҫ������Ⱦɫ��ӱ��������ȫ�����鸴��[13]��
����4 ���ܽ���չ��
������Ŀǰ���о���������ȻGATA�������������еij�Ա��Ŀ��ͬ��������ʽ��һ�¡��о������Ҳ������𣬵��������߲�ֻ��е������DZ��صģ����߲�������ٵķֻ�����ά��ϢϢ��ء�Ȼ����GATA������Ϊ�߲㷢���ı��ص������ӣ����о��ϻ�����������ؽ�������(1)������ͳһ�������������GATA�����Ա������ͳһ�Ĺ�����˸���ʾ��ͬ���ּ����Ա֮���ͬԴ��ϵ�����һ�������ѣ�(2)�о�ȱ����ȣ����������д����ֵ��о�ͣ���ڱ�������������ijһ����ij�������̽��������������ԭ������̽��GATA���幦�ܱ������Լ�����������GATA����Ľ������ɷ����Ѷ����ӡ���ʵ�����ں��������ﵥ����Μ(Urechis unicinctus)���״η���GATA4/5/6�Ǽ����GATA B2���������л���أ�����Ϊת¼�������ӵ������л�ؼ���������������ԭø(Sulfide:quinone oxidoreductase,sqr)��ת¼������Western blot��ⷢ���䵰����������Ӧ������������[113]��GATA�����о���Ȼ������������δ��������о������뷢������������ѧ����ҲԽ��Խ�࣬����ͨ���о���Ա�IJ���Ŭ������GATA����Ĺ��ܺͽ������棬���������������е��о���Խ��Խ�ḻ��
���������
����[1] Patient RK, McGhee JD. The GATA family(vertebrates and invertebrates). Curr Opin Genet Dev, 2002, 12:416-22
����[2] Merika M, Orkin SH. DNA-binding specificity of GATA family transcription factors. Mol Cell Biol, 1993, 13:3999-4010
����[3] Evans T, Reitman M, Felsenfeld G. An erythrocytespecific DNA-binding factor recognizes a regulatory sequence common to all chicken globin genes. Proc Natl Acad Sci USA,
����1988, 85:5976-80
����[4] Tsai SF, Martin DI, ZonLI, et al. Cloning of cDNA for the major DNA-binding protein of the erythroid lineage through expression in mammalian cells. Nature, 1989,339:446-51
����[5] Lowry JA, Atchley WR. Molecular evolution of the GATA family of transcription factors.conservation within the DNA-binding domain. J Mol Evol, 2000, 50:103-15
����[6] Tremblay M, Sanchez-Ferras O, Bouchard M. GATA transcription factors in development and disease .Development, 2018, 145:dev164384
����[7] Whitcomb J, Gharibeh L, Nemer M. From embryogenesis to adulthood: critical role for GATA factors in heart development and function. IUBMB Life, 2020, 72:53-67
����[8]�̽��Σ��ַ�,��÷��. GATA3�Զ��Ϸ�������ά�ֵ����ú���ʦ����ѧѧ��(��Ȼ��ѧ��), 2020, 19:496-502
����[9]��ѩ����,�Ժ�ӱ,��. FOXA2��GATA6�ڷ��ٰ��еı��P�����ٴ����������Ĺ�ϵ��ϲ���ѧ��־,2020, 27:413-7
����[10] Shen W, Niu N, Lawson B, et al. GATA6:a new predictor for prognosis in ovarian cancer. Hum Pathol, 2019, 86:163-9
����[11] LinL, Liang L, Yang X, et al. The homeobox transcription factor MSX2 partially mediates the effects of bone morphogenetic protein 4(BMP4)on somatic cell reprogramming. JBiol Chem, 2018, 293:14905-15
����[12] He C, Cheng H, Zhou R. GATA family of transcription factors of vertebrates phylogenetics and chromosomal synteny. J Biosci, 2007, 32:1273-80
����[13] Gilis WQ, St John J, Bowerman B, et al. Whole genome duplications and expansion of the vertebrate GATA transcription factor gene family. BMC Evol Biol, 2009, 9:207
����[14] Leininger S, Adamski M, Bergum B, et al. Developmental gene expression provides clues to relationships between sponge and eumetazoan body plans. Nat Commun, 2014.
����5:3905
����[15] Nakanishi N, Sogabe S, Degnan BM. Evolutionary origin of gastrulation:insights from sponge development. BMC Biol, 2014, 12:26
����[16] Martindale MQ, Pang K, Finnerty JR. Investigating the origins of triploblasty:'mesodermal gene expression in a diploblastic animal, the sea anemone Nematostella vectensis(phylum, Cnidaria; class, Anthozoa). Development, 2004, 131:2463-74
����[17] Boyle MJ, Seaver EC. Expression of FoxA and GATA transcription factors correlates with regionalized gut development in two lophotrochozoan marine worms:Chaetopterus(A
����nnelida)and Themiste lageniformis(Sipuncula). Evodevo, 2010, 1:2
����[18] illis WQ, Bowerman BA, Schneider sQ. The evolution of protostome GATA factors:molecular phylogenetics, synteny, and intron/exon structure reveal orthologous relationshi
����ps. BMC Evol Biol, 2008, 8:112
����[19] Flores NM, Oviedo NJ, Sage J. Essential role for the planarian intestinal GATA transcription factor in stem cells and regeneration. Dev Biol, 2016, 418:179-88
����[20] Martin-Duran JM, Romero R. Evolutionary implications of morphogenesis and molecular patterning of the blind gut in the planarian Schmidtea polychroa. Dev Biol, 2011,352:164-76
����[21] Gllis WJ, Bowerman B, Schneider sQ. Ectoderm- and endomesoderm-specific GATA transcription factors in the marine annelid Platynereis durmeilli. Evol Dev, 2007, 9:39-50
����[22] Wong KS, Arenas-Mena C. Expression of GATA and POU transcription factors during the development of the planktotrophic trochophore of the polychaete serpulid Hydroides
����elegans. Evol Dev, 2016, 18:254-66
����[23] Yue F, Zhou Z. WangL, et al. A conserved zinc finger transcription factor GATA involving in the hemocyte production of scallop Chlamys freri. Fish Shelfish Immunol, 2014.39:125-35
����[24] Okumura T, Matsumoto A, Tanimura T, et al. An endoderm specific GATA factor gene, dGATAe, is required for the terminal diferentiation of the Drosophila endoderm. Dev BioI, 2005, 278:576-86
����[25] Lee PY, Davidson EH. Expression of Spgatae, the Strongylocentrotus purpuratus ortholog of vertebrate GATA4/5/6 factors. Gene Expr Patterns, 2004, 5:161-5
����[26] Howard-Ashby M, Materna SC, Brown CT, et al. Gene families encoding transcription factors expressed in early development of Strongylocentrotus purpuratus. Dev Biol,200
����6, 300:90-107
����[27] Baugh LR, Hill AA, Claggett JM, et al. The homeodomain protein PAL-1 specifies a lineage specific regulatory network in the C. elegans embryo. Development, 2005,132:184
����3-54
����[28] Gilleard JS, McGhee JD. Activation of hypodermal diferentiation in the Caenorhabditis elegans embryo by GATA transcription factors ELT-1 and ELT-3. Mol Cell Biol, 2001, 21:2533-44
����[29] Smith JA, McGarr P, Gilleard JS. The Caenorhabditis elegans GATA factor elt-1 is essential for differentiation and maintenance of hypodermal seam cells and for normal locomotion. J Cell Sci, 2005, 118:5709-19
����[30] Cassata G, Shemer G, Morandi P, et al. ceh-16/engrailed patterns the embryonic epidermis of Caenorhabditis elegans. Development, 2005, 132:739-49
����[31] Gorrepati L, Thompson KW, Eisenmann DM. C. elegans GATA factors EGL-18 and ELT-6 function downstream of Wnt signaling to maintain the progenitor fate during larval a
����symmetric pisions of the seam cells. Development,2013, 140:2093-102
����[32] Gorrepati L, Eisenmann DM. The C. elegans embryonic fate specification factor EGL-18(GATA)is reutilized downstream of Wnt signaling to maintain a population of larval progenitor cells. Worm, 2015, 4:e996419
����[33] Koh K, Peyrot SM, Wood CG, et al. Cell fates and fusion in the C. elegans vulval primordium are regulated by the EGL-18 and ELT-6 GATA factors apparent direct targets of the LIN-39 Hox protein. Development, 2002, 129:5171-80
����[34] Liu WJ, Reece-Hoyes JS, Walhout AJ, et al. Multiple transcription factors directly regulate Hox gene lin-39expression in ventral hypodermal cells of the C. elegans embryo and larva, including the hypodermal fate regulators LIN-26 and ELT-6. BMC Dev Biol, 2014, 14:17