����ժ Ҫ�� ��Ŀ�ġ��Ż�С��������ȡ�����������ڳ���ЧҺ��ɫ��-�������������õ�С�����ռ�ⷽ��������������С��Ʒ��‘��ũ6��’Ϊ����,����������ȡ���ͳ������������ݷ�������ȡ������ȡС������,���ó���ЧҺ��ɫ��-�������������ü��С��������6��С�����յ���Ժ������������ʹ��80%�Ҵ���Ϊ��ȡҺ�����ϱ�1��20��40�桢40 KHz������ȡ90 min,��ȡЧ�ʽ�������ȡ��ƽ��Ч��Լ��10%������C18��(2.1 mm×50 mm,1.8μm),������0.1%����/ˮ(A)������(B),��ϴ������Ϊ10%������100%����5 min�����ݶ�ϴ��,����25��,����0.4 mL/min;�����ѹ3 500 V��Դ�¶�350����������롢����35 psi����������10 L/min,��5 min���ڿɿ������6��С�����ռ�⡣�����ۡ��������������ݷ������С��������ȡ��,������ȡʱ��,�����ܼ�����;�Գ���ЧҺ��ɫ��-�������������ü��С�����յ�ϴ���ݶȽ����Ż�,���ټ��С�����ա�
�����ؼ��ʣ���С������; ��ȡ����; ����ЧҺ��ɫ��-����������;
����Abstract������Objective�� Optimization of extraction and assay method for adzuki bean saponins by Ultra Performance Liquid Chromatography-Electrospray Ionization Mass Spectrometric. ��Methods�� Azukisaponins were extracted from Jingnong 6 variety of adzuki bean by Soxhlet extraction and Ultrasonic-assisted extraction. The relative content of six azukisaponins in adzuki bean seed were assayed by Ultra Performance Liquid Chromatography-Electrospray Ionization Mass Spectrometric method. ��Results�� Using 80% aqueous ethanol as the extracting solution, 20��1 as the efficiency ratio of solvent to the seed powder, 40 �� and 40 KHz ultrasonic extraction for 90 min, the total azukisaponins was 10% higher than that of Soxhlet extraction. The mobile phase of Agilent C18 column(2.1 mm×50 mm,1.8 μm) was 0.1% aqueous formic acid(A) and acetonitrile(B). The simplified elution conditions were linear gradient elution from 10% acetonitrile to 100% acetonitrile for 5 min. The column temperature was 25 ��, and the flow rate was 0.4 mL/min. The instrument was operated at an ionization voltage of +3500 V and source temperature of 350 ��. Nitrogen was used as nebulizer gas at 35 psi and drying gas at a flow rate of 10 L/min, within 5 min to complete the separation and detection of six azukisaponins. ��Conclusion�� Ultrasonic-assisted extraction method can increase the extraction rate, reduce time and solvent. The gradient elution of azukisaponins by Ultra Performance Liquid Chromatography-electrospray Ionization Mass Spectrometric method were optimized, and azukisaponins are rapidly assayed.
����Keyword����azukisaponins; extraction method; ultra performance liquid chromatograph mass spectrometer;
����С��(Adzuki bean,Vigna angularis),�׳ƺ�С�����ඹ����С��,��Դ���й�,������ʷ�ƾ�[1]��ȫ����30���������ֲС��,�й�������������ܲ�����������λ[2,3]��С��Ӫ���ḻ,�������ơ���ӡ����ͪ������������ʡ�����������ֲ�����������Ϳ�������Ҫ����,ֲ�����ѷ���20 000�������������[4,5];���ƻ����п�ѪС�塢�������������������͵��̴���������Ϊ������������������,��ҽҩ�����ͱ����������Žϴ��Ӧ��DZ��,��������Ϊ�����������ҽҩ�о������ע���ȵ�֮һ[6,7]��

����С���е�������������ʪ�����ס�������Ҫ���Գɷ�[8]���ѱ���С������10��С������[9,10,11];���е�4����������2,3-����-3,5-���ǻ�-6-��-4H-���-4-ͪ����(2,3-dihydro-2,5-dihydroxy-6-methyl-4H-pyran-4-one,DDMP),�����ȷֽ�������ȡ����[10],��������о����١��ѷ����6��С�����վ�������չ����͵����ƻ�����,�ֱ���С������I(Azukisaponin I)��С������II(Azukisaponin II)��С������III(Azukisaponin III)��С������IV(Azukisaponin IV)��С������V(Azukisaponin V)��С������VI(Azukisaponin VI)[9];���ǵ�����ȡ�����֬��ø��������������,��������α-������ø���Ե��������ڴ��̶������������������㶹���϶���С�ⶹ[12]��
����С��������ȡ������������ȡ���ͽ��ݷ�[8,12,13],�����ܼ����Ĵ��ո��ӡ��ɱ��ߡ�������������������ȡ���б����������������ݷ�����Ч�ʸߡ�ʱ��̡��ɱ�����������������ŵ�[14],�÷�����Ӧ����С�ⶹ�������ȶ��ͺ�«�͵���������ȡ[15],����С����δ�����Ӧ�á��������״ΰѳ������������ݷ�Ӧ����С��������ȡ,����������ȡ���ͳ������������ݷ�����ȡЧ�ʽ��бȽϡ�
��������С������I��С������II��С������III��С������IV��С������V��С������VI��6��С������û�б�Ʒ����,���ֱ���,��漵�����չ���Ϊ��Ʒ,��������ֹ��ȷ��ⶨС�������պ���[8],��������6��С�����յĽṹ����,�������ղ������,����ֹ��ȷ���������һ����������������Һ�����ü��С������[13],����δ���ó���ЧҺ�������DzⶨС�����յı�����������ο�Һ�����òⶨ����,���س���ЧҺ�����ü��С������,�Ż�ϴ���ݶȺ�����,����Ч�ʡ�С�����յ���ȡ����Ʒ�Ʊ��ͳ���ЧҺ�����ü�ⷽ�����Ż�,��ΪС��������Դ��С�����ճɷֺ����ⶨ��С�����ոߺ���������Դ��ɸѡ������Ӧ�á�С�����մ�л;������������á�С������ҩ���о��ṩ��Чʵ�õļ�⼼��������
����1 �������뷽��
����1.1 ���� ��
����С��Ʒ��‘��ũ6��’,�ɱ���ũѧԺѡ����
����1.2 ���� ��
����1.2.1 ��ĥ��
�����ø������ܷ����(YW-100,�����̩˹����������˾)��‘��ũ6��’����ĥ��(1 200 r/min),��ɸ(150 μm),40 ����������,���á�
����1.2.2�� ��Ʒ��Һ���Ʊ�
������ȡ 0.40 g��������10 mL�Թ���,���� 8 mL 90% �״�,40 �桢40 KHz������ȡ90 min(PS-60AD,�����пƽ೬���Ƽ�����˾),��ȡҺ0.45 μmĤ���˺���������ȡ1.00 g���۷�����ֽ����,����ֽ��������ȡ����,��250 mLԲ����ƿ�м���100 mL�״�������ȡ3 ��(ÿ��1 h ),��ת������(RE-2000E,�Ϻ��ޫh��������˾)��ת��������,�ü״��ܽⲢ������20 mL,0.45 μmĤ���˹���������
����1.2.3�� ɫ������������
�����ⶨ����Ϊ�����ļ���Һ��������(Agilent 1290-G6470),��ϵͳ�䱸Agilent ZORBAX RRHD Eclipse Plus C18��2.1 mm×50 mm,1.8 μm, ������Ϊ0.1%����/ˮ(A)������(B)����ϴ������Ϊ10% ������100% ���� 5 min�����ݶ�ϴ�ѡ�����25 ��,����0.4 mL/min,������1 μL������������(electrospray ionization-mass spectrometric,ESI-MS)����,���õ����ѹ3 500 V,Դ�¶�350 �����������;����35 psi,�������� 10 L/min,������ģʽ�¶�m/z760��m/z1140����ȫɨ��(MS2 scan)����ѡ�����Ӽ��(SIM,Selected Ion Monitoring)��ⷽʽ��,���������ȡ����������ȡ��ķ������ӡ�����Ƭ����ɨ��(Product Ion Scan)��ʽ��,�����ȡ�����Ƭ���ӡ�
����2�� ��������
����2.1�� С�����շ������Ӷ��Է���
��������6��С�����յķ�����,ȷ����ȡ���д���С������I��С������II��С������III��С������IV��С������V��С������VI,��С����ȡ��ij���ЧҺ��ɫ��-����������(Ultra Performance Liquid Chromatography-electrospray Ionization Mass Spectrometric,UPLC-ESI-MS)��������ɫ��ͼ�б��С�����յ�6����(ͼ1)����ϴ��������,5 min����ɼ��,��ʡ�����ಢ����Ч�ʡ�
����ͼ1 С����ȡ���UPLC-ESI-MS������ɫ��ͼ
����Fig.1 UPLC-ESI-MS total ion chromatograms of adzuki bean total extract
����ע:1��С������IV;2��С������VI;3��С������V;4��С������II;5��С������I;6��С������III��
����Note:1 is Azukisaponin IV; 2 is Azukisaponin VI; 3 is Azukisaponin V; 4 is Azukisaponin II; 5 is Azukisaponin I; 6 is Azukisaponin III.
����2.2 ��С��������Ƭ���Ӷ��Է���
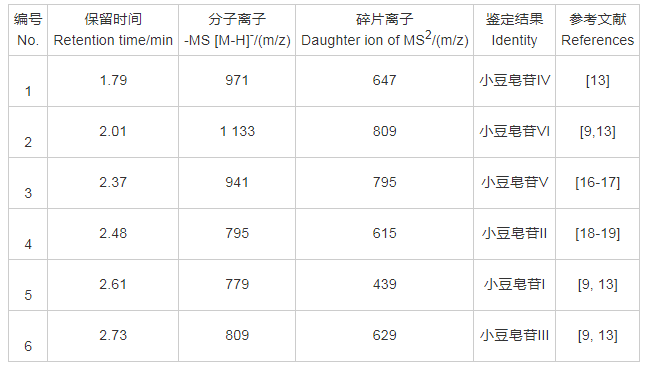
����ͨ���Ƚϱ���ʱ�䡢UPLC-ESI-MS ����(ͼ1)��ESI-MS2(ͼ2),��1��С������IV;��2��С������VI;��3��С������V;��4��С������II;��5��С������I;��6��С������III(��1)��
������1 С���м���6��С�����յ�UPLC-ESI-MS2����
����
����2.3 ��������ȡ��������Ժ�������
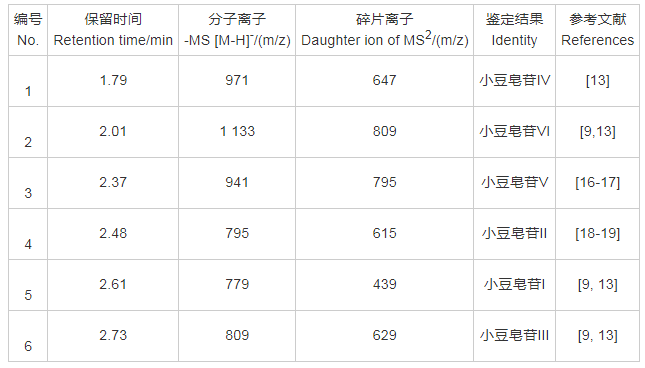
������ѡ�����Ӽ�ⷽʽ����С�����ջ������Ϊ����ָ��,�������������ݷ���ȡ��6��С�����յĵ�������������ȡ��,��ȡʱ�䡢��ȡҺ���С��������ȡ��(��2)�����ó������������ݷ������С�����յ���,������ȡʱ��,��ʡ�ܼ���
������2 �������������ݷ���������ȡ���ıȽ�(n=6)
����3�� �� ��
����������ȡ�����е��ʸߡ�ȷ���ص�,��������ȡ����ȡʱ�䳤�ͳɱ���,����Ӧ���ڴ�����������ȡ��������Ƚ�������ȡ���ͳ������������ݷ��ĵ���,�����������������ݷ���ȡ��6��С�����յĵ�������������ȡ��,��ʡʱ���ɱ��͡���������,�ʺ����ڴ��ģ������Դ������С�������Ʊ���ȡ��
����ͼ2 6��С����������ͼ
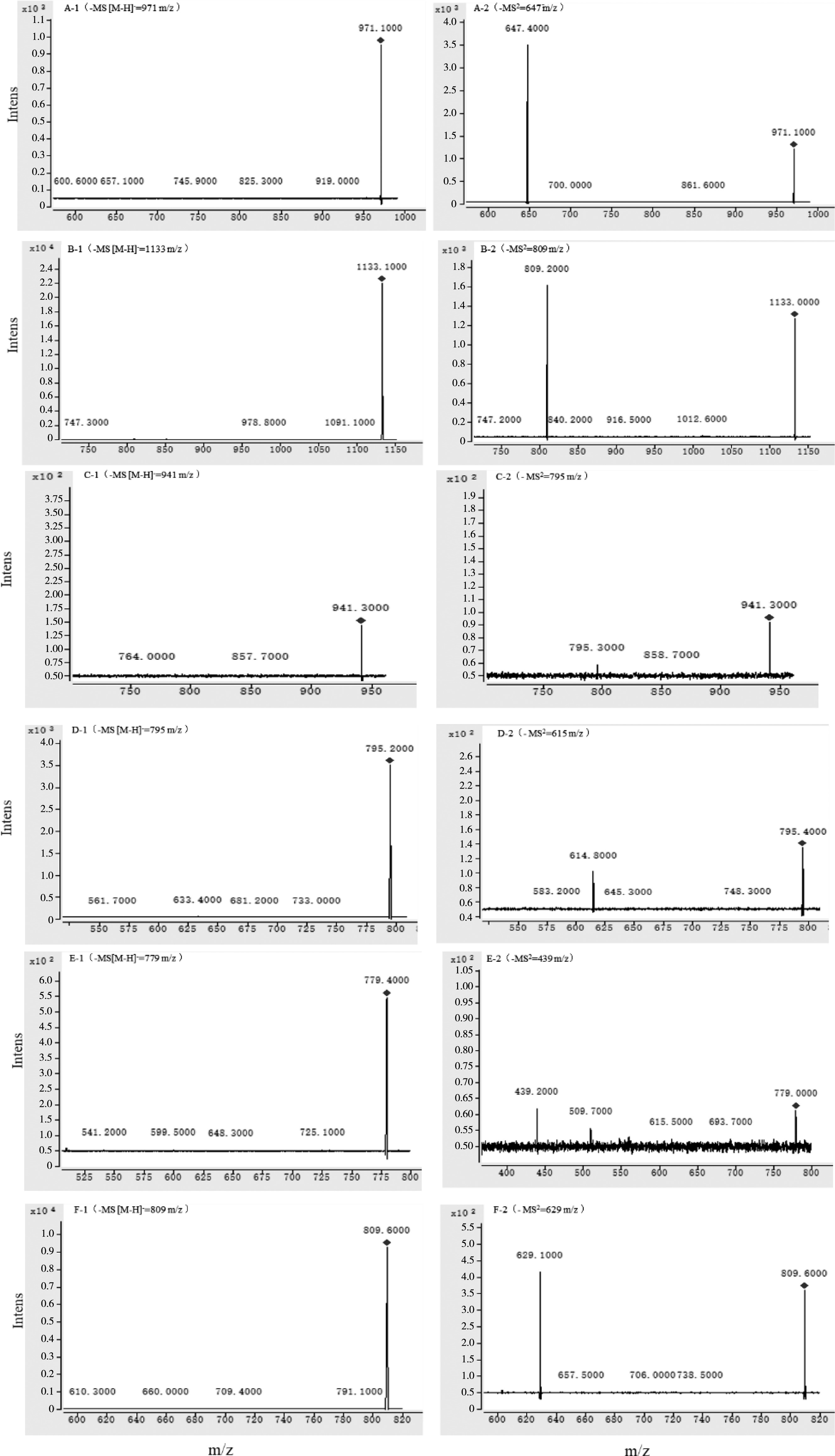
����Fig.2 ESI (-) MS, MS2spectra of identified six azukisaponins in adzuki bean
��������,��ЧҺ��ɫ����ʼ�㷺�������������Ķ����Ͷ��Է�����[20]��Liu��ʹ��Agilent 1100ϵ�и�ЧҺ��ɫ���Ǽ��9��С�����ͪ��6��С������,ʹ��10 mmol/L����狀���������ݶ�ϴ�ѡ���ʼ����Ϊ10%���� 10 min,30 min ��Ϊ15%����,45 min��Ϊ25%����,55 min��Ϊ35%����,60 minʱ45%����, 70 minʱ55%���档����ʱ��Ϊ90 min,����С�����շ���ʱ��Ϊ25 min[13]��������ʹ��Agilent 1290-G6470�����ļ���Һ��������,��ϴ������Ϊ10% ������100% ����10 min�����ݶ�ϴ��,��5 min����ɶ�6��С�����յķ��뼰�ⶨ,��������Ч�ʡ�
���������齨��С������������������ȡ6��С�����յķ�����ȷ������ЧҺ�����ü��6��С�����յķ���,ΪС��������ȡ�������Ʊ��ͼ���ṩ��Ч��������,Ϊ��һ��ɸѡС�����ոߺ�����������Դ������ǿ�����������Լ���ز�Ʒ�Ŀ����춨������
���������
����[1] �Բ�,Ҷ��,������,������,�ⱦ��,��ܾ�,�˽�,��ƽ.��ͬ����С������SSR����Ŵ������Լ���״��������[J].�й�ũҵ��ѧ,2011,44(4):673-682
����[2] Kramer C,Soltani N,Robinson DE,Swanton CJ,Sikkema PH.Control of Volunteer Adzuki Bean in Soybean[J].Agricultural Sciences,2012,3(4):501-509
����[3] ����,�Բ�,������,������,�����,������ķ,�,��ƽ.Ұ��С��������С�����ӱ�����״����[J].����ũѧԺѧ��,2017,32(4):8-13
����[4] ̷��ί.ˮ��2,3-������ϩ����ø����OsOSC7�Ĺ����о�[D].����:�й���ѧԺ��ѧ,2016
����[5] Shanmugam MK,Dai X,Kumar AP,Tan BK,Sethi G,Bishayee A.Oleanolic acid and its synthetic derivatives for the prevention and therapy of cancer:preclinical and clinical evidence[J].Cancer Letters,2014,346(2):206-216
����[6] ��ӱ,�ﺣ��,����Ƽ.������������ϳ�;���о���չ[J].�й�Ұ��ֲ����Դ,2012,31(6):15-17
����[7] ��־��.��Ƥľ������չ�����ܹ���ⶨ����ȡ�������������о�[D].�人:����ũҵ��ѧ,2006
����[8] ���,��Ө��,����,������,��ɽɽ.��ͬ���س�С�������Ƶĺ����ⶨ��Ʒ������[J].ʱ���ҽ��ҩ,2012(2):55-56
����[9] Kitagawa I,Wang H,Saito M,Yoshikawa M.Saponin and sapogenol.XXXII.Chemical constituents of the seeds of Vigna angularis (Willd.) Ohwi et Ohashi.(2).Azukisaponins I,II,III,and IV[J].Chemical & Pharmaceutical Bulletin,1983,31(2):674-682
����[10] Iida T,Yoshiki Y,Kahara T,Okubo K,Ohrui H.A saponin conjugated with 2,3-dihydro-2,5-dihydroxy-6-methyl-4H-pyran-4-one from Vigna angularis[J].Phytochemistry (Oxford),1997,45(7):1507-1509
����[11] Iida T,Yoshiki Y,Okubo K,Ohrui H,Kinjo J,Nohara T.Triterpenoid saponins from Vigna angularis[J].Phytochemistry,1999,51(8):1055-1058
����[12] Liu R.Anti-obesity effects of flavonoids and saponins from adzuki bean [D].Hong Kon:Hong Kong Baptist University,2014
����[13] Liu R,Cai Z,Xu B.Characterization and quantification of flavonoids and saponins in adzuki bean (Vigna angularis L.) by HPLC-DAD-ESI-MSn analysis[J].Chemistry Central Journal,2017,11(1):93-110
����[14] ��ǿ,��ϲ��.��չ�����ȡ���봿���������ⶨ���о�����[J].���ҩѧ,2017(6):68-71
����[15] Navarro Del Hierro J,Herrera T,García-Risco MR,Fornari T,Reglero G,Martin D.Ultrasound-assisted extraction and bioaccessibility of saponins from edible seeds:Quinoa,lentil,fenugreek,soybean and lupin[J].Food Research International,2018,109:440-447
����[16] Oshima Y,Ohsawa T,Hikino H.Structures of Dianosides G,H and I,Triterpenoid Saponins of Dianthus superbus var.longicalycinus Herbs[J].Planta Medica,1984,50(3):254-258
����[17] Avunduk S,Mitaine-Offer AC,Alanku?-Cali?kan O,Miyamoto T,Senol SG,Lacaille-Dubois MA.Triterpene Glycosides from the Roots of Astragalus flavescens[J].Journal of Natural Products,2008,71(1):141-145
����[18] Kinjo J,Hatakeyama M,Udayama M,Tsutanaga Y,Yamashita M,Nohara T,Yoshiki Y,Okubo K.HPLC Profile Analysis of Oleanene-Glucuronides in Several Edible Beans[J].Bioscience,Biotechnology,and Biochemistry,1998,62:429-433
����[19] Sakamoto S,Kofuji S,Kuroyanagi M,Ueno A,Sekita S.Saponins fromTrifolium repens[J].Phytochemistry (Oxford),1992,31(5):1773-1777
����[20] ��ȫ��,�ο���.��չ��Ậ���ⶨ���о���չ[J].�й�ִҵҩʦ,2011,8(7):32-34