����ժ Ҫ����Ŀ�� ���ۿ�Ȯ������֬���嶳�ɷ۵�����ԭ�ԡ����� ����Ȯ������ԭҺϡ����15 IU/mL,�Ʊ�Ϊϡ��Һ���ɷ�(Y1��)������ϡ��Һ���ɷ���֬���嶳�ɷ۰�5��3������Ȼ��,�Ƴ����������(Y2��)��ͬʱ���ö���-���ɷ�����Ȯ������ϡ��Һ��֬�������Ƴɿ�Ȯ������֬���嶳�ɷ�(Y3��)�����������縴�ܺ�,�ֱ���0��3��7��14��21 d��С��ǻ��ҩ,0. 5 mL/ֻ��MTT�����С��Ƣ�ܰ�ϸ����ֳ����,��ʽϸ�������T�ܰ�ϸ��������,ELISA���ⶨС����Һ�п�Ȯ����������IgG(RV-IgG)Ũ�ȡ���� ��Y1�鼰Y2��Ƚ�,Y3��������ߺ�3 dС��Ƣϸ���̼�ָ��(stimulatingindex,SI)ֵ��������(P <0. 01)���������ߺ�7��14��21��28 d,CD4+/CD8+ֵ��������(P <0. 05),�������ߺ�7��14��21 d,RV-IgGŨ����������(P <0. 05)������ ��Ȯ������֬���嶳�ɷ���С�����ھ������õ�����ԭ��,֬�����������������ԭ��,�ӳ����������ʱ��,����������Ϊ��һ���㷺Ӧ�õ�����������
�����ؼ��ʣ�����Ȯ������; ����; ֬����; ����; ����ԭ��;
����Abstract����Objective To evaluate the immunogenicity of liposome lyophilized powder of rabies vaccine. Methods The bulk of rabies vaccine was diluted to a concentration of 15 IU/mL and prepared into diluent lyophilized powder(Y1).The diluent lyophilized powder was mixed with liposome lyophilized powder at a volume ratio of 5 �� 3 to prepare a physical mixture(Y2). Meanwhile,rabies vaccine liposome lyophilized powder(Y3) was prepared with the diluent and liposome by freezing and thawing-lyophilization. The vaccines in various groups were reconstituted and injected i.p. into mice on days 0,3,7,14 and 21 separately,0. 5 mL for each. The proliferation abilities of splenic lymphocytes of the mice in various groups were determined by MTT assay,while the surface markers of T lymphocytes by flow cytometry,and humoral anti-rabies virus IgG(RV-IgG)levels by ELISA. Results Compared with those in Y1 and Y2 groups,the stimulating index(SI)of splenocytes of mice in Y3 group 3 d after the first immunization increased significantly(P < 0. 01),while the CD4+/CD8+ ratio 7,14,21 and 28 d as well as the RV-IgG level 7,14 and 21 d after the first immunization increased significantly(P < 0. 05). Conclusion The rabies vaccine liposome lyophilized powder showed good immunogenicity in mice. The liposome enhanced the immunogenicity and prolonged the time duration of immunity of the vaccine,which was expected to be a widely used novel adjuvant.
����Keyword����Rabies vaccine; Lyophilization; Liposome; Adjuvant; Immunogenicity;
������Ȯ����һ�ִ�Ⱦ��ǿ�������ʸߵ����Դ�Ⱦ������ʱ����������Ԥ����Ȯ�������ʹ�Ⱦ����Ч;�����������Ʊ��У�������ѡ����Ӱ������ʹ��Ч������Ҫ���ء�Ŀǰ�������е���������������������[1,2,3,4,5]�����������[6]�����ߴ̼������ISCOMS������[7,8]��MF59����[9,10,11,12]��AS03��������[13,14,15]��AS04��������[16]�ȣ���Щ�����е���������ǿ��������ԭ�ԣ�ͬʱҲ����һЩȱ�㣬���յ��������͵�һ[17,18,19,20,21]���Ի���ı���������[22]��������Ӧ�����أ�������Ⱥ���ޣ����䡢��������Ҫ���ϸ�����ɱ���[11]�ȡ�֬������ģ������Ĥ��˫���Ӳ�ij���״���������������˫��Ĥ�ṹ���ɽ����������Ĥ�ڣ����������ܵ��ƻ����䲻������Ϊ�������������������ԭ�ԣ�������Ϊ�������������[23]�����⣬֬�������Ҫ�ɷ���֬�����̴����ڻ����ڽ��⣬ȷ��������İ�ȫ�ԡ�
������������ǰ����֬������Ϊ�������������壬��֬���嶳�ɷ����������һϵ�������Ժ��ȶ��Լ�⣬���������֬������Ϊ����������������ǿ���������ԭ�ԣ��������������ȶ��ԣ�������������ѹ��[24,25,26,27,28,29]�������ߵ�14�죬����ԭҺ�кͿ���ˮƽ���Ե���֬�������磬��28��������кͿ���ˮƽ���ƣ���ԭ�������ԭҺ��ԭŨ�ȹ��ߣ�����֬�����������������٣�ʹ֬�����������ò�����[30]����ʵ���ڿ�Ȯ������ԭҺ���ϡ�ͱ���[31]�Ļ����ϣ����ö���-���ɷ�[24]�Ʊ�ϡ��Һ��֬���嶳�ɷۣ������������ԭ�ԣ�ͬʱ���Ȯ������ϡ��Һ���ɷۼ���Ȯ������ϡ��Һ���ɷ���֬���嶳�ɷ������������бȽϣ������ۿ�Ȯ����֬���嶳�ɷ۵�����ԭ�ԡ�
����1�� �����뷽��
����1.1 ������
��������Veroϸ����Ȯ������ԭҺ��δ����Ѫ���ף�RIFFIT���ⶨ��ԭ����Ϊ25.92 EU/mL,ELISA���ⶨЧ��Ϊ40 IU/mL�����϶������ⶨ������Ϊ22 mg/mL�������人������Ʒ�о����������ι�˾��
����1.2�� ��Ҫ�Լ�������
����RPMI1640����Һ��������HyClone��˾����̥ţѪ�壨FCS������������������Ʒ�Ƽ�����˾���������ף�ConA,SigmaC2631��װ����MTT(Amreseco793��װ�����Ա�����������\������˾����ϸ���ѽ�Һ���Ա���������Ƽ�����˾��С���Ȯ������IgG(RV-IgG)ELISA�Լ��й���ɭ��٤����Ƽ�����˾��Anti-mouse CD4 PE��12-0041��Anti-mouse CD8a FITC��11-0081����eBioscience��˾�������Լ���Ϊ���۷�������96�������幺�Խ��ս������¿�ҽ����е����˾��BIO-RAD i MarkTMø���ǹ����������ֹ�˾��Cytomics FC500MPL��ʽϸ���ǹ�������Beckman Coulter��˾��
����1.3 ��ʵ�鶯��
����SPF������С���ԣ�6��8���䣬����18��22 g����������ҽ�ƴ�ѧSPFʵ�鶯�����ģ�����ϸ�֤��Ϊ��SYSK���ᣩ2005-0004��
����1.4 ��������鼰��ҩ
����������Veroϸ����Ȯ������ԭҺϡ����15 IU/mL�������Ʊ�����ϡ��Һ���ɷۣ���Y1�飻����ϡ��Һ���ɷ���֬���嶳�ɷ۰�5��3������Ƚ���������ϣ���Y2�飻���ö���-���ɷ�[28]������Ȯ������ϡ��Һ��֬��������Ϊ��Ȯ������֬���嶳�ɷۣ���Y3�顣��Y1��Y3����Ʒ���ںֱ���0��3��7��14��21 d��С��ǻ��ҩ��0.5 mL/ֻ��ͬʱ��PBS�飨Y4�飩���հ����飨Y5�飩��ÿ���17ֻС��
����1.5�� Ƣ�ܰ�ϸ����ֳ�����ļ��
��������MTT��[24,32]���ڳ������ߺ�3��7��14��21��28 d����С����ժȡƢ�࣬��ĥ���ֱ���������ˮ����ϸ���ѽ�Һ��RPMI1640����Һ������ÿ�μ��봦��Һ����贵����ȣ�338×g����5 min���ú�10%���Ѫ�����ȫ����Һ����Ƣ�ܰ�ϸ������ϸ����Ũ��Ϊ1.5×106��/mL������96�װ壬100μL/�ף�����10μg/mL��ConA��Һ��ͬʱ��հ��տף�����RPMI1640����Һ����100μL/�ף�����3�����ף���37�棬5%CO2ϸ��������������48 h������5 mg/mL��MTT,20μL/�ף���������4 h����ֹ��Ӧ������100μL����Һ�ܽ���ɫ�ᾧ��37������12 h����ø���Ǽ��A570��A630ֵ������ʽ����̼�ָ����stimulatingindex,SI���������ж�С���ܰ�ϸ������ֳˮƽ��
����SI=(A570-A630)Con A��/��A570-A630���հ��տ�
����1.6 ��T�ܰ�ϸ�������ǵļ��
����������ʽϸ����[24]��ȡ1.5�����Ʊ��ij������ߺ�7��14��21��28 dƢ�ܰ�ϸ������PBS����������ϸ����Ϊ3×106��/mL��ȡ1 mL����EP���У��ֱ����1μL��Anti-mouse CD4 PE(L3T4,0.2 mg/mL����1μL��Anti-mouse CD8a FITC(Ly-2,0.5 mg/mL�������ȣ�������ֽ�ܹ���30 min��ͨ��Cytomics FC 500MPL��ʽϸ���Ǽ�⡣
����1.7�� С���Ȯ����������IgG(RV-IgG��ˮƽ�ļ��
��������ELISA�����ڳ������ߺ�7��14��21��28 d��ժȡС������ȡѪ������Ѫ�壬����С��RV-IgG ELISA�Լ��н��м�⣬ͨ��ø���Ǽ��A450ֵ��������ʽ����С��Ѫ����RV-IgGˮƽ��
����RV-IgGˮƽ��IU/mL)=0.029 7×A450ֵ��R2=0.997 2��×ϡ�ͱ���
����1.8 ��ͳ��ѧ����
����Ӧ��SPSS 17.0��������ͳ��ѧ������ʵ�����ݲ��þ�ֵ±������ʽ��ʾ�����Ƚϲ��õ����ط����������P<0.05Ϊ������ͳ��ѧ���塣
����2�� ���
����2.1�� Ƣ�ܰ�ϸ������ֳ����
�����������ߺ�3 d,Y3��С���SI���Ը���Y1��Y2��Y4��Y5�飨F=31.324,P<0.01�����������ߺ�7 d,Y3��SIֵ���Ը���Y2��Y4��Y5�飨F=230.158,P<0.01������Y1�Ƚϲ�����ͳ��ѧ���壨F=1.670,P>0.05�����������ߺ�14 d,Y3����Y1��Y2��Ƚϣ�������ͳ��ѧ���壨F=1.807,P>0.05���������нϸߵ�SIֵ��������֬������Ϊ���弰����������������ǿ��Ƣϸ����ֳ���������ߺ�21 d,Y3����Y5��������ͳ��ѧ���壨F=6.720,P<0.05���������������Ƚϣ��������ͳ��ѧ���壨F=1.37,P>0.05��������21 dʱ�����Ƣ�ܰ�ϸ����ֳ�Ĵ̼����ü����������������������ߺ�7��14 dʱ��Y1��Y3��SIֵ���ϸߣ�������ͣ�21 d�������ƽ�ȡ�����1��
����2.2 ��T�ܰ�ϸ���ı�����
�����������ߺ�7��14��21��28 d,Y3��С��T�ܰ�ϸ��CD4+/CD8+ֵ�����Ը���Y1��Y2��Y4��Y5�飨F�ֱ�Ϊ8.568��6.690��30.236��24.842,P<0.05��������Y3��ϸ������ˮƽ���Ը���Y1�顣Y2��С��T�ܰ�ϸ��CD4+/CD8+ֵ��Y1��Ƚϣ�������ͳ��ѧ���壨F�ֱ�Ϊ0.016��6.400��20.441��0.091��P>0.05���������Ʊ���֬������Ϊ������Կ�Ȯ��������а��ط�����ǿС���ϸ������ˮƽ������2��
����2.3 ��С��Ѫ����RV-IgG��ˮƽ
�����������ߺ�3 d������С��Ѫ���о�δ��RV-IgG��������ʱδ����RV-IgG���塣���������ߺ�21 dʱ��Y4��С��Ѫ�屻��Ⱦδ����⣬�������ߺ�7��14��21��28 d,Y3��RV-IgG�����Ը���Y4��Y5�飨F�ֱ�Ϊ4 061.638��5 268.680��9 486.353��787.351,P<0.01�������ߺ�7��14��21 d,Y3��RV-IgGˮƽ���Ը���Y1��Y2�飨F�ֱ�Ϊ52.959��148.611��21.079,P<0.05�������ߺ�28 d,Y3��RV-IgGˮƽ���Ը���Y1�飨F=13.850,P<0.05��������Y2��Ƚϣ�������ͳ��ѧ���壨F=0.013,P>0.05��������3������Y3����7��28 d��ά�ֽϺõ�����ԭ�ԣ��ڳ������ߺ�14 dС��Ѫ����RV-IgG����ˮƽѸ�����ߣ���Y1��Y2��RV-IgG��������ø��磬ˮƽ���ߡ�
������1 ���ߺ����С��Ƣϸ����SIֵ
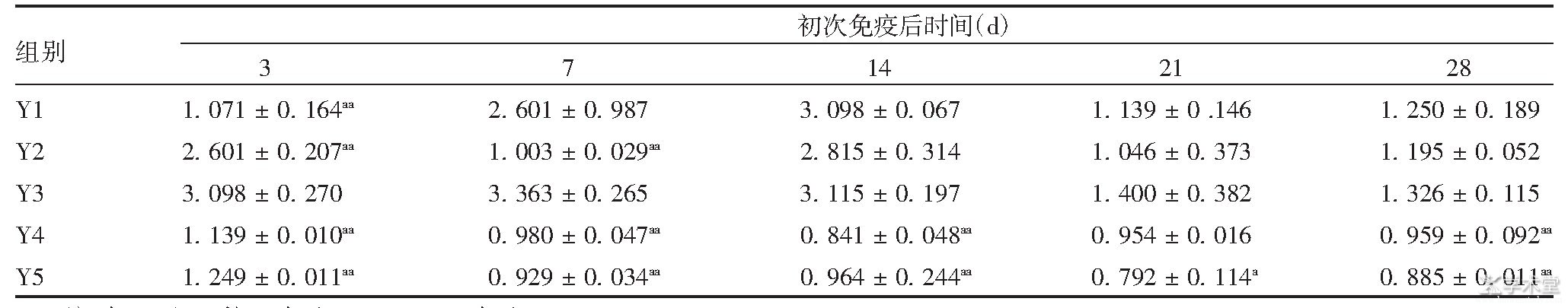
����ע����Y3��Ƚϣ�a��ʾP<0.05;aa��ʾP<0.01��
������2 ���ߺ����С��Ƣϸ����CD4+/CD8+ֵ
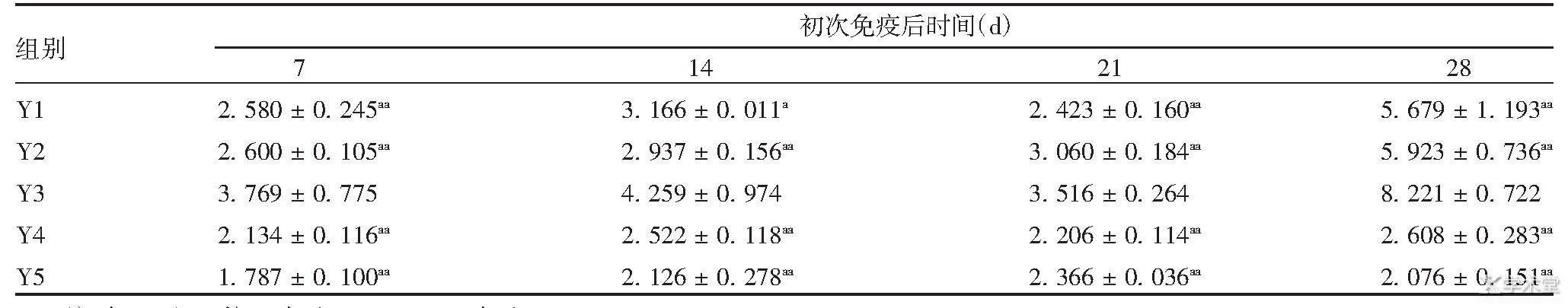
����ע����Y3��Ƚϣ�a��ʾP<0.05;aa��ʾP<0.01��
������3 ���ߺ����С��Ѫ����RV-IgGŨ��
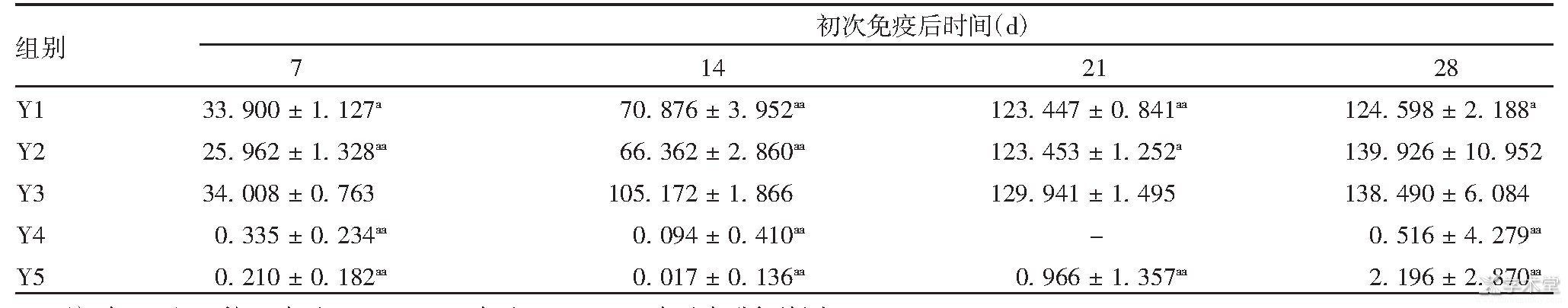
����ע����Y3��Ƚϣ�a��ʾP<0.05,aa��ʾP<0.01��-��ʾδ���м�⡣
����3�� ����
����MTT���������ʾ���������ߺ�3��28 d,Y3��С��Ƣ�ܰ�ϸ����ֳ��ƽ��ˮƽ������Y1��Y2�飨P<0.05);ELISA���ⶨ����������������ߺ�7��21 d,Y3��С�������RV-IgG���Ը���Y1��Y2�飨P<0.05�����������ߺ�28 d,Y3��С�������RV-IgG���Ը���Y1�飨P<0.05������Y2��Y3��С�����RV-IgG��ˮƽһ�¡���ʽϸ�������T�ܰ�ϸ���������������������������ߺ�7��28 d,Y3���CD4+/CD8+ֵ���Ը���Y1��Y2�飨P<0.01��������֬������Ϊ��Ȯ�����������������ܶԻ��������ǿ�ı�������ELISA���ⶨRV-IgG����ʽϸ���Ǽ��T�ܰ�ϸ�������������У��������ߺ�21��28 d,Y3���Y1����ܸ������յ��������ϸ��������Һ���ߣ�P<0.05��������֬������Ϊ�������弰�������ӳ����������ʱ�䡣
������MTT�������У��������ߺ�3 dƽ��SIֵ�ϵͣ����������ڻ���սӴ���ԭ���Դ��ڷ�����������ʶ��ĽΣ��������ߺ�7 dʱSIֵ���ϸߣ����������ھ���ϸ�����ɹ��ܣ�Y3�����Ը���Y1�飨P<0.05��������������֬���������������Ȼ������������״��Ƥϵͳ��reticuloendothelial system,RES���ḻ��Ƣ�࣬T�ܰ�ϸ���ܵ��̼���Ѹ����ֳ���ֻ�����Y2��ϵͿ�������֬�����������ֳ���һ�־�����ϵ�����־���ϸ�������˲�����ԭ�Ŀհ�֬���壬�����������T�ܰ�ϸ������ֳ�ֻ�������SI�ϵͣ��������ߺ�21 d��ƽ��SIֵ�ϵͣ�������21 d���Ѳ����շ�ǿ�ҵ�Ƣ�ܰ�ϸ����ֳ��
����֬��������Ϊ��������ʱ����������ͬ���ڵ����ϡ��Һ���յ���ǿ�����߷�Ӧ���Ұ�ȫ�Ժá�������С��������Ȼ�����ԡ�����Ϊ�뿹ԭ�������շ��뿹ԭ����������Ӧ���ܽ��ͱ�������ԭ�Ķ��ԡ���߿�ԭ�ȶ��ԡ��ӳ����������ʱ����ŵ㣬�����ڲ��õĽ�����Ϊ��һ���㷺Ӧ�õ�����������
���������
����[1]SHEN J Q.Effect of LPSp toimprove the immune efficiency of rabies vaccine[D].Nanning:Guangxi Medical University,2007.(in Chinese)�����.LPSp��ǿ��Ȯ������ԭ����Ч����ʵ���о�[D].��������������ҽ�ƴ�ѧ,2007.
����[2]YUE Z,ZHAO Y X,WANG H.Properties and advance in research of aluminium adjuvant[J].Chin J Biologicals,2016(12):1349-1354.(in Chinese)��,������,����.�����������Լ����о���չ[J].�й�������Ʒѧ��־,2016(12):1349-1354.
����[3]CHEN T T,LU W G.Research progress of aluminum adjuvant[J].World Clin Med,2015(2):128-134.(in Chinese)������,½ΰ��.���������Լ����о���չ[J].�����ٴ�ҩ��,2015(2):128-134.
����[4]LIU Y B,MAO S B,ZHOU F,et al.Aluminium adjuvants and their application in influenza vaccines[J].Int J Biologicals,2016,39(4):187-190.(in Chinese)�����,ë����,�ܷ�,��.���������������������е�Ӧ��[J].����������Ʒѧ��־,2016,39(4):187-190.
����[5]ZHANG B J.Research progress on the properties and action mechanism of aluminum adjuvants[J].Int J Biologicals,2018,41(4):185-189.(in Chinese)�ű���.�����������ʼ����û����о���չ[J].����������Ʒѧ��־,2018,41(4):185-189.
����[6] �����.WHO������������������ĵڶ���ר�����ۻ�[J].����ҽѧԤ������ϡ�������������Ʒ�ֲ�,2003,26(2):76-80.
����[7]SJ�iLANDER A,DRANE D,MARASKOVSKY E,et al.Immune responses to ISCOM formulations in animal and primate models[J].Vaccine,2001,19(17):2661-2665.
����[8]HUO N B.Development of human immune adjuvant[J].JPharm Res,2010,29(2):103-106.(in Chinese)������.��������������ǰ��չ��[J].ҩѧ�о�,2010,29(2):103-106.
����[9]FREY S,POLAND G S,PODDA A.Comparison of the safety,tolerability,and immunogenicity of a MF59-adjuvanted influenza vaccine and a non-adjuvanted influenza vaccine in non-elderly adults[J].Vaccine,2003,21(27):4234-4237.
����[10]GRAZIA G,MEDINI D,BORGOGNI E,et al.Adjuvanted H5N1 vaccine induces early CD4+T cell response that predicts long-term persistence of protective antibody levels[J].Proc Natl Acad Sci USA,2009,106(10):3877-3882.
����[11]SIVAKUMAR S M,SAFHI M M,KANNADASAN M,et al.Vaccine adjuvants-Current status and prospects on controlled release adjuvancity[J].Saudi Pharm J,2011,19(4):197-206.
����[12]O'HAGAN DEREK T,DE GREGORIO E.The path to a successful vaccine adjuvant-′The long and winding′[J].Drug Discov Today,2009,14(11-12):541-551.
����[13]COFFMAN ROBERT L,SHER A,SEDER R A.Vaccine adjuvants:putting innate immunity to work[J].Immunity,2010,33(4):492-503.
����[14]MBOW M L,DE GREGORIO E,VALIANTE N M,et al.New adjuvants for human vaccines[J].Curr Opin Immunol,2010,22(3):411-416.
����[15]LIU Y B,CHEN Z.Application of new generation adjuvants MF59 and AS03 in influenza vaccines[J].Int J Biologicals,2016,39(5):228-232,241.(in Chinese)�����,����.��������MF59��AS03�����������е�Ӧ��[J].����������Ʒѧ��־,2016,39(5):228-232,241.
����[16] ����.��ͬ����������BALB/cС������ϵͳ���õ��о�[D].�������й�ʳƷҩƷ�춨�о�Ժ,2013.
����[17]WEN X B,ZHANG L L,RAN X H.Update of mechanisms of action for aluminum-based adjuvants[J].Modern Animal Husbandry Veter,2016(11):47-52.(in Chinese)������,������,Ƚ��.�����������û����о���չ[J].�ִ�������ҽ,2016(11):47-52
����[18]HE P,HU Z Y.Advance in study on influencing factors of action mechanism and on improvement of aluminum-based adjuvant[J].Chin J Biologicals,29(6):654-659.(in Chinese)����,������.������ЧӦ��Ӱ�����ؼ�����������Ľ����о���չ[J].�й�������Ʒѧ��־,29(6):654-659.
����[19]FANG X,LIANG Z L.Progress in research on action mechanism of adjuvant in vaccines for human use[J].Chin J Biologicals,2015,28(8):866-870.(in Chinese)����.���������������û��Ƶ��о���չ[J].�й�������Ʒѧ��־,2015,28(8):866-870.
����[20]BRITO L A,MALYALA P,O′HAGAN D T.Vaccine adjuvant formulations:a pharmaceutical perspective[J].Seminars Immunol,2013,25(2):130-145.
����[21]WILSON-WELDER J H,TORRES M P,KIPPER M J,et al.Vaccine adjuvants:current challenges and future approaches[J].J Pharm Sci,2010,98(4):1278-1316.
����[22]LIU Y B,GENG X C,WANG J F,et al.Recent progress in researches for action mechanism of adjuvants[J].Chin J Drugs,2015,24(20):58-63.(in Chinese)����,���˳�,����,��.�����������û����о��½�չ[J].�й���ҩ��־,2015,24(20):58-63.
����[23]MUKHERJEE F,PRASAD A,BAHEKAR V S,et al.Evaluation of immunogenicity and protective efficacy of a liposome containing Brucella abortus S19 outer membrane protein in BALB/c mice[J].2016,17(1):1.
����[24] ������.��Ȯ������֬���嶳�ɷ۵��Ʊ���������ԭ���о�[D].��������������ҽ�ƴ�ѧ,2015.
����[25]CHEN J W.A study on immunogenicity of influenza vaccine lyophilized liposome prepared by different methods[J].Acta Univ Med Nanjing(Nat Sci),2013(7):1019-1023.(in Chinese)�½���.��������֬����ɷ��Ʊ�������������ԭ��Ӱ���о�[J].�Ͼ�ҽ�ƴ�ѧѧ��(��Ȼ��ѧ��),2013(7):1019-1023.
����[26]LIN Y J.The preparation of influenza vaccine liposome and thestudy of its properties[D].Kunming:Kunming Medical College,2009.(in Chinese)�����.��������֬������Ʊ��������о�[D].��������������ҽѧԺ,2009.
����[27]XU Y J,MA B,DAI Y B,et al.Study on mucosal immunity of influenza vaccine lyophilized liposome[J].Suzhou Univ JMed Sci,2012,32(4):499-503.(in Chinese)���¾�,����,���Ʋ�,��.��������֬����ɷ��Ĥ�����о�[J].���ݴ�ѧѧ��(ҽѧ��),2012,32(4):499-503.
����[28]XU W Y,QIAO J B,MA B,et al.Cellular immunity of influenza vaccine lyophilized liposome produced by freeze-thawing[J].J Chin Pharm Univ,2015,46(6):730-733.(in Chinese)������,�ǽ���,����,��.����-���ɷ��Ʊ�����������֬�����ϸ�������о�[J].�й�ҩ�ƴ�ѧѧ��,2015,46(6):730-733.
����[29]LU W D,LIN Y J,MA B,et al.Stability of influenza vaccine liposome powder[J].J Chin Pharm Univ,2010,41(4):360-362.(in Chinese)³����,�����,����,��.��������֬����ɷ۵��ȶ���[J].�й�ҩ�ƴ�ѧѧ��,2010,41(4):360-362.
����[30]YE H Y.The preparation and celluar immune study of rabies[D].Kunming:Kunming Medical University,2016.Ҷ����.����-���ɷ��Ʊ���Ȯ������֬���弰��ϸ�������о�[D].��������������ҽ�ƴ�ѧ,2016.
����[31]FAN Y C,FU W,PU M D,et al.Different diluted concentrations of liposomes immunogenicity of rabies vaccine[J].JKunming Med Univ,2019,40(5):14-17.(in Chinese)���,��Χ,���ε�,��.��ͬϡ��Ũ�ȶԿ�Ȯ������֬��������ԭ�Ե�Ӱ��[J].����ҽ�ƴ�ѧѧ��,2019,40(5):14-17.
����[32] �����.ϸ������ѧʵ���о�����[M].�����������ҽ������,2009.