����ժ Ҫ�������ɫ�������������Ժ�ں�������Ⱦ����Ҫ��ԭ��֮һ,�������ֲ���֯��ŧ�Ը�Ⱦ,��������ŧ��֢��ȫ���Ը�Ⱦ,Σ�����ཡ����������ҩ��-�ͼ������ֽ��ɫ�������(MRSA)��Ⱦ�ѳ�Ϊȫ�����������⡣������������(HDT)ͨ�������������߷�Ӧ���Ʋ�ԭ����Ⱦ����������,����Ч��������������ϸ����Ⱦ,�Ǹ�Ⱦ�Լ�����������ҩ����Ⱦ���Ƶ���˼·����Ȼ����Ӧ���ǵֿ�������ԭ�����ֵĵ�һ������,�������Ⱦ���Ͼ���,Ѹ��ļ���ͼ���������Ȼ����ϸ��,������Ȼ����Ӧ��,��������Ӧ������Ӧ��,���������ԭ����������Ҫ����������Ȼ���߷�Ӧ�������������Ͼ���Ⱦ������о���չ��
�����ؼ��ʣ������ɫ�������; �ͼ������ֽ��ɫ�������; ��Ȼ����ϸ��; ������������;
����Abstract����As one of main pathogens of nosocomial and community-acquired infections,staphylococcus aureus can cause pyogenic infection of local tissue,even systemic infection such as sepsis,which leads to serious threat to public health worldwide.Infection caused by methicillin-resistant Staphylococcus aureus(MRSA) has become a global challenge.Host-directed therapy(HDT) aims to control bacterial infection and offer protection by regulating immune response whereas bypassing problem of antibiotic resistance,which is an emerging and adjuvant strategy for treatment of infectious diseases,especially those caused by drug-resistant pathogens through regulating host immune response.Innate immune response constitutes first line of defense against invasive pathogens.Innate immune cells are rapidly recruited and activated to induce immune response when infected by S.aureus.This review mainly presents a comprehensive overview of innate immune response against S.aureus infection in recent years.
����Keyword����Staphylococcus aureus; Methicillin-resistant S. aureus(MRSA); Innate immune cells; Host-directed therapy;
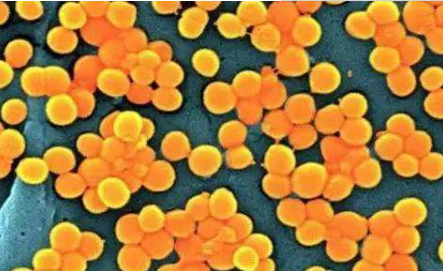
�������ɫ�������(staphylococcus aureus,S.aureus)���“���Ͼ�”,���ڸ���������(gram positive,G+)���,������Ժ�ں�������Ⱦ����Ļ�ŧ�Բ�ԭ��,�ľ�������ı�ǻ���ʺ����Ρ�Ƥ����������,����������״̬����ʱ������Ƥ��������֯��Ⱦ,��ë���ס�����֯�ס�Ƥ��ŧ������,��Ѫ��ɵ��¾�Ѫ֢�����ס���Ĥ�ס������ס�ŧ��Ѫ֢����֢��Ⱦ,������в������������[1,2,3]���ٴ����뵽��G+�²�����,���Ͼ��ļ����λ�ӵ�һ[4]��Ŀǰ��������Ȼ���ٴ�����Ⱦ���Ƶ���ѡҩ������꿹�������õ����˽��Ͼ�������ҩ�ԵIJ��Ͻ������ͼ������ֽ��ɫ�������(methicillin-resistant staphylococcus aureus,MRSA)�Զ����ٴ�һ�߿�������ҩ,�����ٴ��������뾽��[5]����2016�����翹������ҩ�������ͳ��,ȫ��ÿ��Լ70�������ڿ�������ҩ��ϸ����Ⱦ,MRSA������ҪΣ������֮һ��2017���й�CHINETϸ����ҩ��ⱨ������ʾ,MRSA���ٴ�ƽ�����������5���������30%,�ѳ�Ϊ����������ߵ��²���֮һ[4,6]��Ŀǰ,���ù�����ٴ�����MRSA��Ⱦ��һ�߿�����,���ս���������ù����ҩ��������ٴ���MRSA��Ⱦ���Ƶĸ�����[5,7,8,9]�����ܽ������MRSA�����Ϳ������з���ȡ��һ����չ,��Ϊ��ֹ���Ϳ�������ҩ���IJ���,Ѱ���µ����Ʋ��Ծ�����Ҫ���塣
����������Բ�ԭ�������ʶȵ�����Ӧ�����Ч�����ԭ�������������߷�Ӧ���������ڲ�ԭ�����,�������߷�Ӧ��ǿ,�������ϵͳ����֢��Ӧ�ۺ���(systemic inflammatory response syndrome,SIRS),���»�����֯���ˡ������ٹ���˥�ߡ�ŧ��֢,����������������������(host-directed therapy,HDT)�ǽ��꿹��Ⱦ������ֵ��·���,ͨ�����ظ�Ⱦ������������ǿ�����߷�Ӧ,���ٸ�Ⱦ�����Ĺ�����֢���ӷ���,������֯��������,������ҩ,�Ӷ��������塢����Ԥ��[10,11]��
�������Ͼ���Ⱦ������˫������õĶ�̬����,���������²���һ����ȡ���ڲ�ԭ������,��һ����ȡ�����������߷�Ӧ�����Ͼ����²���ǿ����Ҫȡ����������Ķ���(����Ѫ�ء����Ѷ��ء������ء��������ⶾ�ء�ɱ��ϸ���غ��ж����ݿ��ۺ������ص�)����Ϯ��ø(��:Ѫ������ø)��Ϊ��Ӧ�����仯,���Ͼ����ڰ��⸴�����γ�����Ĥ��������,������������߷��������,ʹĤ��ϸ���ӱܻ�������ϵͳ������,ͬʱ��ֹ���ӻ������������ڿ���Ⱦ������,��������Ȼ����ϵͳ�ǻ��巢�����߷���ЧӦ�ĵ�һ������,��������������ߡ�������ϸ������ͻ״ϸ��(dendritic cell,DC)������ϸ��(macrophage,Mφ)���ʴ�ϸ������Ȼɱ��ϸ��(natural killer cell,NK cell)��γδ Tϸ�������ܰ���ϸ��(innate lymphoid cell,ILC)���Dz����Ⱦ�Լ�������Ҫ��Ȼ����ϸ��������ԭ�����ֻ���ʱ,��������Ȼ����ϸ����Ѹ��ļ��������,��������Ӧ��Ӧ��һ������յ������������ϸ������,��������������α(tumor necrosis factor α,TNF-α)��IL-1��IL-6���Լ���������,�絥��ϸ����������1(monocyte chemotactic protein 1,MCP-1)�;���ϸ����֢����(macrophage inflammatory protein 2,MIP-2),�ٽ�������ϸ����Mφ���Ⱦ��λ�ۼ�,����ǿ�����ɹ���[12,13]����һ����,Mφ��������ϸ������DC�������ɡ�ɱ�ˡ��������ֲ�ԭ�������Ų�ԭ��������,�俹ԭ�Ŀɱ�רְ��ԭ���ϸ��(antigen presenting cell,APC),��DC��Mφ��ʸ�T�ܰ�ϸ��,��һ������������Ӧ�����߷�Ӧ[14]��
������Ȼ������������Ȼ����ϸ����η�����ԭ�����Ⱦ������ѧ����������ѧ�������Ҫ���⡣���������ص������ڽ��Ͼ���Ⱦ������������Ȼ����ϸ���ķ���ЧӦ,���ڲ������Ͼ��������֢��Ⱦ�ķ�������,Ѱ�Ҹ����Ⱦ�Լ����ķ��ΰбꡣ
����1 ���Ĥ��������
����Ƥ���Ĥ���Һ��������Ⱥ���γɵ����Ͻṹ�ڵֿ����������Ⱦ�з�����Ҫ����,������Ƥ���ϡ��������ϼ���ѧ���ϡ��Ĥ��Ƥ��֯�����˻����ڱ������������,������Ƥ����Һ�㡣��Ƥϸ�����н���,���ڵ��Һ�������Ĥ����,��ֹ���Ͼ�����;��������Ƥϸ��������ë,��ë�й��ɵİڶ���ʹ�Һ��һ����������,��ֹ���Ͼ�����,�ӿ����ų�[15]������Ĺ�����Ⱥ���Ĥ��������ƾ�Ⱥ,ͨ�������ռ估���ϲ����־�����,Ӫ����������������������������ԭ�������Ļ���,������������[16]��
����2 ��Ԥ�����Ȼ���߷���
����������Ȼ����Ӧ�����Һ������0��4 h��������,��һ�෴ӦѸ�ٵ�ЧӦ����,�翹���ġ��ܾ�ø�������ڵ��ס������ϸ�����ӵȡ��������Ǿ��п������ԵĶ���,��Դ�Կ����ľ��յ����ϳ�,���й���ɱ������,��Ũ�ȵķ���������֯ɱ���ز���ϸ����ʹ���γɿ�,ϸ����ϸ�������˶�����[17]���ܾ�ø���ͷ����������ȼ��Ե�����,�����ܾ�����,������ֱ�����˽��Ͼ�ϸ���ڵı��سɷ�-�ľ���(peptidoglycan,PGN)���½��Ͼ��ܽ�,���ɼ����ʹٽ���������[18]�������ڵ����ǻ�����Ӧ��(���Ⱦ)״̬�·����仯��һ��Ѫ�嵰��,����TNF-α��IL-1β��IL-6��ϸ�������յ�����ϸ������[19]������C��Ӧ������Ϊ�����ؽ�Ͻ��Ͼ����沢�����,�����ͽ���鵰�ȿ���ֹ���Ͼ�������ȡ������ϵͳ��ͨ����¶�ǽ��������;������·;������,�ڰ�ϸ�����������Ĥ�����岢�鵼ϸ���ܽ⡣���弤������в�����C3a��C4b��iC3b�ɹ̶���ϸ������,ͨ��������ϸ������CR1��CR3��CR4��϶��ٽ�����ϸ�����������á�
����3�� ��Ȼ����ʶ��
������Ȼ����ϸ���������ģʽʶ������(pattern recognition receptors,PRRs)��ֱ��ʶ��ԭ��������ı�Ҫ�ͱ��سɷ�-��ԭ��ط���ģʽ(pathogen-associated molecule patterns,PAMPs),����������,��ϸ�����ӡ��������ӡ�𤸽���ӡ��ڽ��Ͼ���Ⱦʱ,Toll������2/6�������(Toll-like receptor 2/6,TLR2/6)��NOD������2(nucleotide binding oligomerization domain-like receptors,NLR2) ����������ͨ����ϸ����Ӧ����,��PGN��ϸ��֬����֬�ױ���(lipoteichoic acid,LTA)�Ƚ�϶�������,������֢ϸ�����Ӳ������������ƽ��ʧ��[20]����PGN �̼���,TLR2 ͨ��ļ��ϸ���ڽ�ͷ���������ֻ�����88(myeloid differentiation factor 88,MyD88)���������ζ����ź�ͨ·,�Ӷ��յ����δ���ϸ������IL-6��TNF-α��IL-1β�ȴٽ���������MCP-1�Ϳ���ϸ������IL-10�Ȳ���[20,21]������TLR2/6 ʶ��,PGN Ҳ�ɱ�����ϸ���е��ܾ�ø����,�����õ���PGN ���سɷְ���������(muramyl dipeptide,MDP)�ܹ���ϸ�����źŵ���NOD2 ��cryopyrin��֢��ʶ����������߷�Ӧ��MDP��NOD2��Ϻ���յ�IL-6��TNF-α��MCP-1����,��cryopyrin��֢�巢���Ѿۻ���ٽ�IL-1β��IL-18����[22,23]��
����4�� ��Ȼ����ϸ��
������Ȼ����Ӧ�����ɶ�����Ȼ����ЧӦϸ������������յ���Ӧ�𡣲�����Ȼ����Ӧ���ϸ����4��96 h��������,�����ص�����������ϸ����DC��Mφϸ�����ʴ�ϸ����NKϸ����γδ Tϸ�������ܰ���ϸ���ڿ����Ͼ���Ⱦ�е����á�
����4.1 ��������ϸ��
����������ϸ��Լռ����Ѫ��ϸ��������50%��70%,�������ѪҺǨ�Ƶ���֢��λ������ϸ��[24]���о�����,������ϸ��ȱʧ��С�������Ⱦ���Ͼ�[25]��������ѿ�ײ���������ϸ�������쳣������Ŵ��Լ���,������ϸ������TLR5��TLR9��CD11b��CD18��CD35��������������(C-X-C motif chemokine receptor 1,CXCR1)����ˮƽ����[26]��TLR5�ı��オ�͵���������ϸ����ʶ��ϸ����ë;CD11b��CD18�ͱ��ﵼ��������ϸ�����ɽ��Ͼ��Ĺ�������;CXCR1���オ�͵���������ϸ�����������ڸ�Ⱦ��λ��
����������ϸ����Ҫͨ�����ɡ��ѿ������γ�������ϸ�������ղ���(neutrophil extracellular traps,NETs)3�ַ�ʽɱ�����ֲ�ԭ��[27,28,29]�����Ͼ���Ⱦʱ,������ϸ�������Fc����Ͳ������屻����,��ǿ����Ͳ���鵼����������,���ɵĽ��Ͼ���������ϸ���ڵĿ����ɷ��γ�����С�����Ŀ����[30]������С���ڵĶ��ֿ����ɽ��ⱻ���ɵ�����,�������ֻ���������,����O2-��H2O2��NO��,��Ϊ��������ֱ��ɱ��ϸ�������������ϸ�������ں����������ø�����Ե���ø����֯����ø���ܾ�ø�������ء���������ø����ԭ��ø������ø����ԭø���������ȶ��ֵ���,����ֱ��ɱ��������ϸ�����������Ĺ��ܡ���ϸ������,��������(S100A8/S100A9)ͨ������ŧ���ڵ�Ӫ������Mn2+��Zn2+������ϸ��������NETs���ڰ����γɵ�,��Ҫ��DNA���鵰�ס����������ø�����Ե���ø����֯����ø G�����ء�����ø�����,Ⱦɫ��DNA�ǹ��ɸ���ά��״�ṹ�ĹǼ�,����������Ƕ������,���ƻ���Ĥ��ϸ��Ĥ��NETs��������һ��˫�н�,����NETs�ɲ����ޡ�ɱ��ԭ��,����Ͼ�,�����ظ�Ⱦʱ,���ڽ��Ͼ���MRSA��Ⱦ���µ�ŧ��֢��,NETs��������,�Ի�������˺�[31,32,33]��NETs���鵰�����������ø�����ķ�ʽ����Ѫ����Ƥϸ������֯,�鵰����TLR2/4-MyD88ͨ·��������Ĵ�������,������Ѫ�ϰ�,�յ�Ѫ˨�γ�[34]��������������,������ϸ���ɷ�ΪN1�ͺ�N2�͡������о�����,N1��������ϸ��������NETs�γ�,N2��������ϸ�������ɲ�ԭ������ױ�����ϸ���������[35,36]�����,����NETs�γɡ��ٽ�������ϸ����N2����������N1 ���������ƽ��Ͼ���MRSA��Ⱦ���µ���֢��Ⱦ����Ч���ԡ�
����4.2 ��DC
����DC��Ŀǰ��֪�Ŀ�ԭ��ʹ�����ǿ��רְ�Կ�ԭ���ϸ��(APC),Ҳ�Ǽ����ʼTϸ�����շ���Ӧ������Ӧ���ʼ��ϸ��,������ʶ������Ӧ������ߵ����з�����Ҫ����[37,38]������APC��Mφϸ����Bϸ���Ƚ��ܴ̼��ѻ��Tϸ���������Tϸ����������֯��δ�����DC�߱���Fc���塢��¶�������TLR�Ȳ�ԭ������,�ͱ���MHC������ӡ����̼����Ӻ�𤸽����,��ȡ�����ɲ�ԭ���������ǿ����ԭ�������������δ�����DC���ɲ�ԭ������֯Ǩ�Ƶ������ܰ�����,���ֻ�Ϊ�����DC������Ӧ������Ӧ�𡣳����DC�߱���MHC��͢�����ӡ�𤸽�غ��̼�����(��CD86��CD80��CD40��),�ͱ���Fc�����ģʽʶ������,��˿�ԭ���������ǿ����ԭ��ȡ�����������ʸ�˹ϸ����λ�ڱ�Ƥ��θ������Ƥ��λ��δ����DC,�ڽ��Ͼ����µ�Ƥ����Ⱦ��,�ʸ�˹ϸ���ܹ����ɽ��Ͼ������ӿ�ԭ�ӹ�����ʵ�����[39]��
������Ϊ����������Ӧ���ʼ����,DC�ڸ�Ⱦ���ڿɷ��ڴ���ϸ������,��IL-6��TNF-α��IL-12�Ȳ���������ߵ���[38]��IL-12����Ȼ���߷�Ӧ������Ҫ��ϸ������֮һ,DCͨ������IL-12�ٽ� CD4+T ����ϸ������ֳ�ͷֻ�,�Ӷ��յ�Th1�����߷�Ӧ���о�����,CD11c-DTRת����С������DCȱʧ,����IL-12�������衣��Ұ����С�����,CD11c-DTRת����С����Ͼ���Ⱦ�������֢���˸�Ϊ���ء������ʸ���,ͨ����δ��������DC���䵽����BALB/cС������,С������β����Ͼ�������ǿ������ǻע����Դ��IL-12��,DCȱʧ��С���Ͼ���Ⱦ�����߹��ָܻ�[40]������DC����ͨ������IL-12������Ȼ���ߺ���Ӧ�����߷�Ӧ,�ֿ����Ͼ���Ⱦ��CD40L���ɻ��ѪС����ڵ���������,���дٽ�DC����MRSA�ͳ���ȹ���[41]��
����4.3 ��Mφϸ��
����Mφϸ����רְ��APC,����ǿ������ɹ���,�㷺�ֲ��ڸ���֯��,����̬��������������֯��λ�����������о�������֯����Mφϸ�������Դ����̥�е��ѻ���[42]������̬������,�����ڷ��ݡ��ԡ�����ͱ�Ƥ����֯��Mφϸ���ܹ����Ҹ��¶�����Ҫѭ���е���ϸ���IJ���;����֢������,ѪҺѭ���еĵ���ϸ������ļ������֯,���ֻ�Ϊ������֯�����Թ��ܵ�Mφϸ��,��Ϊ��ļ��Mφ����֢Mφϸ��[43]��Mφϸ���ܹ�ʶ�����ɲ�����������IJ�ԭ��,������ԭ��ʸ���Χ���ܰ����ٵ�Tϸ��,�շ���Ӧ������Ӧ��
����Mφϸ���ڽ��Ͼ���Ⱦ�з�����Ҫ�����߷������á���С�����в�����Ⱦ��ķ���ģ����,ͨ��GM-CSF�鵼�ķ���Mφϸ������ӿ�������ڻ���ֿ��̷��Ľ��Ͼ���Ⱦ,�������Ҫͨ�����ӷ���Mφϸ�������Ļ�����ʵ��[44]�����Ͼ�ϸ���ڵijɷ�PGN��LTA�̼�Mφϸ������IL-33[45]��IL-33ͨ���ٽ�������ϸ������ֳ��ļ�����ɲ�ɱ�˽��Ͼ�[46]������,IL-33ͨ����������ST2��ϴӶ�����Akt-cateninͨ·�ٽ�NO�ͷ�ɱ��[47]�����Ͼ�ϸ���ڳɷ�֬����Ҳ�ܹ�ͨ���������ϸ��TLR2��������NO����,����NO���ͷ��ܹ���Ч�ر����������ڽ��Ͼ���Ⱦ[48]��TNF-α��IL-6��ǰ��֢���ӵĵ��ʹ���,ǰ�ڵ���֢��Ӧ�����ڻ�����Ƹ�Ⱦ����ɢ����TLR2����ϵ�С��ԭ����ǻ����ϸ����,���Ͼ��յ�TNF-α��IL-6��IFN-γ��������[49]��
����Mφϸ������ǿ�Ŀ�����,�����ⲻͬ�������¿ɷֻ�ΪM1�ͺ�M2��[50]��M1���ֳƾ�����Mφϸ��,����TNF-α��IL-1��IL-12��NO�ȴ���֢ϸ������,���н�ǿ�Ŀ�ԭ��ʺ�ɱ������,����֢���ڷ�����Ҫ����,��������֢���ӵIJ���Ҳ������“ϸ�����ӷ籩”,����������֯;M2�ͱ���Ϊ������Mφϸ��,����IL-10��TGF-β��������ϸ������,������֯�����˿�����,����֢�ָ��η�����Ҫ����[51]�����,�ڽ��Ͼ���MRSA��Ⱦ���µ�ŧ��֢����,�ٽ�M1��M2ת��,��ŧ��֢С����б�������[52]��
����4.4 ���ʴ�ϸ��
�����ʴ�ϸ����Ƥ�����Ĥ����Ҫ�ڱ�ϸ��,��Ҫ����IgE�鵼�ij�����Ӧ,ͬʱҲ������������Ⱦ����Ӧ�𡣵����屻ϸ����Ⱦʱ,�ʴ�ϸ����ͨ����������ֱ��ɱ�����ֵIJ�ԭ��,����ͨ��ֱ��ʶ��ԭ���P����������������Ӧ���ʴ�ϸ�������ص����ܹ��ڰ����д������TNF-α,���TNF-α�Ŀ����ͷ��Ƿʴ�ϸ������ı�־�����Ͼ���Ⱦ�����,�ʴ�ϸ��ͨ���ѿ����ͷ�TNF-α,��ͨ���ϵ�Ѫ��ϸ����𤸽����1��Eѡ����ļ��������ϸ����DC,ǰ���ܹ�ֱ��ɱ�˽��Ͼ�,������������Ӧ������Ӧ���з�����Ҫ����[53,54]��
����4.5�� NKϸ��
����NKϸ��ͨ����Mφϸ����������ϸ��������ò�����忹���Ͼ���Ⱦ����Ȼ���ߡ��о�����,NKϸ�������Mφϸ���������������Mφϸ���Խ��Ͼ������ɼ����[55]�����Ͼ���Ⱦʱ,NKϸ�����ڵ�IL-22��IL-17��ϸ�����������ڻ�����Ƹ�Ⱦ��IL-22��IL-10�����Ա֮һ,��Ҫ��Tϸ������,Ҳ����NKϸ�������ܰ���ϸ��������IL-22���յ�Ƥ����֢��λ�����ܹ����ƽ��Ͼ������Ŀ���������S100A7��CAP18/LL37[56]��ͬʱ,IL-22����ͨ���STAT3�ź�ͨ·,�ٽ��������ƽ��Ͼ���ֳ���ܵĵ���SLURP1����[57]��IL-17��Ҫ��Tϸ������,Ҳ����NKϸ����γδ Tϸ�������ܰ���ϸ���ȷ���,�ڽ��Ͼ���ȾʱIL-17Ҳ��ļ��������ϸ��������֢��λ[58]��
����4.6 ��γδ Tϸ��
����γδ Tϸ����Ϊ������Ȼ���ߵ�Tϸ��Ⱥ��,ռ����Ѫ����Tϸ����5%��10%,��Ҫ�ֲ����Ĥ��Ƥ����֯,���������Ӻ����ߵ��ڵȹ���,����ϵ��Ȼ���ߺ���Ӧ�����ߵ�����������γδ Tϸ����ռ��Ȼ����ϸ���е�С����,�����ڿ����Ͼ���Ⱦ�����е����ò��ݺ��ӡ����µ��о���һ��֤ʵVγ6+Vδ4+Tϸ���ǽ��Ͼ���Ⱦ�����о������߱������õ���Ҫγδ Tϸ����Ⱥ[59]���ڽ��Ͼ�Ƥ����ȾС��ģ����,��Ⱦ��λ�д���γδ Tϸ���ۼ�[60,61]��γδ Tϸ��ͨ����������IL-17,�յ�������ϸ����ļ���ʹ���֢ϸ��������IL-1��TNF���ͷ�[58]����Ұ����С�����,γδ Tϸ��ȱʧ�Ľ��Ͼ���Ⱦ��С��������ϸ��ļ���ܵ�����,�ֲ���֯���˸�Ϊ����,ϸ������������[62]��
����4.7�� ILC
����ILC����Դ�ڹ�ͬ�ܰ���ϸ����������Ȼ����ϸ���������ܰ�ϸ����ILC�ɷ�Ϊ3������:ILC1��ILC2 ��ILC3��ILC1��ILC2��Ҫ�ֲ��ڸ���ͳ����Ȳ�λ,�ڿ����������ھ��ͼ������Ⱦ�����з�����Ҫ����[63]��ILC3��Ҫ�ֲ��ڱ����弰�������в�,�ڿ�ϸ����Ⱦ�з�����Ҫ����,�ɷ���IL-22��IL-17��ϸ������[64]����ʾILC3����ͨ��������������ϸ�����ӿ����Ͼ���Ⱦ���á�
����5 ���ܽ���չ��
�����������������ѧ���Ϻ���Ȼ����ϵͳ��ͬ��ɵֿ�������ԭ�����ֵĵ�һ�����ߡ���ԭ��������������ϸ��ˮƽ������������²�����Ҫ���ڡ��ڽ��Ͼ���Ⱦ������,��Ȼ����ϸ���ڲ�ԭ�������ɡ�ʶ�������������ؼ����á���Ȼ����ϸ��ͨ��PRRs�Խ��Ͼ���PAMPs����ʶ��,������������ź�ͨ·,��������ϸ������(��TNF-α��IL-6��IL-1β��IL-17��IL-22��IL-33��)����������(��MCP-1��MIP-2��),��ļ�����������������ЧӦϸ��,��������ϸ����Mφϸ����DC���յ���Ȼ����Ӧ��ͬʱ,�����˽��Ͼ���DCǨ�����ܰͽᲢ������Ӧ�����߷�Ӧ������,�ڿ���Ⱦ������,Mφϸ�����ӿ�ԭ������á������Բ�ԭ��ijɹ������ǿ��ٵ���Ȼ���߷�Ӧ����Ӧ�����߷�Ӧ�Ĺ�ͬ�����
���������ڵֿ���ԭ�����ֹ����в�����������֢ϸ������,�ʵ���ϸ�����Ӻϳɺͷ��ڶ������������߷�����˵�DZ�Ҫ��,���ǹ��ȵ���֢��Ӧ�ᵼ��SIRS,������������ٹ����ϰ�,���յ���������HDTּ�ڼ��ٸ�Ⱦ�����й��ȵ���֢��Ӧ,�ڲ��λƽ���������߷�Ӧ,�Ӷ��Ի����𱣻����á�������ҩ������Ч�ɷ��ڿ����Ͼ���Ⱦ����չ�ֳ���������,����ҩ��Ƶ���Ч�ɷ�-������Ƽ�(ephedrine hydrochloride,EH)�������õ����ߵ������á��ڽ��Ͼ���Ⱦ���µļ��Ը�Ĥ��С��ģ����,EHͨ���ٽ���������IL-10���ں����ƴ�������TNF-α�ı���,�����������ಡ������,���С������[21,65]��̨�庬Ц�ı��������������-��Ц����(micheliolide,MCL)���µ�MRSA��ȾС��Ѫ����IL-6��TNF-α��MCP-1��IFN-γ����֢���ӷ���,����Ρ�����֯��������,����С��������[66]�����,��HDT�Ƕȳ���,�������������߷�Ӧ,Ϊ�����Ͼ�����������ҩ����Ⱦ�ṩ��˼·��
���������
����[1] Knox J,Uhlemann AC,Lowy FD.Staphylococcus aureus infections:Transmission within households and the community[J].Trends Microbiol,2015,23(7):437-444.
����[2] Wertheim HF,Melles DC,Vos MC,et al.The role of nasal carriage in Staphylococcus aureus infections[J].Lancet Infect Dis,2005,5(12):751-762.
����[3] Dayan GH,Naglaa M,Scully IL,et al.Staphylococcus aureus:The current state of disease,pathophysiology and strategies for prevention[J].Exp Rev Vaccines,2016,15(11):1373-1392.
����[4] ����Ʒ,����,�����,��.2017��CHINET�й�ϸ����ҩ�Լ��[J].�й���Ⱦ�뻯����־,2018,18(3):241-251.Hu FP,Guo Y,Zhu DM,et al.Antimicrobial resistance profile of clinical isolates in hospitals across China:Report from the CHINET Surveillance Program,2017[J].Chin J Infect Chemother,2018,18(3):241-251.
����[5] Hassoun A,Linden PK,Friedman B.Incidence,prevalence,and management of MRSA bacteremia across patient populations-A review of recent developments in MRSA management and treatment[J].Crit Care,2017,21(1):211.
����[6] Nelson RE,Slayton RB,Stevens VW,et al.Attributable mortality of healthcare-associated infections due to multidrug-resistant Gram-negative bacteria and methicillin-resistant Staphylococcus aureus[J].Infect Contr Hosp Epidemiol,2017,38(7):848-856.
����[7] ����,������,��ΰ��,��.�ͼ������ֽ��ɫ����������о���չ[J].�л�ҽԺ��Ⱦѧ��־,2014,24(14):3638-3640.Xing Q,Jiang RL,Ma WB,et al.Research progress of methicillin-resistant Staphylococcus aureus[J].Chin J Nosocomiol,2014,24(14):3638-3640.
����[8] Baek JY,Chung DR,Ko KS,et al.Genetic alterations responsible for reduced susceptibility to vancomycin in community-associated MRSA strains of ST72[J].J Antimicrob Chemother,2017,72(9):2454-2460.
����[9] Werth BJ,Jain R,Hahn A,et al.Emergence of dalbavancin non-susceptible,vancomycin-intermediate Staphylococcus aureus (VISA) after treatment of MRSA central line-associated bloodstream infection with a dalbavancin-and vancomycin-containing regimen[J].Clin Microbiol Infect,2018,24(4):429.
����[10] Zumla A,Rao M,Wallis RS,et al.Host-directed therapies for infectious diseases:Current status,recent progress,and future prospects[J].Lancet Infect Dis,2016,16(4):47-63.
����[11] Kaufmann SHE,Dorhoi A,Hotchkiss RS,et al.Host-directed therapies for bacterial and viral infections[J].Nat Rev Drug Dis,2018,17(1):35-56.
����[12] Doster RS,Kirk LA,Tetz LM,et al.Staphylococcus aureus infection of human gestational membranes induces bacterial biofilm formation and host production of cytokines[J].J Infect Dis,2017,215(4):653-657.
����[13] Pang X,Liu X,Cheng Y,et al.Sono-immunotherapeutic nanocapturer to combat multidrug-resistant bacterial infections[J].Adv Mater,2019,31(35):e1902530.
����[14] Iwasaki A,Medzhitov R.Control of adaptive immunity by the innate immune system[J].Nat Immunol,2015,16(4):343-353.
����[15] ��ѩ��,��ά.ҽѧ����ѧ(��3��)[M].����:��������������,2015:150-175.Cao XT,He W.Medical Immunology(3 ed)[M].Beijing:People′s Med Publishing House,2015:150-175.
����[16] Grice EA,Segre JA.The skin microbiome[J].Nat Rev Microbiol,2011,9(4):244-253.
����[17] Sierra JM,Fusté E,Rabanal F,et al.An overview of antimicrobial peptides and the latest advances in their development[J].Exp Opin Biol Ther,2017,17(6):663-676.
����[18] Ragland SA,Criss AK.From bacterial killing to immune modulation:Recent insights into the functions of lysozyme[J].PLoS Pathog,2017,13(9):e1006512.
����[19] Gabay C,Kushner I.Acute-phase proteins and other systemic responses to inflammation[J].N Engl J Med,1999,340(6):448-454.
����[20] Takeuchi O,Akira S.Pattern recognition receptors and inflamm-ation[J].Cell,2010,140(6):805-820.
����[21] Zheng Y,Yang Y,Li L,et al.Ephedrine hydrochloride inhibits PGN-induced inflammatory responses by promoting IL-10 production and decreasing proinflammatory cytokine secretion via the PI3K/Akt/GSK3β pathway[J].Cell Mol Immunol,2013,10(4):330-337.
����[22] McDonald C,Inohara N,Nu��ez G.Peptidoglycan signaling in innate immunity and inflammatory disease[J].J Biol Chem,2005,280(21):20177-20180.
����[23] Davis KM,Nakamura S,Weiser JN.Nod2 sensing of lysozyme-digested peptidoglycan promotes macrophage recruitment and clearance of S.pneumoniae colonization in mice[J].J Clin Invest,2011,121(9):3666-3676.
����[24] Rigby KM,Deleo FR.Neutrophils in innate host defense against Staphylococcus aureus infections[J].Semin Immunopathol,2012,34(2):237-259.
����[25] Robertson CM,Perrone EE,Mcconnell KW,et al.Neutrophil depletion causes a fatal defect in murine pulmonary Staphylococcus aureus clearance[J].J Surg Res,2008,150(2):275-285.
����[26] Hartl D,Lehmann N,Hoffmann F,et al.Dysregulation of innate immune receptors on neutrophils in chronic granulomatous disease[J].J Allergy Clin Immunol,2008,121(2):375-382.
����[27] Lewis ML,Surewaard BGJ.Neutrophil evasion strategies by Streptococcus pneumoniae and Staphylococcus aureus[J].Cell Tissue Res,2018,371(3):489-503.
����[28] Guerra FE,Borgogna TR,Patel DM,et al.Epic immune battles of history:Neutrophils vs Staphylococcus aureus[J].Front Cell Infect Microbiol,2017,7:286.
����[29] Spaan AN,Surewaard BG,Nijland R,et al.Neutrophils versus Staphylococcus aureus:A biological tug of war[J].Annu Rev Microbiol,2013,67(1):629-650
����[30] Segal AW.How neutrophils kill microbes[J].Annu Rev Immunol,2005,23:197-223.
����[31] ��ά��,������,�����,��.������ϸ�������ղ���(NETs)������������Լ������о���չ[J].�й�����ѧ��־,2019,35(5):635-638.Cao WJ,Shao ZW,Duan MT,et al.Research progress of neutrophil extracellular trap (NETs) in related inflammatory diseases[J].Chin J Immunol,2019,35(5):635-638.
����[32] Hsu CC,Hsu RB,Ohniwa RL,et al.Neutrophil extracellular traps enhance Staphylococcus aureus vegetation formation through interaction with platelets in infective endocarditis[J].Thromb Haemost,2019,119(5):786-796.
����[33] Bj?rnsdottir H,Dahlstrand RA,Klose FP,et al.Phenol-soluble modulin α peptide toxins from aggressive Staphylococcus aureus induce rapid formation of neutrophil extracellular traps through a reactive oxygen species-independent pathway[J].Front Immunol,2017,8:257.
����[34] Shen XF,Cao K,Jiang JP,et al.Neutrophil dysregulation during sepsis:An overview and update[J].J Cell Mol Med,2017,21(9):1687-1697.
����[35] Andzinski L,Kasnitz N,Stahnke S,et al.Type �� IFNs induce anti-tumor polarization of tumor associated neutrophils in mice and human[J].Int J Cancer,2016,138(8):1982-1993.
����[36] Cai W,Liu S,Hu M,et al.Functional dynamics of neutrophils after ischemic stroke[J].Transl Stroke Res,2020,11(1):108-121.
����[37] Durai V,Murphy KM.Functions of murine dendritic cells[J].Immunity,2016,45(4):719-736.
����[38] Banchereau J,Briere F,Caux C,et al.Immunobiology of dendritic cells[J].Annu Rev Immunol,2000,18:767-811.
����[39] Qi R,Liu M,Gao XH,et al.Histone deacetylase activity is required for skin langerhans cell maturation and phagocytosis[J].J Dermatol Sci,2012,65(2):152-155.
����[40] Schindler D,Gutierrez MG,Beineke A,et al.Dendritic cells are central coordinators of the host immune response to Staphylococcus aureus bloodstream infection[J].Am J Pathol,2012,181(4):1327-1337.
����[41] Nishat S,Wuescher LM,Worth RG.Platelets enhance dendritic cell responses against Staphylococcus aureus through CD40-CD40L[J].Infect Immun,2018,86(9):e00186-18.
����[42] McGrath KE,Frame JM,Fegan KH,et al.Tissue-resident macrophages originate from yolk-sac-derived erythro-myeloid progenitors[J].Nature,2015,518(7540):547-551.
����[43] Ginhoux F,Guilliams M.Tissue-resident macrophage ontogeny and homeostasis[J].Immunity,2016,44(3):439-449.
����[44] Subramaniam R,Barnes PF,Fletcher K,et al.Protecting against post-influenza bacterial pneumonia by increasing phagocyte recruitment and ROS production[J].J Infect Dis,2014,209(11):1827-1836.
����[45] Wu G,Zhu B,Hong X,et al.Role of cytokines in host defense against Staphylococcus aureus skin infection[J].Histol Histopathol,2017,32(8):761-766.
����[46] Burg ND,Pillinger MH.The neutrophil:Function and regulation in innate and humoral immunity[J].Clin Immunol,2001,99(1):7-17.
����[47] Li C,Li H,Jiang Z,et al.Interleukin-33 increases antibacterial defense by activation of inducible nitric oxide synthase in skin[J].PLoS Pathog,2014,10(2):e1003918.
����[48] Kim NJ,Ahn KB,Jeon JH,et al.Lipoprotein in the cell wall of Staphylococcus aureus is a major inducer of nitric oxide production in murine macrophages[J].Mol Immunol,2015,65(1):17-24.
����[49] Nandi A,Dey S,Biswas J,et al.Differential induction of inflammatory cytokines and reactive oxygen species in murine peritoneal macrophages and resident fresh bone marrow cells by acute Staphylococcus aureus infection:Contribution of Toll-like receptor 2 (TLR2)[J].Inflammation,2015,38(1):224-244.
����[50] Mantovani A,Sica A,Sozzani S,et al.The chemokine system in perse forms of macrophage activation and polarization[J].Trends Immunol,2004,25(12):677-686.
����[51] Murray PJ.Macrophage polarization[J].Annu Rev Physiol,2017,79:541-566.
����[52] Arora H,Wilcox SM,Johnson LA,et al.The ATP-binding cassette gene ABCF1 functions as an E2 ubiquitin-conjugating enzyme controlling macrophage polarization to dampen lethal septic shock[J].Immunity,2019,50(2):418-431.
����[53] Abel J,Goldmann O,Ziegler C,et al.Staphylococcus aureus evades the extracellular antimicrobial activity of mast cells by promoting its own uptake[J].J Innate Immun,2011,3(5):495-507.
����[54] Rochadesouza CM,Berentmaoz B,Mankuta D,et al.Human mast cell activation by Staphylococcus aureus:Interleukin-8 and tumor necrosis factor alpha release and the role of Toll-like receptor 2 and CD48 molecules[J].Infect Immun,2008,76(10):4489-4497.
����[55] Zhao H,Li W,Gao Y,et al.Exposure to particular matter increases susceptibility to respiratory Staphylococcus aureus infection in rats via reducing pulmonary natural killer cells[J].Toxicology,2014,325:180-188.
����[56] Wolk K,Kunz S,Witte E,et al.IL-22 Increases the innate immunity of tissues[J].Immunity,2004,21(2):241-254.
����[57] Yasuhiro M,Kiyoko T,Toshinori N,et al.IL-22/STAT3-induced increases in SLURP1 expression within psoriatic lesions exerts antimicrobial effects against Staphylococcus aureus[J].PLoS One,2015,10(10):e0140750.
����[58] Cho JS,Pietras EM,Garcia NC,et al.IL-17 is essential for host defense against cutaneous Staphylococcus aureus infection in mice[J].J Clin Invest,2010,120(5):1762-1773.
����[59] Marchitto MC,Dillen CA,Liu H,et al.Clonal Vγ6+Vδ4+T cells promote IL-17-mediated immunity against Staphylococcus aureus skin infection[J].Proc Natl Acad Sci USA,2019,116(22):10917-10926.
����[60] Murphy AG,O′Keeffe KM,Lalor SJ,et al.Staphylococcus aureus infection of mice expands a population of memory γδ T cells that are protective against subsequent infection[J].J Immunol,2014,192(8):3697-3708.
����[61] Dillen CA,Pinsker BL,Marusina AI,et al.Clonally expanded γδ T cells protect against Staphylococcus aureus skin reinfection[J].J Clin Invest,2018,128(3):1026-1042.
����[62] Malhotra N,Yoon J,Leyva-Castillo JM,et al.IL-22 derived from γδ T cells restricts Staphylococcus aureus infection of mechanically injured skin[J].J Allergy Clin Immunol,2016,138(4):1098-1107.
����[63] Seillet C,Jacquelot N.Sensing of physiological regulators by innate lymphoid cells[J].Cell Mol Immunol,2019,16(5):442-451.
����[64] Eken A,Yetkin MF,Vural A,et al.Fingolimod alters tissue distribution and cytokine production of human and murine innate lymphoid cells[J].Front Immunol,2019,10:217.
����[65] He W,Ma J,Chen Y,et al.Ephedrine hydrochloride protects mice from staphylococcus aureus-induced peritonitis[J].Am J Transl Res,2018,10(3):670-683.
����[66] Jiang X,Wang Y,Qin Y,et al.Micheliolide provides protection of mice against Staphylococcus aureus and MRSA infection by down-regulating inflammatory response[J].Sci Rep,2017,7:41964
�ɾ����Ŀ�ɸѡ�������෨��Һ�෨��ǰ���б군��ֱ�Ӱ���������Ŀ�ɸѡ�������������ڵ���A/G��ɽ�ϰб����IgG,������Ƚ�IgG���Ŀ���Һ���з�������ͨ���뵰��A/G��Ϻ���ϴ��ȥ��δ����ɾ����¡��...