
硫是植物生态系统中的必要元素,它对农作物的生长发育及品质优劣起着重要作用[1].目前硫已经成为世界公认的继氧、磷和钾后的第 4 位植物生长必要元素[2-3].但过量的硫也会造成环境污染,所以硫的分析成为重要的常规分析和监控项目之一[3].
土壤中硫的测定一般包含两步: ①土样的前处理; ②处理后样液中硫的测定.常规前处理方法是用硝酸和高氯酸或者硝酸/高氯酸氢氟酸浸提法.但这种浸提的方法有很大的缺点,一是提取不完全,土壤中难溶态、包蔽态硫不易被浸提出来; 二是浸提液要进行过滤容易造成硫的损失; 三是浸提液基质复杂,对测定方法的要求苛刻.另一种应用较广的前处理方法是将土壤、碳酸钠和硝酸钠的混合物在400 ℃ 下 加 热 30 min,然 后 在 950 ℃ 融 熔10 ~ 20 min[4],混熔体溶于盐酸并用亚甲基蓝法测定[5].这种方法步骤繁琐,耗时费力,形成的待测液成分复杂,且带来很高的盐分含量,常规溶液中硫的测定方法不适用,需开发专用分析方法,特别是对土壤中较低含量的硫的分析存在困难.
本研究提出使用热分解前处理,使土壤中的硫热分解富集到溶液中,实现了快速获得待测液及待测液的简单化.同时对此待测液,使用常规的可见光分光光度法进行检测.实现了利用常规溶液中硫的分析方法对土壤中总硫进行简单、快速和准确的分析.
1 实验部分
1. 1 试剂与仪器
铬酸钡、含钙氨水、硫酸钾、95%乙醇、NaOH、过氧化氢、三氧化钨、氯化钠均为分析纯.
热分解设备见图 1,包括空气泵、气体流量计、热分解石英管( Φ30 mm ×550 mm) 、SRJK-2-13 管式炉、热分解瓷舟( 15 mm × 70 mm × 13 mm) ; 722 可见光分光光度计.
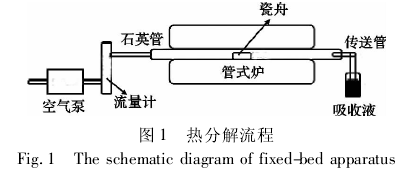
1. 2 实验方法
称取 1. 0 g 土壤样品置于瓷舟中,待管式炉炉温稳定在 1 000 ℃时,将瓷舟推至热分解管的中央位置,封闭入口.吸收端接入 20 mL 的 0. 05 mol/L的氢氧化钠吸收液.控制载气流量为0. 1 L/min,开始分解计时 35 min.分解完成后,将吸收液定容到50 mL,利用铬酸钡分光光度法在波长 420 nm 处进行测定[6].
2 结果与讨论.
2. 1 热分解前处理系统条件的优化
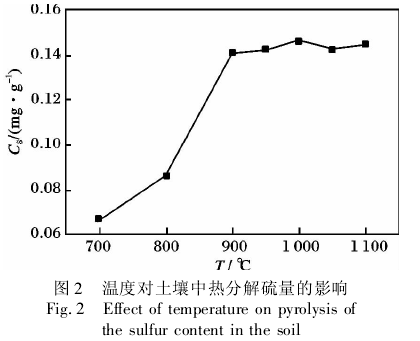
2. 1. 1 分解温度的选择 由图 2 可知,土壤中的硫分解量随温度升高逐渐增大,1 000 ℃ 时已经达到其最大分解.进一步提高分解温度分解量反而下降,类似的结果在文献[7]中也报道过,其原因是温度过高使样品熔融,不利于硫的氧化物从熔体中挥发,导致分解的硫含量偏低.此外,温度太高,会减少石英管的使用寿命,增加分析成本.综合考虑,管式炉温度优化条件为 1 000 ℃.
2. 1. 2 热分解时间和载气流量对硫的热分解的影响 由图 3a 可知,开始 30 min 内,硫分解量逐步增大; > 30 min,硫分解量没有明显的变化,表明土壤中的硫已分解完全,为了使硫分解得更充分,将热分解时间设定为 35 min.
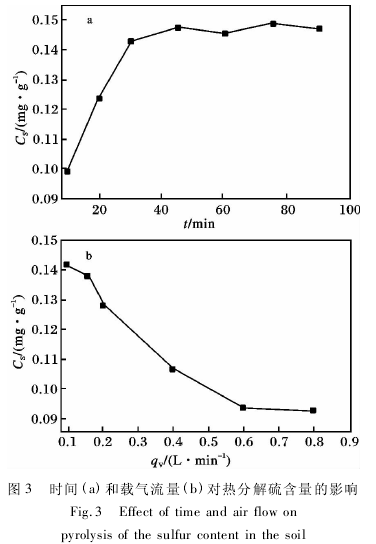
由图 3b 可知,硫含量随着载气流量的增大而减少,其原因是随着载气流量( qv) 的增大,吸收液溢出大量气泡,使得分解的硫的氧化物来不及被吸收液吸收,随着气泡逸散到空气中.因此,控制载气流量为 0. 1 L/min.
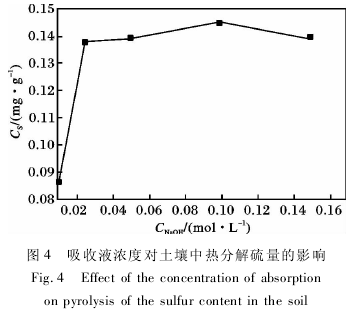
2. 2 吸收液浓度和体积的优化由图 4 可知,NaOH 的浓度≤0. 01 mol/L 时,无法完全吸收热分解出来的硫的氧化物,吸收液浓度从0. 02 mol/L 增至0. 15 mol/L 时,硫的测定量基本不变,所以在吸收液浓度设定为 0. 05 mol/L 就可以满足要求.
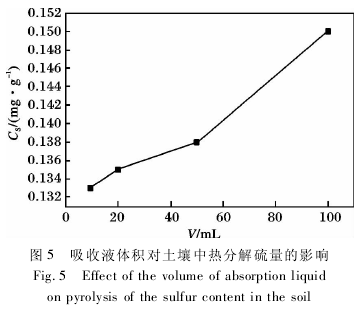
由图 5 可知,随着吸收液体积的增大,所测得的硫含量逐步增大.其原因是吸收液体积增大,吸收液高度增加,使得载气中的硫的氧化物能被充分吸收,减少了硫的损失.
2. 3 土壤粒径及添加剂优化
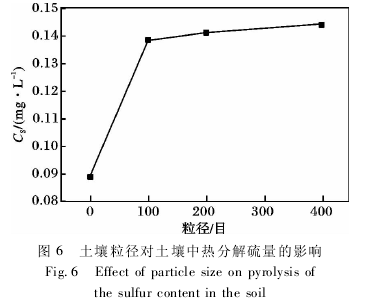
由图 6 可知,土壤粒径较大时,所测得的硫含量较低,粒径从 100 ~400 目时,所测得的硫含量缓慢增大.说明粒径的大小对硫的分解有一定的影响,原因可能是通过碾磨可以对包蔽态硫有一定的破环,使这部分难分解的硫释放出来,从而使硫的分解量增加.因此,在实验室条件允许的情况下,尽可能使用小粒径土样进行检测.
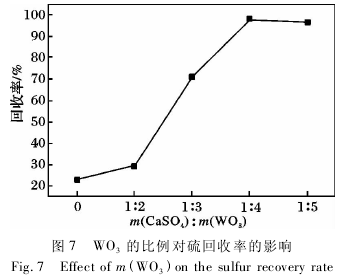
WO3作为热分解促进剂,在高温下对水泥中的氟、氯、溴及硫等元素的影响已有文献报道[8-9].由于土壤中的无机硫主要为硫酸盐,因此选择硫酸钙作为代表物来验证 WO3对土壤中的无机硫的分解促进作用.实验取 5 份 0. 05 g 硫酸钙,按照一定比例关系分别加入 WO3混匀,进行热分解测定,结果见图 7.
由图 7 可知,未加促进剂时,1 000 ℃时硫酸钙的回收率较低; 当加入促进剂 WO3,回收率逐步增大; 当硫酸钙与加入的三氧化钨含量比为 1∶ 4 时,回收率明显增大,达到 96%,说明热分解促进剂三氧化钨对硫酸钙的分解有明显的促进作用.
2. 4 方法检出限
利用铬酸钡分光光度法测定土壤中的硫,在选定的测定条件下,硫的含量在 0. 033 ~ 0. 165 mg/g范围内,具有良好线性关系,其检出限( 3σ,n = 10)为 0. 02 mg/g.受地域及环境影响,土壤中硫含量也存在差异.
为解决部分低硫土壤硫含量利用本方法难以检测的问题,本研究设计了累积吸收实验,即同一份吸收液对多次进样所分解的硫进行叠加吸收.以 0. 5 g 土样为标准,1 g 即为 2 次各 0. 5 g 进样量的累积量,逐次增加进样次数,2. 5 g 为 5 次各 0. 5 g 进样量的累积量.随进样次数的增加,所测硫含量也随着累积进样量呈线性增加,并且在累积进样量为 2. 5 g时,土壤中硫含量测定并没有出现明显的降低.表明利用累积吸收的方法,可以拓宽该方法的检测范围,提高检测的灵敏度,实现对部分低硫土壤进行检测.采用累积吸收实验,可以将本方法的最低检出范围 拓 宽 至 0. 006 mg/g,方 法 检 出 限 也 降 为0. 006 mg / g.
2. 5 前处理方法对比
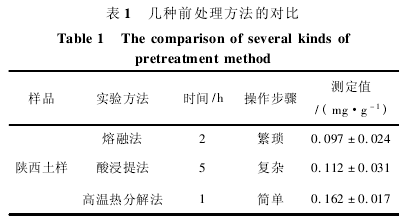
由表 1 可知,土样经过熔融和浸提的前处理方法进行分析,步骤繁琐,耗时费力,形成的待测液成分复杂,对测定结果有比较大的影响.热分解前处理过程,操作简单、快速,测定值准确.
2. 6 实际样品的分析
1 号为陕西某地土样,2 号为辽宁某地土样,3号为陕西某地农业土样.均取自土壤层位 20 cm处,实验用量均为 1. 0 g,每个样品各重复测定 3 次,获得了总硫含量,同时加入硫标准溶液,进行加标回收实验,结果见表 2.
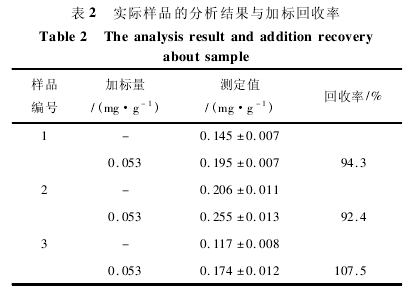
由表 2 可知,回收率为 92. 4% ~107. 5%,能满足分析要求.
2. 7 准确度实验
用本法对国家一级标准物质 GBW07425 土壤、GBW07454 土壤、GBW( E) 070041 土壤进行分析,结果见表 3.
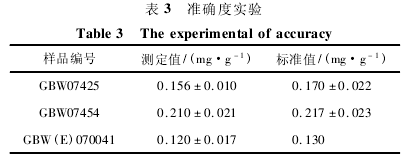
3 结论
利用热分解前处理结合分光光度计法快速测定土壤中的硫,与常用检测方法的前处理过程相比,本方法的前处理过程操作简单、快速,仅用时 35 min左右; 使用化学试剂较少,对环境友好; 所用分析测定仪器均为实验室常规仪器; 检出限相对较低,检测结果准确、可靠,可以用于土壤中硫的分析.
参考文献:
[1] 中国土壤学会. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社,2000: 223-224.
[2] 刘婷琳,马名扬,张浩原,等. 弱碱性土有效硫测定方法的改进[J]. 理化检验: 化学分册,2010( 7) : 841-842.
[3] 吴俊生. 硫将成为第四养分[N]. 农资导报,2013-5-10( A04) .
[4] Landerst D H,David M B,Mitchell M J. Analysis of or-ganic and inorganic sulfur constituents in sediments,soilsand water[J]. Water Air and Soil Pollution,1987,35:157-170.
[5] Johnson C M,Nishita H. Microestimation of sulfur in pla-ntmaterials,soils,and irrigation waters[J]. Anal Chem,1952( 24) : 736-742.
[6] 葛明,朱剑禾. 铬酸钡分光光度法分析土壤中水溶性硫酸盐[J]. 苏州大学学报,2002( 5) : 23-25.
[7] 程思海,陈道华,王飞. 元素分析仪法快速测定海洋地质样品中的硫[J]. 化学分析计量,2010( 3) : 32-34.
[8] Yasunari Noguchi,Zhang Liang,Toshihisa Maruta,et al.Simultaneous determination of fluorine,chlorine and bro-mine increment with ion chromatography after pyrolysis[J]. Analytica Chimica Acta,2009,640( 1) : 106-109.
[9] 钟吕玲,张良. 热分解法结合电导检测离子交换色谱快速测定水泥中的 SO3[J]. 水泥,2010( 4) : 57-59.