����ժҪ���������������ͨ����һ�������ǻ���������ˮ������Ԫ�Ϲ��ɣ�����Ϊ��ͳ�в�ҩ�Ļ��Գɷ����Ź㷺Ӧ�á��������������Ĵ�ͳ��ȡ�����Ǵ�ֲ������ȡ������ֲ����������������ﺬ���ϵͣ�ֲ�������ܵ�������Դ��������������Ӱ��ϴ�������Լ������ģ�ƹ��Ӧ�á����úϳ�����ѧ��������ƹ�������ϸ�������ϳ�������������ﱻ��Ϊ��һ�ֱ���Ե�������������Ϊ�µ��о��ȵ㡣���������������ĺϳɹ����У��ǻ�ת��ø������Ҫ���á����Ľ����������ǻ�ת��ø�ϳ����������������о���չ��Ϊ�������������Ľ�һ��Ӧ���ṩ�ο���
�����ؼ��ʣ���������; �ǻ���; �ǻ�ת��ø; �ϳ�����ѧ;
��������飺 ��ŵ�(1995—),Ů,˶ʿ�о���,lnuonan@163.com; �(1970—),��,��ʿ,����,lichun@bit.edu.cn;
�����ո����ڣ�2019-05-31
�������� ������Ȼ��ѧ�����ص���Ŀ(21736002);
����The applications of glycosyltransferases in the synthesis of triterpenoid saponins
����LI Nuonan LI Chun
����School of Chemistry and Chemical Engineering, Beijing Institute of Technology The State Key Laboratory of Bioreactor Engineering, East China University of Science and Technology
����Abstract��Triterpenoid saponins are usually composed of one or more glycosyl groups attached to hydrophobic aglycones, which are widely used as active ingredients in traditional Chinese herbal medicines. The traditional method for obtaining triterpenoid saponins is extracted from plants, due to the low content of triterpenoid saponins in plants and the limitation of plant growth by land resources, climate and environment, it has greatly restricted its large-scale promotion and application. Thus��It’s hard to be applied and popularized on large scale. The use of synthetic biology principles to design and construct microbial cell factories to synthesize triterpenoids is considered to be the most promising alternative and has become a new research hotspot. Glycosyltransferases play a key role in the synthesis of triterpenoid saponins. This article will describe the research progress in the synthesis of triterpenoid saponins using glycosyltransferases, and provide a reference for the further application of triterpenoid saponins.
����Keyword��triterpenoid saponins; glycosylation; glycosyltransferases; synthetic biology;
����Received�� 2019-05-31
������ ��
���������������һ����6�������ϩ��Ԫ��C5H8����ɵĽṹ�����Ļ������ֲ����������ﳣ�����ǻ�����ʽ�洢[1]——���������ա�������������ˮ����������Ԫ����һ�������ǻ�����[2,3]��ͼ1����ֲ�����ڵ����������������ֲ������������ʳ�ݶ����ֺ����źŴ����ȷ�������Ҫ����[2]���ִ�ҩ��ѧ�о�֤ʵ��һЩ������������������Ҳ�к�ǿ���������ԣ���˴��ڽϸߵ�ҩ�ü�ֵ[2]����ҽ�ƽ�����ҵ[4]��ʳƷ��ҵ[5,6]��ũҵ[7]�ȷ������Ӧ�ã��ܵ��㷺��ע���������������Ĵ�ͳ�Ʊ������Ǵ�ֲ������ȡ��������ֲ���к����ϵ�[5,8]������ȡ���ո��ӣ���ֲ֮���������ڽϳ����ܵ�����������Ӱ��ϴ�[9]����Ϊ��Ȼ������ȡ�ṩ�ȶ���ԭ����Դ�����������������ģ���������⣬Ҳ������ֲ��ϸ�������ķ��������������[10]������������ֲ��ϸ���������ڳ������������������ɱ��ϸߣ����Ҵ���Ŀ���л����IJ������ȶ�������[11]�����Խ��й�ҵ����������ѧ�ϳɷ����棬����������Ȼ����ṹ�ϸ��ӣ��ϳɹ��̷������ϳɵIJ����д��������칹�����Է��룬����ʵ�ֹ�ҵ�����������ھ����������ڶ̣�����������̼Դ�����ڽ��д��ģ���͵��ŵ㣬Ϊ���ֲ����Ȼ�����ȡ�����д��ڵ���Դ��ȱ�ͻ�����Ⱦ�������ṩ���µ�˼·[12]�����úϳ�����ѧ����������������������������������ϸ�������ѳ�Ϊ�����о����⡣
����ͼ1 �����������������ṹʽ
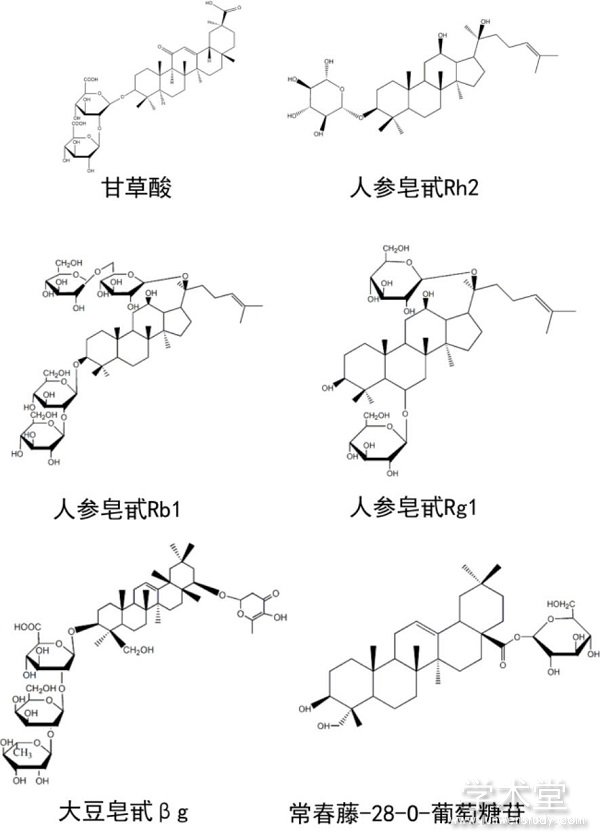
����Fig.1 Structural formulae of some triterpenoid saponins
�������úϳ�����ѧ��������������ϸ����������ֲ����Ȼ����Ĺؼ��Ƕ����л;�����н������ھ�ؼ�����Ԫ������������Ż��������Դ��������������������ԣ������Դ�л;�������Ż������������������ϳɹ����У����ƹǼܵ��ǻ����ǹؼ��ķ�Ӧ���������ǻ�ת��øʹ�ǻ�����Ȼ����֮���γ��ض������ռ����ϳ��������������ڶ���������Ӧ��ǰ�����Ʊ���״���з����Ļ����ϣ��������ǻ�ת��ø�������������պϳ��е�Ӧ�ã�Ϊ�������������δ���Ĺ�ҵ�������ṩ˼·��
����1 �������յ�Ӧ��ǰ�����Ʊ���״
����1.1 �������յ�Ӧ��ǰ��
������ֲ���У�������������ﱻ��Ϊ��ֲ�������ԭ�����ʳ�ݶ����ֺ���һ�����ұ�������[9,13]����ֲ������ֺ����źŴ����ȷ����������Ҫ����[14]��������Щ�����������Ҳ����������[15]����˳�����ҽҩ������������������ص�����������ʳƷ��ҩƷ����ױƷ������Ҳ���й㷺�������磬����Ϊ“���”���˲���Ϊһ�ִ�ͳ��������ҩ�����ҹ���ʹ����ʷ������ǧ�꣬����ũ���ݾ��������˲ξ��а�����Ŀ���������ٵĹ�Ч���˲�������һ����ԭ�˲ζ�����ԭ�˲���������չ���Ϊ��Ԫ���ǻ���������ܳ�[16]���ִ�ҩ��ѧ�о�֤ʵ���˲μ��˲���Ʒ�����ٴ�ҩ��������Ҫ�����������������������Щ�����������з���������[4,17]���˲�������ȡ�ﱻ�㷺Ӧ�õ������������������ж����˲�������ȡ����ص�ʳƷ������Ʒ��ҩƷ���ۡ����˲�ͬ����ӿƵij����������ļ�������ص㳣������װ��ֲ��ӳ����ٵ�Ҷ������ȡ�õ��ij�������ȡ���ڿ�����[18]��������[19]�ȷ�������ֳ���ǿ��Ч����ͨ��������ȡ��ɷֽ���HPLC���������������������ȡ�����к��ж�����չ�������������[20]����Ϊ��ͳ��ҩ�ĸʲݣ�����Ч�ɷָʲ���Ҳ��һ���������գ����б��λ��Ρ����ס�ƽ���ȹ�Ч[5]����ҩƷ����ױƷ����ҵ�й㷺Ӧ�ã�ͬʱ����ʲ��������ζ��Ҳ��������ζ�����ӵ�ʳƷ��[21]������������������������㷺����ˣ���θ�Ч��ȡ��������Ϊ�����ǹ�ע�Ľ��㡣
����1.2 �������յ��Ʊ���״
����������������ȡ�������������ķ�ʽ��Ҫ�Ǵ�ֲ������ȡ����Ӹʲ�����ȡ�ĸʲ���[22]�����˲�����ȡ���˲�����[23]���������ķ�չ������������ʽ�������ı�Ҳ�������֡����ȣ�����ֲ���ռ��������Դ��ֲ�����������һ��ϳ���ֲ�������ܵ����ա��¶ȡ����������Ӱ��ϴ���Σ���Щ�������������������ֲ��μ���л�����ֲ���к����ϵͣ��Һ����ܵ���������Ӱ��ϴ�[24,25]������֮�⣬��ֲ������ȡ��Щ������Ĺ��̽Ϸ������漰����ĥ���顢��ȡ�����롢Ũ��������ᾧ�Ȳ���[22]����ȡЧ�ʽϵͣ���ȡ���������õ������л��Լ���Ϊ�ܼ����������ķ�ҺҲ��Ի��������Ⱦ��
����ϸ��ȫ�������۵����Ϊ��ȡ��Ȼ���↑����һ���µ�·������ͨ��ֲ��ϸ�������ķ�����ȡֲ����Ȼ�����ֲ��ϸ������Ҳ�����Ŷ�Ӫ��Ҫ���Ͽ��������������׳��ֺֻ����������[26]�����⣬��ͬϸ��ϵ֮��ϳ���Ȼ������������ڽϴ���죬���ɸѡ�õ��ȶ��ĸ߲�ϸ��ϵҲ���о���Ա���ٵ�һ�����⣬ֲ��ϸ�����Խ��д��ģ��������Ҳ�谭���乤ҵ��Ӧ�á�
���������������ַ����⣬��ѧ�ϳɷ����������պϳ���Ҳ����ʵ�ִ��ģӦ�á������������սṹ���ӣ���ѧ�ϳɲ��跱�������跴Ӧ�����Ͽ����Һϳɹ����п��ܴ����ѷ�������Ի������Щ����ʹ�û�ѧ�ϳɷ��ھ���Ч���ϲ��߱������������Խ����ƹ㡣
���������Щ���⣬�������е���Ҫһ����ɫ�ġ��ɳ����ġ�����Ч��ߵ�����ģʽ��ͻ�ƴ�ͳ��������������������߱��������ڶ̡�����������̼Դ�����ƣ�Ϊ�ɳ�����չ�ṩ�˿��ܡ�Ϊ�����ͳ���Ʊ����������ıˣ��о���Ա����̽����������������ϸ��������ʵ�ָ�Ч��ɫ������ֲ����Ȼ���Ϊ�����������ೢ�ԣ�ͨ����������ϳ����༰����������Ѿ�ȡ����һЩ�����ijɹ���2013�꣬Keasling�����ڿ�ű��ҩ��ǰ��������ĺϳ���ȡ�õijɹ�Ϊ�����ṩ�˼��������[27]���˺�Խ��Խ��Ľṹ�����ӵ���������ﱻ�ϳɣ�������˲�����[28,29,30,31]����ѩ������[32,33]������������[34,35,36]�ȡ�������������ϳ���Ȼ����Ĺ����У�Ŀ�����Ԫ�����ھ���ڽ�����Ȼ����ĺϳ�;��������Ҫ��
�������������ڣ����������Ҫ��������ϩ�������ᣨIPP����Ԫ�ۺ϶��ɣ�IPP��Ҫ�ɼ�������;����MVA;�����ͼ�����-4-����;����MEP;����������ͼ2��������Ȼ���У����ƺͱ�����ͨ��MVA;���ϳɣ������ơ����ƺ�����ͨ��MEP;���ϳɣ�ͼ2��[2]�����������յĺϳɹ����У���һ��������ƹǼܶ������ķ�Ӧ��������ϩ����ø��OSC�����Ļ�����Ӧ����ͬ��ֲ�����ں������������OSCø�����Դ��γɲ�ͬ�����ƻ����Ǽܡ����ϸ��ɫ��P450ø��CYP450�������ƹǼܽ������Σ��õ����빦���Թ����ţ�-OH��-COOH�ȣ�������Ԫ[37,38]��CYP450���ܵĶ����Խ�һ���������γɵ����Ʋ���Ķ����ԣ�ͬʱ��CYP450����ʹ�ý�һ�����ǻ������γ�Ϊ���ܣ�Ҳ��������������ˮ���Ժ��������[2]����ֲ����Ȼ����ĺϳ��У����ǻ�����Ӧ��ø��Ҫ��UDP-�ǻ�ת��ø��UGT��������ø�Ժ���������Ϊ�ǻ����壬��������Ԫ��Ϊ�ǻ����壬��UGT�Ĵ��£�����֮������γ����ռ���������������[39]��
����ͼ2 MVA ;����MEP;��ʾ��ͼ
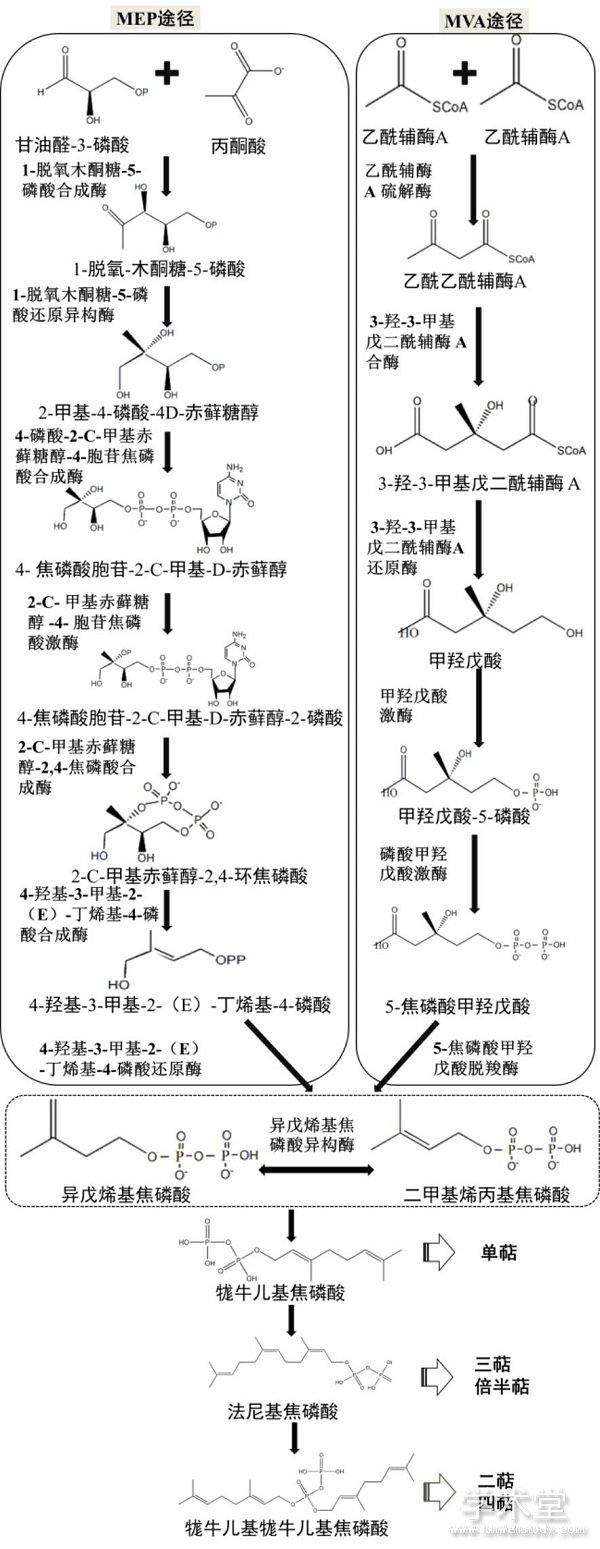
����Fig.2 Schematic diagram of MVA pathway and MEP pathway
����1.3 �������պϳ���ػ�����ھ�
����ͨ����ֲ����Ȼ�����л;�����н����������ھ�ֲ����Ȼ�����л;������������Ԫ��������ʵ���������յĸ�Ч������
�������Ų������IJ��ϱ��ͽ�����Խ��Խ��ķ�ģʽֲ��������ҩ��ֲ��Ļ�������̱�����[8,40,41]��������Ϣ������Ԥ���������պϳ���صĻ���[42]��ͨ������ת¼���������ھ��ѡ������ͨ���Ƚϸ߲��͵Ͳ�ֲ�����֮֯���ת¼����죬�����ھ���������պϳ���صĹؼ��������磬ͨ���Ըʲݵ�ת¼�����ݽ��з�����Liu��[43]�ھ���773����ʲ��дμ���л����ϳ���صĻ���40���������Ǽܺϳ���صĻ���16����ʲ���ϳ���صĻ�������ڲε�ת¼�������[17]��Zhang��ͨ������ڲε�ת¼����ͷ��װ�Լ���ͨ��RNA-seq��������19.6 Gbp��ת¼�������з�����66,403�� Unigenes����������34,639��Unigenes������ע�ͣ���������Ԥ����������չǼ�������ص�34��ϸ��ɫ��P450ø�����18��UDP-�ǻ�ת��ø����Tang��[44]�ӽ�״���ߣ�һ���˲���ֲ���ת¼�����״��ھ���4����չ���������ȩ���ת��ø���������Ե�����չ����C-3λ�ǻ���ת��������ȩ����ţ�������չ���3-O-β-������ȩ�ᣬΪ�ϳ���չ������˲����մ��������õĻ�����
���������ھ����������ǿ��ø��Ҳ��ѧ�߽������ӷ��Ե�øӦ�õ���Ȼ����ϳ�;���С�Dai��[45]������һ�������ڿݲ�ѿ�߸˾�168��Bacillus subtilis 168�����ǻ�ת��øBs-YjiC���ϳ��˲����գ�����ʵ��֤ʵ����ԭ�˲�������PPT����Ϊ�ǻ����壬UDP-��������Ϊ�ǻ�����ʱ��Bs-YjiC�ܽ������ǻ���ת�Ƶ�PPT��C3λOH��C6λOH��C12λOH�ϣ��ϳ�������PPT���˲����գ����а����˲�����Rh1�����ַ���Ȼ���˲����գ���������������ĵ����ӷ��Ե��ǻ�ת��ø�ںϳ������˲����շ�����кܴ��DZ��������һ�������ڿݲ�ѿ�߸˾� Bacillus subtilis�ĵ����ӷ��Ե�øUGT109A1Ҳչʾ����ǿ�ĵ����ӷ��ԣ���UGT109A1�ڴ˾�����Դ����ֱ����˲�����Re��Rf��Rh1����R1��Ϊ�ǻ����壬UDP-����Ϊ�ǻ�����������ⷴӦ�����������UGT109A1���Խ��ǻ�ת�Ƶ��˲�����Re���˲�����R1��C-3λOH�ϣ�Ҳ���Խ��ǻ�ת�Ƶ��˲����� Rf���˲�����Rh1��C-3λ�ǻ���C-12λ�ǻ��ϣ������а������ַ���Ȼ���˲�����[46]�����⣬Ҳ���о������ý�ĸ��Դ���ǻ�ת��øUGT51�������˲����գ�ͨ������UGT51�ľ���ṹ�������ݾ���ṹ������а�������ƣ����������ԭ�˲ζ��������˲����� Rh2��Ч�������1800����ͨ�����������ǻ�ת��øUGT51���뵽�߱���ԭ�˲ζ����ϳ�;������ƽ�ĸ�У�ʹ����ƽ�ĸ�����˲�����Rh2�IJ�����0.0032 mg/g DCW ��Dry Cell Weight�����ӵ�0.39 mg/g DCW[47]����Щ�о���ʾ���˵����ӷ��Ե�ø��ֲ��������������Ȼ������Դ�ϳ��еľ�DZ����Ϊ���õ����ӷ��Ե�ø������Ȼ����ϳ��ṩ��ָ����
����2 �ǻ�ת��ø���������յĺϳ�
����������������ˮ������Ԫ����һ�������ǻ����ɣ������ǻ�ת��ø����һ������������Ҫ���ã��ǻ����ı���ֲ�������ƻ������һЩ�������ʺ��������[48]��
�����ǻ�ת��ø��һ�ཫ����ǻ�����ת�Ƶ���������ϵ�ø��Ϊ�ǻ�ת��ø�ṩ�ǻ�����ķ��ӽ϶࣬������Ҫ��Ϊ�������Ǻ����������Լ����ữ����[49]��������UDP-����Ϊ�ǻ������һ���ǻ�ת��ø����ΪUDP-�ǻ�ת��ø[50]���ǻ�����Ӧ����Ȼ��ֲ��㷺����������������ʡ�֬�ʡ������Լ�һЩ��ȻС���ӣ���Ҫ��һЩ�μ���л�����[51]���ǻ�������������������ֱ�ӷ��ӹ㷺���ܣ���������������ά��ϸ���ṹ�������ԡ���Ϣ�洢�봫�䡢����ʶ��ϸ��֮������á�ϸ�����ڡ����߷�Ӧ�����Ժͻ�ѧ������[8,51,52]��
����2.1 �ǻ�ת��ø�ķ��༰������
�����ǻ���һ�������Ȼ����ϳɹ����е����һ����Ӧ���������γ�ֲ��μ���л����Ķ����ԡ�Ŀǰ�ձ��Ͽɵ��ǻ�ת��ø������ǰ��հ������������ƶ������з��࣬CAZy���ݿ⣨http://www.cazy.org�����ѱ������ǻ�ת��ø�����˷��࣬���ݰ������������ƶȡ������ƵȲ��죬�����Ϊ106������[48]���������ǻ�ת��ø�����γɵ����ռ����ͷ��࣬�ֿɷ�ΪO-���ռ����ǻ�ת��ø��N-���ռ����ǻ�ת��ø��S-���ռ����ǻ�ת��ø��C-���ռ����ǻ�ת��ø�ȣ����У���ֲ����Ȼ�����γɵ��ǻ�ת��ø��O-���ռ���Ϊ��������ΪN-���ռ��ͺ�S-���ռ���[51]��
�����ǻ�ת��ø���ǻ�ת�Ƶ��˵��ǻ������ϣ����ǻ������ϵ���ͷ̼������ת�Ƶ��ǻ��������Ƿ����ı�ɽ��ǻ�ת��ø��Ϊ�����ͺͷ�ת�ͣ����������仯��Ϊ�����ͣ��������ı伴Ϊ��ת��[51]��ͼ3������ת���ǻ�ת��ø���õ���ֱ���û�SN2����Ӧ��ø������λ�㰱����IJ�����Ϊ���������������˹������γɹ���̬���������ʴ���������϶�ȡһ�����Ӵ�ʹ�����칹������˹���������ʹ���ռ��γɣ��������ı䡣���ڱ����͵��ǻ�ת��ø�Ĵ����������ۣ�һ�ּ����DZ������ǻ�ת��ø��ѭ˫�û����ۣ����ǻ���ø���γɹ����м��壬��ת�Ƶ�����������γ����ռ�[10]��
����������������������������յĺϳ�Ϊ���������ǻ�ת��ø���ھ�Ӧ�á�
����ͼ3 ��ת�ͺͱ������ǻ�ת��ø������
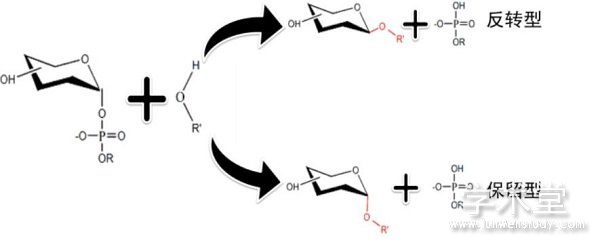
����Fig.3 Inverting and retaining glycosyltransferase catalysis mechanism
����2.2 �ǻ�ת��ø���������պϳ��е�Ӧ��
����2.2.1 �˲����պϳ���ص��ǻ�ת��ø
�����˲����ҹ�������ҩ������Ϊ“���”���˲ζ��ڵ���Ѫѹ����л�����ߵȷ����������[53,54]����ֱ���˲������������˲��б���ȡ�������˲ε�ҩ�û����ű�֤ʵ[53]�����е��˲���������ﱻȷ�����˲η������������[53]����Ѫѹ[53]���������ȹ�Ч����Ҫ����[4,53,55,56,57]����2013�꣬Dai��[28]ͨ������ƽ�ĸ�������������˲εĴ���ϩ����-II��ø�����ԭ�˲ζ�����ø�����Լ����������Ͻ��NADPH-ϸ��ɫ��P450��ԭø���ɹ�������ƽ�ĸ�й�����ԭ�˲ζ�����PPD���ϳ�·����ԭ�˲ζ��������ﵽ��0.05 mg/g DCW��֮����ͨ��������ض̵�3-�ǻ�-3-��-�������øA��ԭø��������������ø������ϩ��ø����2,3-������ϩ��ø����������ǰ����ϩ��2,3-������ϩ�Ĺ�Ӧ����ͨ����ԭ�˲ζ�����ø��������������Ż�����˸�ø����ƽ�ĸ�еı���������Щ���Թ�ͬʹ��ԭ�˲ζ����IJ��������262�������ͨ������͵ķ���ʹ��ԭ�˲ζ����IJ����ﵽ��8.40 mg/g DCW ��1189 mg/L��������ϩ����-II�IJ����ﵽ��10.94 mg/g DCW ��1548 mg/L�������о�Ϊ������ƽ�ĸ�����˲������ṩ�˻�����2015�꣬�й���ѧԺ�Ϻ�ֲ��������̬�о������й���ѧԺ�Ϻ�ҩ���о����Լ�������ѧ������ѧѧԺ������ҽѧ��ѧ�о������Ϻ��������˲��п�¡�õ�������UGT��������UGTPg45ѡ���Եؽ������ǻ�ת�Ƶ�ԭ�˲ζ��������˲����յ�C3�ǻ��ϣ�UGTPg29ѡ���Եؽ�һ�������ǻ���ת�Ƶ�Rh2��C3λ�������ǻ����ϡ����ڴˣ����������ǻ�ת��ø����ת�Ƶ����Ժϳ�ԭ�˲ζ�������ƽ�ĸ�У�ʵ��������������������ϡ�е��˲�����Rh2��Rg3[58]���˺��о��Ŷ�ͨ������ƽ�ĸ����������MVA;�������Ż��Լ����CYP450�������ˮƽ��ԭ�˲ζ�����ҡƿ�����ﵽ��529.0 mg/L����10L�������ɴﵽ11.02 g/L�������������˲����յ�ǰ��ԭ�˲ζ����Ĺ�Ӧ����ͨ�������ǻ�ת��øUGTPg45�Ļ�������������������ӹ��̸��죬��ͨ����UGTPg45���ж������������Ч�ʣ����⣬ͨ���ھ��µ��ǻ�ת��øUGTPn50������Щ���ԵĹ�ͬ�����£�ͬʱ��������ø�����˲�����Rh2��ҡƿ�����ﵽ��179.3 mg/L����10L �����в����ﵽ��2.25 g/L [30]��2014�꣬Zhou����ͨ����NCBI���ݿ�����˲λ������ݿ����ھ���479689����װ��cDNA���У�ͨ������ֲ��μ���л�����ǻ�ת��ø�������У�PSPG-box��ȷ����512��DZ�ڵ�UGT�������У�����¡�õ���16���������У�����Щ�����з�����һ�����Դ������˲�����CK���ǻ�ת��øUGTPg1[59]���˺��о����ֱ�����ƽ�ĸ[47]���ݲ�ѿ�߸˾�[46]�������з�����һЩ�����ӷ��Ե�ø���ֱ���Դ������˲�����Rh2��һЩ����Ȼ���˲����ղ����Щ�о���ȫ��ĵؽ���������˲����յĺϳ�·����Ϊʵ����Ȼ����ĺϳ�����ѧ���켰��������������Ȼ�����ṩ�˷�����
����2.2.2 �ʲݴ���������ϳ���ص��ǻ�ת��ø
�����ʲ����ҹ���ͳ��ҩ������“ʮ���Ų�”���������о����֣��ʲݼ���ȡ�ԸʲݵĻ��Գɷ־߱���̵[60]��ƽ��[61]��������[62]�ͱ��λ���[63]�ȹ�Ч���ʲ��е���������ﺬ����5%-11%����[64]��Ŀǰ���ڸʲ��з���õ����������վ�Ϊ��չ�����������Ԫ��������[64]�����У��Ըʲݴ�����Ϊ��Ԫ���������������ռ�����ϴ�ǰ���ʲݴ���ϳ���صĹؼ�ø���ϳ�;������̱�����[65,66,67]���ʲݴ����Ǹʲ������Ԫ�����ǻ�ת��ø�������£�����������ȩ����ű�ת�Ƶ��ʲݴ����C-3λOH�ϣ��õ��ʲ��ᣨͼ1����Ŀǰ����ʲ���ϳ���ص��ǻ�ת��ø�ı������٣���2016�꣬Xu��[68]�������ڸʲ����ھ���һ���µ��ǻ�ת��ø����ø���Դ�����������ת�ǻ���Ӧ��������о�δ��������������2018�꣬He����[69]ͨ�����ѱ����ĵ��������ʲ�ת¼�����ݽ��з������ھ�����γ�C-30λ�������ǻ�ת��ø������43����ѡ�����У��ɹ���¡�õ���16�������Ըʲ�����Ϊ�ǻ����壬��UDP-��������Ϊ�ǻ����壬��֤�ھ��µ��ǻ�ת��ø�Ĵ����ԣ�����ɸѡ�õ���һ���µ��ǻ�ת��øUGT73F17����ø�ɽ������ǻ���ת�Ƶ��ʲ����30λ�ǻ��ϣ����ɸʲ�����A3��UGT73F17���廷����������C-30/C-29���Ȼ������ϸ�����������ԣ������ǻ�������ֳ��߶ȵ��ӷ��ԣ��Ҹ�øֻ�ܴ���չ��������Ƽ����������C29/30λ�ǻ���������֮�⣬Liu��[70]����������������ŷ��ɽ����ǻ�ת��øBVEc���ʲݴ����������ǻ���������ǻ�ת��øBVEc���Խ������ǻ�ת�Ƶ��ʲݴ����3��λ�ϣ�����3-O-�������ǻ��ʲݴ��ᡣ��Щ�о���̽���ʲ����������������ϳɷ�ʽ����ָ�����塣
����2.2.3 �����ռ�������ǻ�ת��ø
����������Ҫ�������������Ǵ����գ���������Ԫ��ͬ����ΪDDMP�����պ�Group A���գ�DDMP�����Դ���B��Ϊ��Ԫ��Group A�����Դ���A��Ϊ��Ԫ��DDMP���ռ�������������彡����һ�����洦[71,72]������Group A����������ɬζ��Ӱ����ڸ�[2]��������βg�ǵ��͵�DDMP�����գ�Ҳ�Ǵ��е���Ҫ�����գ��ڴ���B��3��λ�ǻ��������������ǻ�——������ȩ����������ǻ��������ǻ���UGT73P2��UGT91H4�ֱ���ת�Ƶڶ����͵������ǻ���������[73]���������ڴ���������λ��ת��������ȩ����ŵ��ǻ�ת��ø���ڴ������б���[74]��������ػ�����Ϣ��δ������������C-3λ���ǻ�����Group A���յ�C-22λ�ǻ�Ҳ�����ǻ���ϣ�Sayama ��[75] ������UGT73F4��UGT73F2�ɷֱ�ľ�Ǻ�������ת�Ƶ��Ѿ���C-22λ�ǻ���ϵİ��������ϣ������������ǻ�ת�Ƶ�C-22λ�ǻ��ϵ��ǻ�ת��ø��δ��������
����3 չ��
�������úϳ�����ѧ�ʹ�л�����ֶΣ���ƿ��١���ݵ���Դ�ϳ��������������ķ������ž��Ӧ��ǰ��������������У��ǻ�ת��ø���Źؼ����á������ǻ�ת��ø���ж��ص�����ѡ���Ժ�����ѡ���ԣ���ˣ��ڽ���ø�ľ���ṹ�����ϣ�������ͬ���ǻ�ת��ø���������յIJ�ͬλ�úͲ�ͬ�������γ��еĴ����ƶ��ڸ�Ч�ϳ��������ռ�������������������Ҫ���塣Ŀǰ���о��϶���ǻ�ת��ø��Ҫ�Dz����γ�O-���ռ����ǻ�ת��ø�������ڲ����γ�N-���ռ���S-���ռ��Լ�C-���ռ����ǻ�ת��ø���о����٣������ǻ�ת��ø���ںϳ��µ����ջ�����ر��Ƕ�����������������������˵�Ǽ����������ġ�
����������������ǰ���úϳ�����ѧ�����������ǻ�ת��ø�����ǻ�����Ӧ�ϳ����������������о��ܵ��㷺��ע������Ŀǰͨ����������ϸ����������ȡ��Ȼ�����������ʽ��Ԥ�ڻ���һ����࣬������Ȼ����ϳ�;����صĻ���Ԫ�����ھ��Լ��ϳ�·���Ľ��������ڳ���̽���Σ���ξ�ȷ��Ч��Ԥ����ػ���Ԫ��һֱ���������ٵ����⡣���⣬��������ϸ��������ȡֲ����Ȼ����ķ�ʽ��������ȫ�����ͳ�ķ���������ϳ�һЩ��Ȼ����IJ����в����Դﵽ��ҵ��Ҫ������Ԥ���������źϳ�����ѧ�ʹ�л���̵ķ�չ���Լ���ͨ���������ʹ�л��ѧ�����ķ�չ����ģʽֲ��Ļ������ת¼��IJ�����Ӹ�Чȷ��ͨ������Щ�����顢ת¼�����ݽ����ھ������ӿ�������������ϳ���ص��»���ķ��֣�����������������Ȼ����ϳ�;���Ľ���Ҳ���������롣�������˹��������ۺͼ����ķ�չ��δ����ͨ�����˹����ܵ��Զ����������»�����ھ�ɸѡ����л;�����Ż�����Чϸ�������Ĺ�����������������ؽ������������ķѡ���ʡʱ��ɱ���
����ͨ���ھ���ػ���Ԫ������ƺϳ�·��������ϸ����������Ч��ȡ������Ȼ���ォ������Ϊδ��һ��ʱ����о�����Щ�꣬���Ž�ĸ��������������ֲ����Ȼ���﷽��ȡ�������Ž�չ�������ĸ����������;������������չ��Ϊһ���ʺ���������������﹤ҵ�������Ĺ��ա������ڲ��õĽ��������ǽ�ӭ��һ��ȫ�µ���������ϳ�ֲ����Ȼ����ĺϳ�����ѧʱ����
������ �� ˵ ��
����CYP450——ϸ��ɫ��P450ø
����DCW——ϸ������
����DMAPP——����ϩ����������
����HPLC——��ЧҺ��ɫ��
����IPP——����ϩ��������
����MVA——��������
����MEP——������-4-����
����NADPH——��ԭ�������������ʶ�����������
����OSC——������ϩ����ø
����PPT——ԭ�˲�����
����PSPG-box——ֲ��μ���л�����ǻ�ת��ø��������
����UGT——���ն������ǻ�ת��ø
����βAS——β-����֬����ø
���������
����[1] Vincken J P, Heng L, Groot A D, et al. Saponins, classification and occurrence in the plant kingdom[J]. Phytochemistry, 2007, 68(3): 275-297.
����[2] Sawai S, Saito K. Triterpenoid biosynthesis and engineering in plants[J]. Frontiers in Plant Science, 2011, 2(25): 1-8.
����[3] Gauthier C, Legault J, Pichette A. Recent progress in the synthesis of naturally occurring triterpenoid saponins[J]. Mini-Reviews in Organic Chemistry. 2009, 6(4): 321-344.
����[4] Qi L W, Wang C Z, Yuan C S. Ginsenosides from American ginseng: chemical and pharmacological diversity[J]. Phytochemistry, 2011, 72(8): 689-699.
����[5] Zhao Y J, Lv B, Feng X D, et al. Perspective on biotransformation and de novo biosynthesis of licorice constituents[J]. Journal of Agricultural and Food Chemistry, 2017, 65(51): 11147-11156.
����[6] Itkin M, Davidovich-Rikanati R, Cohen S, et al. The biosynthetic pathway of the nonsugar, high-intensity sweetener mogroside V from Siraitia grosvenorii[J]. Proceedings of the National Academy of Sciences. 2016, 113(47): E7619-E7628.
����[7] Scognamiglio M, D'Abrosca B, Fiumano V, et al. Oleanane saponins from Bellis sylvestris Cyr. and evaluation of their phytotoxicity on Aegilops geniculata Roth[J]. Phytochemistry, 2012, 84(12): 125-134.
����[8] Zhao Y J, Li C. Biosynthesis of plant triterpenoid saponins in microbial cell factories[J]. Journal of Agricultural and Food Chemistry, 2018, 66(46): 12155?12165.
����[9] Szakiel A, P?czkowski C, Henry M. Influence of environmental biotic factors on the content of saponins in plants[J]. Phytochemistry Reviews, 2011, 10(4): 471-491.
����[10] Lairson L L, Henrissat B, Davies G J, et al. Glycosyltransferases: structures, functions, and mechanisms[J]. Annual Review of Biochemistry, 2008, 77: 521-555.
����[11] Roberts S C. Production and engineering of terpenoids in plant cell culture[J]. Nature Chemical Biology, 2007, 3(7): 387-395.
����[12] Zhao F L, Bai P, Nan W H, et al. A modular engineering strategy for high�\level production of protopanaxadiol from ethanol by Saccharomyces cerevisiae[J]. AIChE Journal, 2019, 65(3): 866-874.
����[13] Kuzina V, Ekstr?m C T, Andersen S B. Identification of defense compounds in Barbarea vulgaris against the herbivore Phyllotreta nemorum by an ecometabolomic approach[J]. Plant Physiology, 2009, 151(4): 1977-1990.
����[14] Augustin J M, Sylvia D, Tetsuro S, et al. UDP-glycosyltransferases from the UGT73C subfamily in Barbarea vulgaris catalyze sapogenin 3-O-glucosylation in saponin-mediated insect resistance[J]. Plant Physiology, 2012, 160(4): 1881-1895.
����[15] Xu J, Wang X D, Zhang H Y, et al. Synthesis of triterpenoid derivatives and their anti-tumor and anti-hepatic fibrosis activities[J]. Natural Product Research, 2018: 1-7.DOI:10.1080/14786419.2018.1499642.
����[16] ��ס��, ����, ��־��, ��. ֲ����Ȼ����ϳ�����ѧ�о�[J]. �й���ѧԺԺ��, 2018, 33(11): 106-116.
����[17] Zhang S P, Wu Y Y, Jin J, et al. De novo characterization of Panax japonicus C. A. Mey transcriptome and genes related to triterpenoid saponin biosynthesis[J]. Biochemical and Biophysical Research Communications, 2015, 466(3): 450-455.
����[18] Gül?in ?, Mshvildadze V, Gepdiremen A, et al. The antioxidant activity of a triterpenoid glycoside isolated from the berries of Hedera colchica: 3-O-(beta-D-glucopyranosyl)-hederagenin[J]. Phytotherapy Research, 2006, 20(2): 130-134.
����[19] Cheng L, Liang S, Wu J, et al. A hederagenin saponin isolated from Clematis ganpiniana induces apoptosis in breast cancer cells via the mitochondrial pathway[J]. Oncology Letters, 2018, 15(2): 1737-1743.
����[20] ������, ������, ��ѩ��, ��. ������ҩ��HPLCָ��ͼ��8�ֳɷֵĺ����ⶨ����[J]. ����ҩ�ƴ�ѧѧ��, 2017, 34(11): 979-986.
����[21] ������, ����ƽ, �Ų�, ��. �ʲ���Ч�ɷֵ�ҩ�������о���չ[J]. ��Ȼ�����о��뿪��, 2006,18(2): 343-347.
����[22] ������, ��, ����ΰ. �ʲ����Ʊ��¹��յ��о�[J]. ̫ԭ������ѧѧ��, 2001, 32(3): 271-273.
����[23] ������, ����, ����, ��. ����Һ���Ʊ�ɫ���봿������Ҷ߰���˲���߰����Rb3[J]. ��У��ѧ����ѧ��, 2005, 19(2): 192-196.
����[24] ����ӱ, ������. ��, ��, �����ʩ�ö��˲�����Ӱ����о�[J]. ����ָ��, 1996, (6): 36-37.
����[25] ���ΰ�,�����. ���������Բ���̼ˮ��������˲���߰������Ӱ��[J]. ����ũҵ��ѧѧ��, 1994, (3): 15-17.
����[26] �Ͻ���, �Ե���, ��ï��, ��. ֲ��ϸ������������ͪ������о���չ[J]. �й����﹤����־, 2001, 21(1): 47-50.
����[27] Paddon C J, Westfall P J, Pitera D J, et al. High-level semi-synthetic production of the potent antimalarial artemisinin[J]. Nature, 2013, 496(7446): 528.
����[28] Dai Z B, Liu Y, Zhang X A, et al. Metabolic engineering of Saccharomyces cerevisiae for production of ginsenosides[J]. Metabolic Engineering, 2013, 20: 146-156.
����[29] Dai Z B, Wang B B, Liu Y, et al. Producing aglycons of ginsenosides in bakers’yeast[J]. Scientific Reports, 2014, 4: 3698.
����[30] Wang P P, Wei W, Ye W, et al. Synthesizing ginsenoside Rh2 in Saccharomyces cerevisiae cell factory at high-efficiency[J]. Cell Discovery, 2019, 5(1): 5.
����[31] Jung S C, Kim W, Park S C, et al. Two ginseng UDP-glycosyltransferases synthesize ginsenoside Rg3 and Rd[J]. Plant and Cell Physiology, 2014, 55(12): 2177-2188.
����[32] Kim O T, Um Y, Jin M L, et al. A novel multifunctional C-23 oxidase, CYP714E19, is involved in asiaticoside biosynthesis[J]. Plant and Cell Physiology, 2018, 59(6): 1200-1213.
����[33] Kim O T, Jin M L, Lee D Y, et al. Characterization of the asiatic acid glucosyltransferase, UGT73AH1, involved in asiaticoside biosynthesis in Centella asiatica (L.) Urban[J]. International Journal of Molecular Sciences, 2017, 18(12): 2630.
����[34] Han J Y, Chun J H, Oh S A, et al. Transcriptomic analysis of Kalopanax septemlobus and characterization of KsBAS, CYP716A94 and CYP72A397 genes involved in hederagenin saponin biosynthesis[J]. Plant and Cell Physiology, 2017, 59(2): 319–330.
����[35] Erthmann P ?, Agerbirk N, Bak S. A tandem array of UDP-glycosyltransferases from the UGT73C subfamily glycosylate sapogenins, forming a spectrum of mono- and bisdesmosidic saponins[J]. Plant Molecular Biology, 2018, 97(1/2): 1-19.
����[36] Liu Q, Khakimov B, Cárdenas P D, et al. The cytochrome P450 CYP72A552 is key to production of hederagenin�\based saponins that mediate plant defense against herbivores[J]. New Phytologist, 2019, 222(3): 1599-1609.
����[37] Sun W T, Qin L, Xue H J, et al. Novel trends for producing plant triterpenoids in yeast[J]. Critical Reviews in Biotechnology, 2019, 39(5): 618-632.
����[38] Augustin J M, Kuzina V, Andersen S B, et al. Molecular activities, biosynthesis and evolution of triterpenoid saponins[J]. Phytochemistry, 2011, 72(6): 435-457.
����[39] Seki H, Tamura K, Muranaka T. P450s and UGTs: key players in the structural diversity of triterpenoid saponins[J]. Plant and Cell Physiology, 2015, 56(8): 1463-1471.
����[40] Jeena G S, SFatima, Tripathi P, et al. Comparative transcriptome analysis of shoot and root tissue of Bacopa monnieri identifies potential genes related to triterpenoid saponin biosynthesis[J]. BMC Genomics, 2017, 18(1): 490.
����[41] Luo H M, Sun C, Sun Y Z, et al. Analysis of the transcriptome of Panax notoginseng root uncovers putative triterpene saponin-biosynthetic genes and genetic markers[J]. BMC Genomics, 2011, 12(5): S5.
����[42] Moses T, Pollier J, Faizal A, et al. Unraveling the triterpenoid saponin biosynthesis of the African shrub Maesa lanceolata[J]. Molecular Plant, 2015, 8(1): 122-135.
����[43] Liu Y L, Zhang P F, Song M L, et al. Transcriptome analysis and development of SSR molecular markers in Glycyrrhiza uralensis Fisch[J]. Plos One, 2015, 10(11): e0143017.
����[44] Tang Q Y, Chen G, Song W L, et al. Transcriptome analysis of Panax zingiberensis identifies genes encoding oleanolic acid glucuronosyltransferase involved in the biosynthesis of oleanane-type ginsenosides[J]. Planta, 2018, 249(2): 393–406.
����[45] Dai L H, Li J, Yang J G, et al. Use of a promiscuous glycosyltransferase from Bacillus subtilis 168 for the enzymatic synthesis of novel protopanaxatriol-type ginsenosides[J]. Journal of Agricultural and Food Chemistry, 2018, 66(4): 943?949.
����[46] Zhang T T, Gong T, Hu Z F, et al. Enzymatic synthesis of unnatural ginsenosides using a promiscuous UDP-glucosyltransferase from Bacillus subtilis[J]. Molecules, 2018, 23(11): 2797.
����[47] Zhuang Y, Yang G Y, Chen X H, et al. Biosynthesis of plant-derived ginsenoside Rh2 in yeast via repurposing a key promiscuous microbial enzyme[J]. Metabolic Engineering, 2017, 42: 25-32.
����[48] Rahimi S, Kim J, Mijakovic I, et al. Triterpenoid-biosynthetic UDP-glycosyltransferases from plants[J]. Biotechnology Advances, 2019. DOI:org/10.1016/j.biotechadv.2019.04.016.
����[49] Gloster T M. Advances in understanding glycosyltransferases from a structural perspective[J]. Current Opinion in Structural Biology, 2014, 28: 131-141.
����[50] Meech R, Hu D G, McKinnon R A, et al. The UDP-glycosyltransferase (UGT) superfamily: new members, new functions, and novel paradigms[J]. Physiological Reviews, 2019, 99(2): 1153-1222.
����[51] Liang D M, Liu J H, Wu H, et al. Glycosyltransferases: mechanisms and applications in natural product development[J]. Chemical Society Reviews, 2015, 44(22): 8350-8374.
����[52] Osbourn A. Saponins and plant defence — a soap story[J]. Trends in Plant Science, 1996, 1(1): 4-9.
����[53] Leung K W, Wong A S T. Pharmacology of ginsenosides: a literature review[J]. Chinese Medicine, 2010, 5(1): 20.
����[54] Lu J, Yao L, Li J X, et al. Characterization of UDP-glycosyltransferase involved in biosynthesis of ginsenosides Rg1 and Rb1 and identification of critical conserved amino acid residues for its function[J]. Journal of Agricultural and Food Chemistry, 2018, 66(36): 9446-9455.
����[55] Xu Q F, Fang X L, Chen D F. Pharmacokinetics and bioavailability of ginsenoside Rb1 and Rg1 from Panax notoginseng in rats[J]. Journal of Ethnopharmacology, 2003, 84(2): 187-192.
����[56] Lee S J, Lee J S, Lee E, et al. The ginsenoside metabolite compound K inhibits hormone-independent breast cancer through downregulation of cyclin D1[J]. Journal of Functional Foods, 2018, 46: 159-166.
����[57] Liao L M, Zhang Y, Lin S F, et al. Enzymatic Transformation from protopanaxadiol ginsenoside Rb1 into rare ginsenoside C-K and its anti-cancer activity[J]. Advanced Materials Research, 2013, 641: 752-755.
����[58] Wang P P, Wei Y J, Fan Y, et al. Production of bioactive ginsenosides Rh2 and Rg3 by metabolically engineered yeasts[J]. Metabolic Engineering, 2015, 29: 97-105.
����[59] Yan X, Fan Y, Wei W, et al. Production of bioactive ginsenoside compound K in metabolically engineered yeast[J]. Cell Research, 2014, 24(6): 770.
����[60] ��ѩ��, ����ȫ, κʤ��, ��. �ʲݼ�����Գɷֵ�ҩ�������о���չ[J]. �й���ҩ��־, 2009, 34(21): 2695-2700.
����[61] Armanini D, Fiore C, Mattarello M J, et al. History of the endocrine effects of licorice[J]. Experimental and Clinical Endocrinology & Diabetes. 2002, 110(06): 257-261.
����[62] Cinatl J, Morgenstern B, Bauer G, et al. Glycyrrhizin, an active component of liquorice roots, and replication of SARS-associated coronavirus[J]. The Lancet, 2003, 361(9374): 2045-2046.
����[63] Mabuchi A, Wake K, Marlini M, et al. Protection by glycyrrhizin against warm ischemia-reperfusion-induced cellular injury and derangement of the microcirculatory blood flow in the rat liver[J]. Microcirculation, 2010, 16(4): 364-376.
����[64] л��, ������,����ƽ. �ʲ���ֲ��������������о�����[J]. ���ݻ���, 2004,32(1): 1-5.
����[65] Zhu M, Wang C X, Sun W T, et al. Boosting 11-oxo-β-amyrin and glycyrrhetinic acid synthesis in Saccharomyces cerevisiae via pairing novel oxidation and reduction system from legume plants[J]. Metabolic Engineering, 2018, 45: 43-50.
����[66] Seki H, Sawai S, Ohyama K, et al. Triterpene functional genomics in licorice for identification of CYP72A154 involved in the biosynthesis of glycyrrhizin[J]. The Plant Cell, 2011, 23(11): 4112-4123.
����[67] Seki H, Ohyama K, Sawai S, et al. Licorice β-amyrin 11-oxidase, a cytochrome P450 with a key role in the biosynthesis of the triterpene sweetener glycyrrhizin[J]. Proceedings of the National Academy of Sciences of the United States of America, 2008, 105(37): 14204-14209.
����[68] Xu G J, Cai W, Gao W, et al. A novel glucuronosyltransferase has an unprecedented ability to catalyse continuous two-step glucuronosylation of glycyrrhetinic acid to yield glycyrrhizin[J]. New Phytologist, 2016, 212(1): 123–135.
����[69] He J B, Chen K, Hu Z M, et al. UGT73F17, a new glycosyltransferase from Glycyrrhiza uralensis, catalyzes the regiospecific glycosylation of pentacyclic triterpenoids[J]. Chemical Communications, 2018, 54(62): 8594-8597.
����[70] Liu X C, Zhang L, Feng X D, et al. Biosynthesis of glycyrrhetinic acid-3-O-monoglucose using glycosyltransferase UGT73C11 from Barbarea vulgaris[J]. Industrial & Engineering Chemistry Research, 2017, 56(51): 14949-14958.
����[71] Lee S O, Simons A L, Murphy P A, et al. Soyasaponins lowered plasma cholesterol and increased fecal bile acids in female golden Syrian hamsters[J]. Experimental Biology and Medicine, 2005, 230(7): 472-478.
����[72] Kinjo J, Imagire M, Udayama M, et al. Structure-hepatoprotective relationships study of soyasaponins I-IV having soyasapogenol B as aglycone[J]. Planta Medica, 1998, 64(03): 233-236.
����[73] Shibuya M, Nishimura K, Yasuyama N, et al. Identification and characterization of glycosyltransferases involved in the biosynthesis of soyasapoin I in Glycine max[J]. FEBS Letters, 2010, 584(11): 2258-2264.
����[74] Kurosawa Y, Takahara H, Shiraiwa M. UDP-glucuronic acid: soyasapogenol glucuronosyltransferase involved in saponin biosynthesis in germinating soybean seeds[J]. Planta, 2002, 215(4): 620–629.
����[75] Sayama T, Ono E, Takagi K, et al. The Sg-1 glycosyltransferase locus regulates structural diversity of triterpenoid saponins of soybean[J]. The Plant Cell, 2012, 24(5): 2123–2138.