摘 要: 运用点击反应将四苯乙烯基乙炔与紫檀芪、叠氮等取代的三嗪分子连接,得到了一种含有四苯基乙烯结构的聚集诱导发光紫檀芪衍生物分子,并进一步研究了分子的毒性及细胞摄取等相关的生物活性和药理学性质.这种低毒的荧光探针分子可直观地观察到药物在细胞内外的移动和释放,为下一步靶向药物分子的设计奠定了良好的基础.
关键词: 四苯乙烯基乙炔; 紫檀芪; 聚集诱导发光; 生物活性;
Abstract: In this paper,tetrastyrylacetylene is linked to pterostilbene and azide substituted triazine by click reaction,and a kind of aggregation induced luminescent pterostilbene derivative molecule containing a tetraphenylethylene structure is obtained.In addition,the toxicity of the molecule as well as the related biological activity and pharmacological properties of cell uptake are further studied.This low toxicity fluorescent probe molecule can directly observe the movement and release of drugs in and out of cells,which lays a good foundation for the design of targeted drug molecules in the next step.
Keyword: tetrastyrylacetylene; pterostilbene; aggregation induced luminescence; biological activity;

自从人类第一次用气相沉积法制成了电致发光(EL)装置后,有机发光二极管(OLED)的研究越来越引起大家的兴趣[1,2,3,4].它的各种光学和电子特性稳定,这正好契合了高效有机材料以及制造技术的需要.在传统的发光材料中,发光物质在溶液中能发出很强的荧光,但在聚集态或固态却没有荧光发出.最近,具有聚集诱导发光(AIE)的分子引起了人们的热捧.在这其中,四苯基乙烯(TPE)(图1)是一种结构简单且具有明显的聚集诱导发光的分子[5,6,7,8].科学家们利用TPE分子去构建不同的固态发光物质和其他功能性材料,尤其在有机发光二极管和生物检测等方面[9,10].传统的发光物质在聚集状态的荧光往往是猝灭的,这就是聚集导致的荧光猝灭现象(ACQ).这种荧光猝灭现象很大程度上限制了生物样品的标记浓度,让研究者不得不采用稀溶液来做生物检测,从而降低了检测的灵敏度.而利用四苯基乙烯具有的聚集诱导发光特性,可以使高浓度的分子在聚集状态也发出很强的荧光,并用于生物检测.
图1 TPE结构图
Fig.1 The structure of TPE
本研究将TPE分子连接到紫檀芪和叠氮取代的三嗪分子上,得到了一种含有四苯基乙烯结构的聚集诱导发光紫檀芪衍生物分子,进一步研究了分子的毒性及细胞摄取等相关生物活性和药理学性质.这种优质低毒的荧光探针物质的引入,使之在作为药物载体的同时,可以更直观地观察到药物在体内的移动和释放.
1、 实验部分
1.1、 仪器和试剂
SHB-ⅢA循环水式多用真空泵、2XZ-2型旋片真空油泵、R-201旋转蒸发仪、ZF-1型紫外分析仪、XS204电子天平、HZ-9310K型恒温振荡培养箱、酶标仪(BIO-RAD680,配570nm滤光片)、倒置荧光显微镜、磁力搅拌器、离心机、烘箱及其他有机合成玻璃仪器.
1-(4-溴苯基)-1,2,2-三苯基乙烯、四三苯基膦钯、碘化亚铜、2-甲基-3-丁炔-2-醇、三乙胺、石油醚、乙酸乙酯、甲苯、氢氧化钾、2-叠氮-4-氯-6-[4-(3,5-二甲氧基苯乙烯基)苯氧基]三嗪、介孔铜氧化物、叔丁醇、水、盐酸、无水硫酸镁、四氢呋喃、HELA细胞、COS-7细胞、CHL细胞、GSE细胞、乙醇、二甲基亚砜等.
试剂均系市售商品或工业品,用前未经处理.
1.2 、四苯乙烯基乙炔的制备(图2)
称取0.822g 1-(4-溴苯基)-1,2,2-三苯基乙烯、0.15g Pd(Ph3P)4、0.025g CuI、0.242mL 2-甲基-3-丁炔-2-醇,NEt3作为溶剂,剧烈加热回流4h后,冷却至室温,过滤,将滤液转干,以石油醚和乙酸乙酯(体积比为3∶1)作为洗脱剂柱层析分离得0.692g黄色油状物1,产率为83.5%.
称取0.828g(2mmol)产物1、0.112g(2mmol)KOH,甲苯作为溶剂,加热回流3h后,冷却至室温,用10mL质量分数为10%的盐酸洗涤1次,再用100mL水洗涤2次,干燥过滤,旋干,以石油醚作为洗脱剂柱层析分离得到0.400g白色固体2,产率为56.1%.
图2 合成路线1
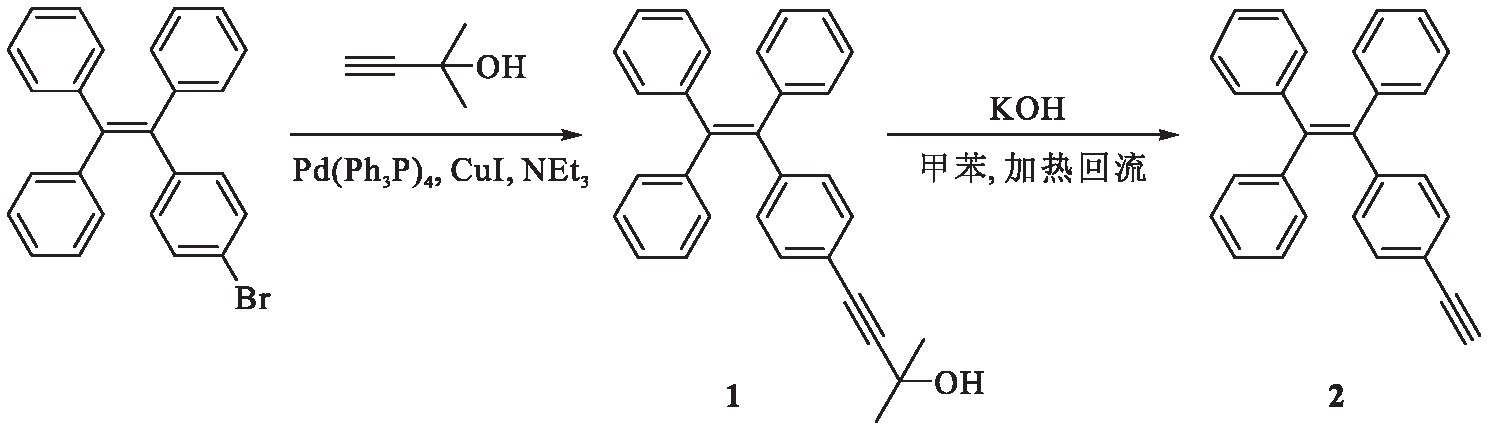
Fig.2 Synthesis route 1
1.3 2-氯-4-[4-(3,5-二甲氧基苯乙烯基)苯氧基]-6-{4-[4-(1,2,2-三苯基乙烯基)苯基]-1H-1,2,3-三唑-1-基}三嗪的制备(图3)
将0.493g(1.2mmol)2-叠氮-4-氯-6-[4-(3,5-二甲氧基苯乙烯基)苯氧基]三嗪(化合物3)、0.356g(1mmol)产物2、0.008g(0.1mmol)介孔铜氧化物、20mL叔丁醇、2mL水,搅拌溶解加热至90℃,反应10h.过滤,把叔丁醇旋干,用10mL乙酸乙酯萃取洗涤,无水硫酸镁干燥,用石油醚和乙酸乙酯(体积比为15∶1)作为洗脱剂柱层析的方法分离,得到0.430g产物4,产率为56%.
图3 合成路线2
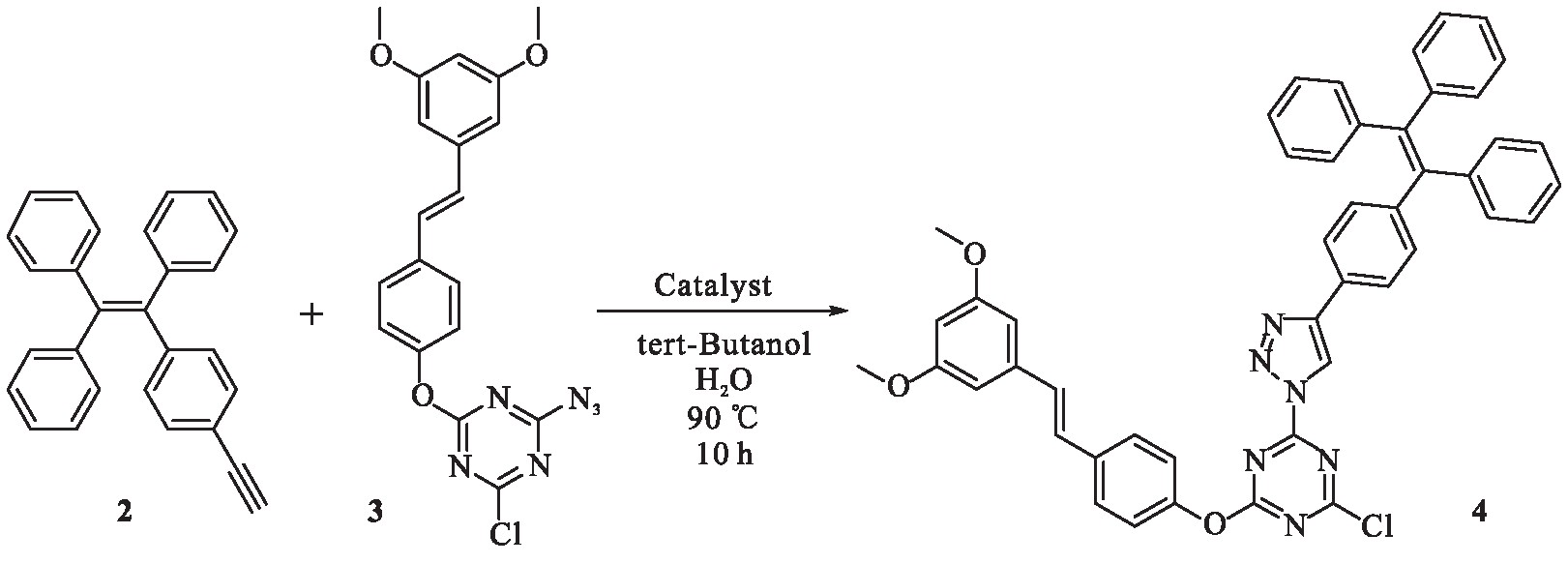
Fig.3 Synthesis route 2
1.4、 产物的表征
[2-(4-Ethynylphenyl)ethene-1,1,2-triyl]tribenzene(产物2)[11]
Mp:152~153℃.
MS(ESI):m/z (%)357.164 0[M+H]+.
IRvmax/cm-1:3 440,3 276,3 072,3 020,1 519,1 442,1 262,1 071,1 028.
1 H NMR (500MHz,CDCl3)δ7.28~6.96(m,19H),3.05(s,1H).
2-Chloro-4-[4-(3,5-dimethoxystyryl)phenoxy]-6-{4-[4-(1,2,2-triphenylvinyl)phenyl]-1H-1,2,3-triazol-1-yl}-1,3,5-triazine(产物4)[12]
Mp:165~166℃.
MS(ESI):m/z (%)767.253 8[M+H]+.
IRvmax/cm-1:3 445,3 072,3 020,2 961,2 916,2 849,2 190,1 752,1 623,1 588,1 532,1 465,1 420,1 365,1 295,1 120,1 051,1 023.
1 H NMR (500MHz,CDCl3)δ8.58(s,1H),7.68(d,J=8.3Hz,2H),7.62(d,J=8.6Hz,2H),7.26(d,J=8.6Hz,2H),7.11(dddd,J=14.1,10.0,8.7,6.6Hz,19H),6.71(d,J=2.1Hz,2H),6.45(s,1H),3.87(s,6H).
1.5 、化合物的紫外及荧光检测
图4(a)为产物2和化合物3在99%的水和100%的四氢呋喃(THF)中的荧光图谱,图4(b)为产物4在99%的水和100%的THF中的荧光图谱.如图4(a)所示,在350nm波长的激发下,产物2在THF中几乎没有荧光,而在含99%水的溶液中,具有很强的荧光,且发射波长为494nm,说明产物2具有明显的AIE现象,即聚集诱导发光效应.而在相同条件下,化合物3在THF和含99%水的溶液中都无明显的荧光现象.图4(b)中350nm波长的激发下,产物4在THF中也几乎没有荧光,而在99%水的溶液中,具有很强的荧光,其发射波长为496nm.与产物2相比,略有红移,但不是很明显.图4(c)紫外吸收光谱显示,化合物3在310nm处有吸收,产物2在321nm处有吸收,产物4在333nm处有吸收.
图4 荧光紫外谱图和紫外吸收光谱图
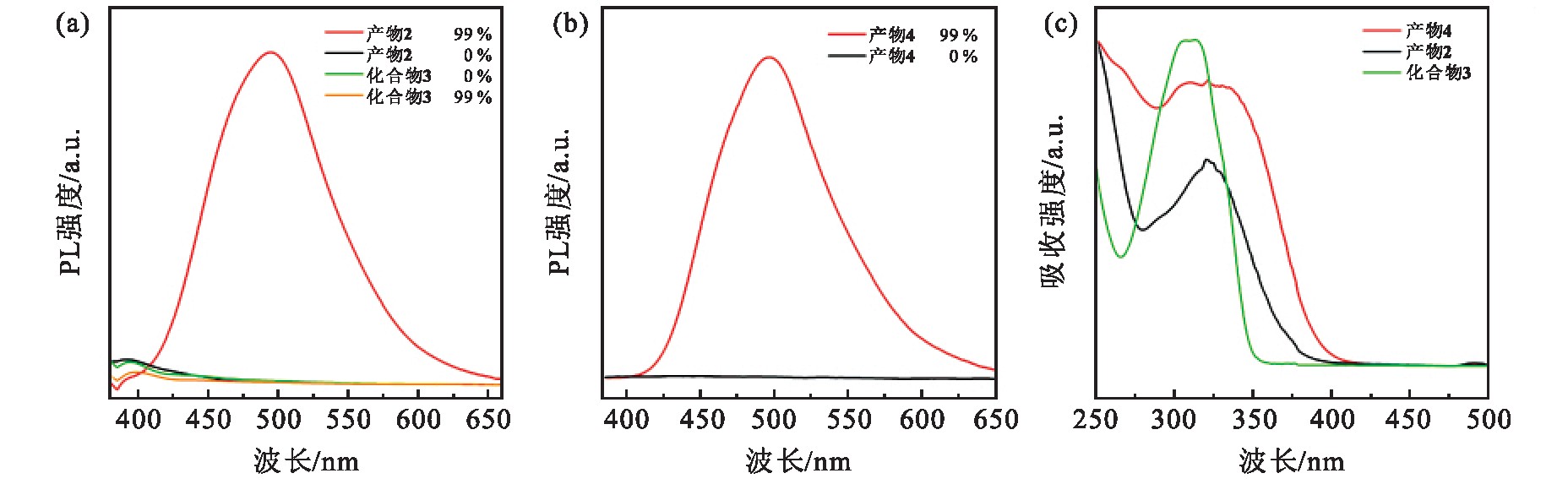
Fig.4 Fluorescent UV spectrum and UV absorption spectrum
(a)化合物3、产物2的荧光紫外谱图;(b)产物4的荧光紫外谱图;(c)化合物3、产物2、产物4的紫外吸收光谱图.
1.6、 MTT法测定产物2和产物4的细胞毒性
1)细胞接种:(1)HELA细胞用含10%小牛血清的DMEM培养液配成单个细胞悬液;(2)用0.25%胰蛋白酶消化单层COS-7细胞,用含10%小牛血清的RPMI1640培养液配成单个细胞悬液;(3)CHL细胞用含10%小牛血清的RPMI1640培养液配成单个细胞悬液;(4)GSE细胞用含10%胎牛血清的DMEM培养液配成单个细胞悬液,将细胞接种到96孔板上,每孔8 000个细胞,每孔体积200μL.
2)细胞培养:将培养板放入CO2培养箱,在37℃、5%CO2及饱和湿度条件下培养16~18h.
3)吸去培养液,用PBS清洗细胞,加入无血清培养液,在细胞板孔中分别加入产物2和产物4的DMSO溶液,使每孔中产物2和产物4的质量浓度分别为20、40、60、80、120、160、200、240μg/mL,每孔液体的总体积为200μL(每个样品每种浓度均为三复孔).
4)产物2和产物4与细胞共孵育24h.
5)吸去培养基,每孔加入90μL无血清培养液和10μL质量浓度为5mg/mL的MTT溶液,37℃孵育3h.
6)翻板法弃去液体,每孔加入100μL DMSO,在微量振荡器上振荡10min.
7)在酶标仪上测570nm波长处OD值.
8)统计细胞活力.
由图5可见,产物2对4种细胞的活性影响不大,属于低毒范围.产物4则毒性较大,在GSE和HELA细胞中当其质量浓度达到80μg/mL时,细胞毒性低于50%,而在CHL和COS-7细胞上其质量浓度达到40μg/mL时,细胞已经全部失活.分析研究发现,产物4对上皮组织细胞的毒性较大,而紫檀芪属于抗氧化的抗癌辅助天然化合物,理论上属于低毒化合物,所以可能是由于该化合物中含有活泼的氯原子,对上皮组织中的某种酶有影响,故毒性较大.
图5 产物2和产物4对4种不同细胞在不同浓度下的细胞毒性
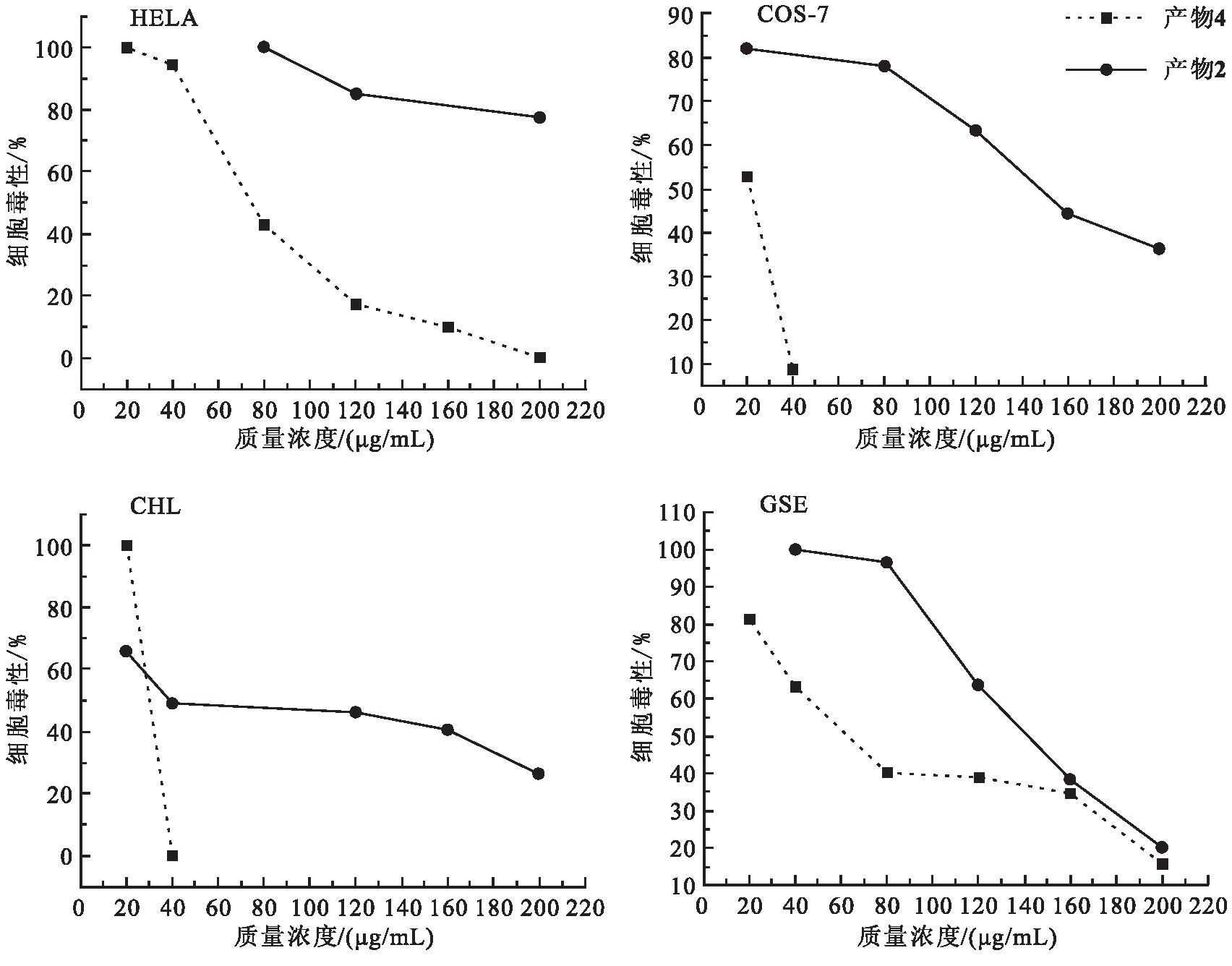
Fig.5 Cytotoxicity of product 2and product 4to four different cells at different concentrations
1.7 、产物2和产物4的细胞摄取实验
1)细胞接种.
将普通洁净盖玻片放入70%乙醇中浸泡5min,于超净台内吹干.将盖玻片置于24孔板内,种入细胞培养过夜,使细胞密度为70%~80%.将圆形载玻片放入24孔板的每个孔中.
神经胶质瘤细胞用含10%小牛血清的DMEM培养液配成细胞悬液,将细胞接种到24孔板上,每孔2×104个细胞,每孔体积500μL.于CO2培养箱中培养24h,待细胞密度为70%~80%时进行摄取实验.
2)产物2和产物4的溶液分别用DMSO配制成20μg/mL的溶液.
3)细胞摄取实验.
孵育24h后,将24孔板中的培养液吸去,加入400μL无血清的DMEM培养液,将配好的两种溶液分别加入24孔板中,在37℃、5%CO2培养箱中培养2.5h后取出,重复前一步骤,再吸去两个孔板中的培养液,加入400μL无血清的DMEM培养液,将配好的两种溶液分别加入24孔板中,在37℃、5%CO2培养箱中培养0.5h.
吸去培养液,用PBS洗涤3次,每次200μL,吸去PBS,每孔加入200μL 0.5μg/mL的Hoechst溶液,孵育6min后,吸去Hoechst溶液,用PBS洗涤3次.
4)倒置荧光显微镜观察.
由图6可发现,产物4在细胞吞噬3h后荧光负载的药物比0.5h的要多,且与产物2比较发现,无论是3h还是0.5h,产物4的细胞吞噬效果都要比产物2好.分析其原因,可能是由于分子量的增大使得细胞更易吞噬且不易流出,所以分子量大的产物4更易被细胞吞噬.这一结果使笔者将荧光与药物相结合的设想成为可能,可以更直观地看出药物被细胞吞噬的形态、数量及分布状况[13].
图6 细胞摄取图像
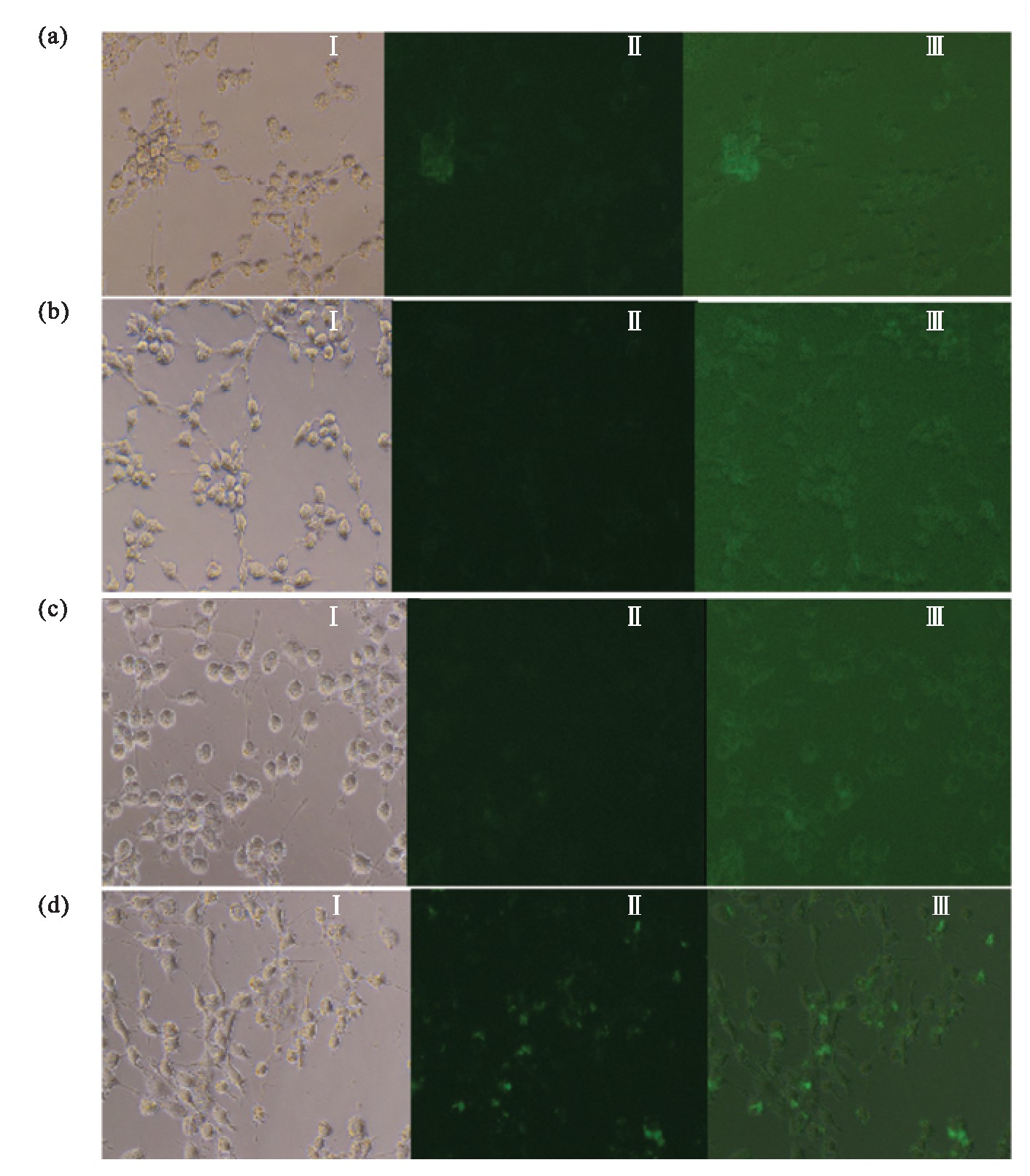
Fig.6 Cell uptake image
(a)0.5h产物2;(b)0.5h产物4;(c)3h产物2;(d)3h产物4.Ⅰ为白光条件下细胞,Ⅱ为蓝光条件下细胞,Ⅲ为两图合并的效果图.
2、结果与讨论
本研究把具有AIE聚集诱导发光效应的四苯乙烯基引入到三氯三嗪分子中,同时连载上具有抗氧化性的辅助抗肿瘤分子紫檀芪,通过荧光测定,确定分子在水中仍具有聚集诱导发光的特性.MTT检测发现,产物2在不同细胞中毒性较小,但随着浓度的增加毒性有所加强,在相同条件下,产物4由于分子中有氯元素的存在,毒性更大.细胞摄取实验发现在一定时间内,吞噬时间越长,细胞摄取效果越好,产物4因含有抗氧化性的紫檀芪且分子量较大,所以细胞摄取情况优于产物2.
这一系列的检测说明,我们可以利用产物4荧光显色的特性,研究其被细胞吞噬后药物的分布、数量及形态等,使得对三嗪化合物产物4的研究不再停留在最基础的化学合成阶段,对它的药理性能也有了更多的认识,为下一步靶向药物分子设计奠定了良好基础.
参考文献
[1]LIM M S,NAM M,CHOI S,et al.Two-dimensionally stretchable organic light-emitting diode with elastic pillar arrays for stress relief[J].Nano Letters,2020,20(3):1526-1535.
[2]HWANG J,LEE C,JEONG J E,et al.Rational design of carbazole-and carboline-based polymeric host materials for realizing highefficiency solution-processed thermally activated delayed fluorescence organic light-emitting diode[J].ACS Applied Materials&Interfaces,2020,12(7):8485-8494.
[3]TONNELC,STROET M,CARON B,et al.Elucidating the spatial arrangement of emitter molecules in organic light-emitting diode films[J].Angewandte Chemie International Edition,2017,56(29):8402-8406.
[4]KABE R,NOTSUKA N,YOSHIDA K,et al.Afterglow organic light-emitting diode[J].Advanced Materials,2016,28(4):655-660.
[5]LIU H Q,WANG Y,MO W Q,et al.Dendrimer-based,high-luminescence conjugated microporous polymer films for highly sensitive and selective volatile organic compound sensor arrays[J].Advanced Functional Materials,2020,30(13):1910275.
[6]YIN G Q,WANG H,WANG X Q,et al.Self-assembly of emissive supramolecular rosettes with increasing complexity using multitopic terpyridine ligands[J].Nature Communications,2018,9(1):567.
[7]HUANG J S,YU Y L,WANG L,et al.Tetraphenylethylene-induced cross-linked vesicles with tunable luminescence and controllable stability[J].ACS Applied Materials&Interfaces,2017,9(34):29030-29037.
[8]XIONG J B,FENG H T,SUN J P,et al.The fixed propeller-like conformation of tetraphenylethylene that reveals aggregation-induced emission effect,chiral recognition,and enhanced chiroptical property[J].Journal of the American Chemical Society,2016,138(36):11469-11472.
[9]ZHANG C Q,LIU C,XUE X D,et al.Salt-responsive self-assembly of luminescent hydrogel with intrinsic gelation-enhanced emission[J].ACS Applied Materials&Interfaces,2014,6(2):757-762.
[10]LIU J L,ZHUO Y,CHAI Y Q,et al.BSA stabilized tetraphenylethylene nanocrystals as aggregation-induced enhanced electrochemiluminescence emitters for ultrasensitive microRNA assay[J].Chemical Communications,2019,55(67):9959-9962.
[11]KANG Q,XIAO Y,HU W P,et al.Smartly designed AIE triazoliums as unique targeting fluorescence tags for sulfonic biomacromolecule recognition via ‘electrostatic locking’[J].Journal of Materials Chemistry C:Materials for Optical and Electronic Devices,2018,6(46):12529-12536.
[12]徐伟明,章鹏飞,李万梅,等.一种白藜芦醇系列荧光标记分子及其合成方法:CN106967049[P].2017-06-21.
[13] XU W M,ZHANG P F,LI W M,et al.Series of resveratrol-derivative fluorescently labeled molecules and synthesis method thereof:US10125119B2[P].2018-11-13.