
小反刍兽疫(Peste des petits Ruminants,PPR)又称羊瘟、小反刍兽瘟,是由副黏病毒科、麻疹病毒属的小反刍兽疫病毒(PPR virus,PPRV)所引起的一种急性接触型传染性疾病,主要感染小反刍兽,特别是山羊和绵羊,其发病率可达100%,严重暴发期病死率为100%,野生动物偶尔感染,目前未见有人感染该病的报道。鉴于PPR的危害,国际兽疫局(Office International Des Epizooties,OIE)将其列为必须报告的A类动物疫病,我国将其列为一类动物疫病,是《国家动物疫病中长期防治规划(2012-2020年)》明确规定重点防范的外来动物疫病之一。
小反刍兽于1942年首次在非洲的科特迪瓦发生〔1〕,1970年至1972年间,PPR在东非国家苏丹发生,1983年传至阿拉伯半岛,1987年传至印度南部,PPR主要流行于非洲、阿拉伯半岛、中东、中亚和南亚的大部分国家〔2〕,在我国西部边境省份形成包围态势。近年来,我国周边一些国家频频发生PPR.2007年,我国首次在西藏地区暴发PPR疫情〔3〕。随后,在新疆、甘肃、内蒙古等多省区出现疑似PPR症状,2013年底~2014年在我国多数省、区发生PPR.
1小反刍兽疫的病原
1.1小反刍兽疫病毒及分型
小反刍兽疫病毒(PPR virus,PPRV)隶属于副黏病毒科 (Paramyxoviridae)、副 黏病毒亚科 (Pa-ramyxovirinae)、麻疹病毒属(Morbolivirus),同属的其它成员有:人麻疹病毒(Measles virus,MV)、牛瘟病毒 (Rinder pest virus,RPV)、犬瘟热病毒(Canine distemper virus,CDV)、海豹瘟病毒(Por-poise distemper virus,PDV)、海豚瘟病毒(Dolphindistemper virus,DDV;或Dolphin Morbilli Vires,DMV)等。PPRV与麻疹病毒同属的其它病毒具有相似的物理化学及免疫学特性,但抗原性不同,在琼脂扩散试验和补体结合试验中会表现部分交叉保护和交叉反应现象,但可以通过血清中和试验进行鉴别。
目前,PPRV仅有1个血清型。根据PPRV部分基因序列,将其分为4个系,其中Ⅰ、Ⅱ、Ⅲ系源于非洲(Ⅰ系-西非、Ⅱ系-北部非洲、Ⅲ系-东非),Ⅳ系源于亚洲(Ⅳ系-中东和西亚)。Ⅳ系分布最广,分布于南亚、中东和北部非洲,Ⅲ系分布于中东和东非,Ⅰ和Ⅱ系仅见于非洲〔4〕。在我国西藏地区发生的PPR属于Ⅳ系,所以推测是从印度传入我国的。
1.2小反刍兽疫病毒的形态结构特征
PPRV病毒粒子呈多形性,多呈圆形或椭圆形,直径约为130~390nm;病毒颗粒的外层有8.5~14.5nm厚的脂质囊膜,囊膜上有8~15nm长的纤突,病毒的纤突中只有血凝素(Hemagglutinin,H)蛋白,无神经氨酸酶(Nueraminidase,N),但却同时具有神经氨酸酶和血凝素活性;病毒核衣壳为螺旋中空杆状并有特征性的亚单位,其衣壳总长约为1 000nm,呈 螺 旋 对 称,直 径 约18nm,螺 距5~6nm,并且核衣壳缠绕成团。
1.3小反刍兽疫病毒的理化特征
小反刍兽疫病毒(PPRV)具有囊膜,在自然环境下抵抗力较弱,37 ℃条件下,PPRV感染力的半衰期为1~3h,56 ℃的半衰期仅为2.2min,70 ℃以上迅速灭活。在冷藏和冷冻组织中能存活较长时间。病毒粒子在pH 5.8~9.5之间稳定,pH高于9.6或低于5.6,病毒迅速灭活;PPRV对热、紫外线、干燥环境等非常敏感,因此不能在常态环境中长时间存活。
对化学试剂敏感,如酒精、乙醚、甘油和一些去垢剂。乙醚12h可将其灭活,酚类、2%的NaOH等作用24h可以灭活该病毒,使用非离子去垢剂可使病毒的纤突脱落,降低感染力。
1.4小反刍兽疫病毒的基因组及蛋白特征
PPRV为单股负链无节段RNA病毒,其基因组长15 948bp,是麻疹病毒属中已知基因组最长的,从RNA的3‘端至5’端依次为N-P/C/V-M-F-H-L共6个基因,分别编码核衣壳蛋白(Nucleocap-sid,N)、磷蛋白(Phosphoprotein,P)、囊膜基质蛋白(Capsule membrane matrix protein,M)、纤突糖蛋白(The spike glycoprotein,F)、血凝素(Hemagglu-tinin,H)和大蛋白(Large protein,L)6种结构蛋白,其中N蛋白、P蛋白和L蛋白构成病毒的核衣壳;此外,P基因还编码C和V2种非结构蛋白;各基因间有一定的基因间序列相间隔。除H和L基因间的密码子为CGT外,其它基因间都被密码子CTT相互分开;除F基因是以AGGG开始以外,其他均AGGA序列开始,并以至少4个A碱基扩展序列结束,见图1.
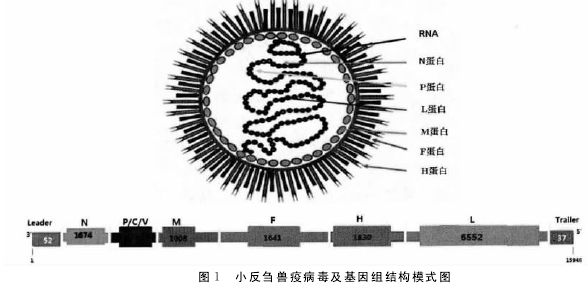
2小反刍兽疫的流行病学
2.1小反刍兽疫的地理分布
1942年,PPR首次 在科特迪瓦(原 称象牙 海岸)发 现后,一些非洲国家,如 尼日 利 亚、塞 内 加尔、加纳等也相继发生PPR.1979年以前,只是在科特迪 瓦 临 近 的 一 些 国 家 局 限 性 发 生,期 间 在1962年,疫情跨过了利比里亚、几内亚等多个国家,长 距 离 蔓 延 至 塞 内 加 尔。此 后,PPR不 断 向东、南和北三个方向蔓延。1984年PPR扩散至苏丹,随后又蔓延至东非的肯尼亚、埃塞俄比亚和乌干 达。1987年,PPR扩 散 至 印 度 北 部 地 区。在1993~1995年期间,疫情蔓延至阿拉伯半岛、中东以及印度其他地区,包括伊朗、伊拉克、以色列、约旦、科威特、黎巴嫩、阿曼、沙特、阿联酋、也门、叙利亚等国家。1999年,小反刍兽疫蔓延到土耳其。2003年以来,我国周边的老挝、印度、尼泊尔、俄罗斯、巴基斯坦和缅甸等国暴发了大规模PPR疫情。2007年PPR疫情扩散至中国的西藏,2008年扩散撒哈拉沙漠以北的摩洛哥、突尼斯以及赤道以南的坦桑尼亚,2010年继续向南扩散至赞比亚,向东扩散至不丹;2011年继续向北扩散至阿尔及利亚。
至今,小反刍兽疫向北已跨过撒哈拉沙漠扩散至北非,向南已越过赤道扩散至赞比亚、安哥拉,向东早已越过非洲扩散至阿拉伯半岛、南亚、西亚、中亚以及土耳其和中国。
2013年以来,全球共有26个非洲国家、16个亚洲国家以及地处欧亚交界的土耳其等43个国家报告发生小反刍兽。2013年9月,塔吉克斯坦向OIE报告发生PPR疫情。2014年,全球除美国、阿根廷等48个国家无PPR疫情外,非洲、亚洲和南美一些国家存在有PPR疫情,见图2.
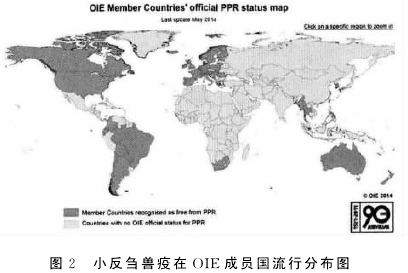
2007年7月26日,我国首次报道在西藏日土县热帮乡龙门卡村发生PPR疫情〔3〕。2008西藏阿里地区革吉县文布当桑乡罗玛村发生野生岩羊小反刍兽疫疫情,未见家畜发病〔5〕。同年6月,西藏那曲地区尼玛县双湖区嘎措乡发生PPR疫情;2010年5月,西藏阿里地区日土县多玛乡乌江村斯亚点发生PPR疫情〔6〕。
2013年11月,新疆伊犁哈萨克自治州霍城县三官乡一村羊发生疑似小反刍兽疫,新疆自治区动物疫病预防控制中心诊断为疑似小反刍兽疫疫情,经国家外来动物疫病研究中心确诊为小反刍兽疫疫情,这是我国新疆首次报道发生小反刍兽疫疫情。12月新疆再次发生小反刍兽疫疫情,哈密地区哈密市五堡镇、阿克苏地区库车县哈尼喀塔木乡和柯坪 县玉尔其乡玉拉拉村和上 库 木 力村,巴州轮台县策达雅乡萨依巴格村分别发生羊的小反刍兽疫。
2014年1月甘肃省武威市古浪县黄花滩乡、2月内蒙古自治区巴彦淖尔市乌拉特后旗乌盖苏木和丰村,以及相邻的抗棉后旗团结镇建设村,3月贵州省沿河县甘溪乡任家宅村〔7〕、江西修水县〔8〕、黑龙江省某县〔9〕分别发生羊的小反刍兽疫。
2.2小反刍兽疫的疫情特点
从小反刍兽疫的来源、易感动物、感染途径、发病症状和流行情况等方面看,小反刍兽疫及其疫情具有以下一些特点:
2.2.1小反刍兽疫感染动物的宿主局限性:小反刍兽疫主要感染山羊、绵羊等小反刍动物,山羊比绵羊更易感,临床症状更严重,3~8月龄的山羊最易感,哺乳期的动物抵抗力较强,岩羊、野山羊、盘羊、瞪羚、鹿、羚羊等野生小反刍动物也易感,对牛等大反刍动物可感染但不发病,目前尚无人感染的报道。
2.2.2小反刍兽疫传播及流行性:PPRV存在于感染动物的眼鼻分泌物、唾液、咳嗽释放的飞沫、尿液、粪便甚至在乳汁中,污染区域内的水源、料槽、垫料等都会被感染动物的分泌物污染从而成为传染源,疾病后期粪便中含毒量较高,但不会长时间保持传染性。感染的山羊、绵羊等小反刍动物在感染后的潜伏期间及发病期间传播本病,但感染羊恢复后不会成为慢性带病原者;小反刍兽疫主要通过呼吸道和消化道感染,其传播方式可通过病畜与健康畜的直接和间接接触而传染。呼吸系统是主要的感染途径,大多为呼吸道飞沫传染。因此,小反刍兽疫疫情的传播扩散,主要取决于动物移动,特别是动物及其产品的调运。目前,全球和我国的小反刍兽疫疫情的迅速发生也就充分证明了这一点。
2.2.3小反刍兽疫疫情发生的阶段性和疫情类型:根据小反刍兽疫疫情发生过程及疫情发生的特点,小反刍兽疫疫情表现出:(1)疫情的输入:因动物的移动以及跨区域调运,从疫区等传入非疫区,由于调入动物在早期不发病,或都处于潜伏期,动物不表现任何临床症状,使调入动物成为引发疫情的隐患,这种疫情称隐蔽性疫情。将染有小反刍兽疫的动物引入当地,因此将这种没有与本地羊接触,单纯在调入羊中发生的疫情称之为输入性疫情。(2)疫情发生与扩散:调入的感染动物经过潜伏期后,一些羊出现临床症状,发生小反刍兽疫疫情。因从疫区调运的感染动物未进行隔离观察,直接与本地羊混群饲养,或者把调入羊转卖给别的养殖场户,或者与其它养殖户羊放牧接触,或者经人员往来传播到其它养殖场户造成疫情扩散蔓延,这类疫情称为扩散性疫情。羊感染小反刍兽疫主要表现口炎、眼有黏性分泌物、胃肠炎(腹泻)、肺炎(支气管肺炎或称小叶肺炎)等典型临床症状,且发病率、死亡率都比较高。
3小反刍兽疫的诊断
3.1临床诊断
3.1.1羊感染后的临床症状:该病临床症状和牛瘟相似,但只有山羊和绵羊感染后才出现症状,感染牛则不出现临床症状。小反刍兽疫的临床症状可总结为:D-D-B-D,即眼鼻黏分泌物(Discharges)、腹泻 (Diarrhoea)、支 气 管 肺 炎 (Bronchopneumo-nia),以及高死亡率(Death)。病羊主要表现出眼鼻分泌物增多、流涎、嘴唇肿胀,口腔黏膜表面糜烂,后出现坏死及溃疡,并有干酪样分泌物;呼吸失调、咳嗽,后期伴有支气管肺炎;水样腹泻后期带血、严重脱水,消瘦。幼年动物发病率和死亡率都很高,发病 率 可 达100%,死 亡 率 可 达100%,一 般 超过50%.
3.1.2病理变化:尸体剖解病变与牛瘟相似,患羊出现结膜炎、坏死性口炎等肉眼病变,口腔和鼻腔黏膜糜烂坏死;支气管肺炎,肺尖肺炎。在鼻甲、喉、气管等处有出血斑,严重病例可蔓延到硬腭及咽喉部。皱胃常出现病变,病变部常出现有规则、有轮廓的糜烂,创面红色、出血。而瘤胃、网胃、瓣胃很少出现病变,肠可见糜烂或出血,大肠内和盲肠、结肠结合处出现特征性线状出血或斑马样条纹。
3.2实验室诊断
3.2.1病原学检测:病毒的分离鉴定和病毒中和实验(VN)具有特异性好的优点,并且VN可以鉴别PPRV和RPV以及PPRV的不同毒株之间的差异,但两者都因试验操作比较复杂,耗时较长,且很难实现大规模样品的监测,在实际应用中受到了极大的限制。相对而言,进行PPRV抗原检测,如捕获酶联免疫吸附试验(icELISA)、琼脂凝胶免疫扩散(AGID)和对流免疫电泳(CIEP),方法简单、经济,对实验室条件要求低,甚至可在野外完成检测,但是灵敏度较低。
3.2.2分子生物学检测:目前,对PPRV核酸进行检测的方法主要采用特异性的cDNA探针和反转录PCR(RT-PCR)两种方法。
3.2.3血清免疫学诊断:常用的抗体检测方法是酶联 免 疫 吸 附 法 (ELISA),OIE推 荐 用 于 检 测PPRV抗体的方法是一种用抗PPRVH蛋白单克隆抗体作为特异性的竞争单抗建立的竞争ELISA(cH-ELISA),后来一些研究者应用杆状病毒表达系统表达的N蛋白和抗N蛋白特异性单克隆抗体建立的cH-ELISA方法进行检测。
4小反刍兽疫的防控
目前,对PPR尚无有效的治疗方法,发病初期使用抗生素和磺胺类药物等支持性疗法可以降低死亡 率,还 能 有 效 预 防 继 发 性 感 染 的 发 生。当PPRV首次出现时,需进行快速确诊。一旦确诊,立即采取严格的封锁、扑杀、隔离检疫、消毒以及疫苗接种等措施。
4.1小反刍兽疫疫情处置措施
一旦发生本病,应按《中华人民共和国动物防疫法》规定,按一类动物疫情处置方式扑灭疫情,以“早、快、严”的原则,坚决扑杀、彻底消毒,严格封锁、防止扩散。一旦确诊,立即进行疫点、疫区和受威胁区的划定,实施封锁,全面禁止活畜和产品交易,禁止牲畜过牧、交换。对疫点内的所有山羊和绵羊实施扑杀,并对所有病死羊、被扑杀羊及羊鲜乳、羊肉等产品按国家规定标准进行无害化处理;疫点进行彻底的消毒处理。对受威胁区羊群进行免疫,建立免疫隔离带。
4.2小反刍兽疫的常规防控
4.2.1加强对小反刍兽疫的检疫和日常饲养管理和消毒工作:加强PPR疫情监控工作,严格实施兽医卫生检疫,是防止小反刍兽疫发生及传播扩散的重要措施。小反刍兽疫的兽医卫生检疫包括产地检疫、屠宰检疫、运输检疫和边境检疫。通过严格的兽医卫生检疫,达到羊等易感动物的监测排查,及时发现和消除隐患。同时,做好日常饲养管理和消毒工作,切实提高生产安全水平。
4.2.2对PPR呈地方性流行的区域,最常用的防控方法是疫苗接种。目前,世界上预防该病仍以传统的弱毒疫苗为主,但一些针对PPR的各种新型疫苗已陆续进行研制。经典的PPR弱毒疫苗是1989年Diallo等学者通过在vero细胞上的连续传代,将Nigeria/75/1株致弱,成功地研制出第1株PPR的同源性弱毒 苗。通 过 对 山 羊 和 绵 羊 的 试验,证明了Nigeria/75/1株能有效预防PPRV强毒的感染,对羊没有副作用,并且保护性抗体可持续3年以上。此后,世界其他国家的研究人员也研制出了类似的弱毒疫苗。虽然PPRV Nigeria75/1属于PPRVⅠ系,但对PPRV的其他3个系的强毒同样具有较高的保护率。至今,弱毒疫苗Nigeria75/1仍是OIE规定的唯一允许使用的PPRV疫苗。
自2007年7月首次在西藏地区发生小反刍兽疫疫情后,我国生产的用于西藏和新疆部分地区进行紧急免疫的小反刍 兽疫 弱 毒 活 疫 苗 为Nigeri-a75/1株。无疑PPR弱毒疫苗能交叉保护各个群毒株的攻击感染,很好地预防PPR的发生,但弱毒疫苗热稳定性差,且最大的缺点是无法从血清学上区别疫苗株和野毒株的感染,这就造成了无法在接 种 疫 苗 地 区 进 行 血 清 学 调 查。此 外,由 于PPR和牛瘟(RP)在血清学上有交叉反应,这也影响了同时流行这两种疾病地区的RP血清学调查。
现在已 经 有 许 多 新 型PPR疫 苗 研 究 的 报 道,如PPR重组亚单位疫苗、表达PPRV F和H基因的山羊痘病毒活载体疫苗、嵌合病毒疫苗、PPR核酸疫苗等,但这些疫苗还需进一步研究,在生产中得到应用仍需要一些时间。
参考文献
〔1〕Gargadennec L,Lalanne A.La peste des petits rumi-nants.Bulletin des Services Zoo Techniques et desEpizooties de I Afrique occidentale Francaise〔J〕。1942(5):16~21.
〔2〕Banyard A C,Parida S,Batten C,et al.Global distribu-tion of peste des petits ruminants virus and prospects forimproved diagnosis and control〔J〕。J Gen Virol,2010,91:2885~2897.
〔3〕王志亮,包静月,吴晓东,等。我国首例小反刍兽疫诊断报告〔J〕。中国动物检疫,2007,24(8):24~26.
〔4〕Dhar P,B P Sreenivasa,T Barrett,et al.Recent epidemi-ology of peste des petits ruminants virus(PPRV)〔J〕。VetMicrobiol,2002,88:153~159.
〔5〕Bao J,Z Wang,L Li,et al.Detection and genetic charac-terization of peste des petits ruminants virus in freelivingbharals(Pseudois nayaur)in Tibet,China〔J〕。Res VetSci,2011,90:238~240.
〔6〕王乐元,次真,吴国珍,等。中国西藏小反刍兽疫的发生状况与防控〔J〕。畜牧兽医学报,2011,42:717~720.
〔7〕李忠全,杨秀强,崔玉林,等。山羊小反刍兽疫疫情调查诊断报告〔J〕。湖北畜牧兽医,2014,35(4):21~22.
猪地方流行性肺炎是猪呼吸道疾病中较常见、难治愈的的一种疾病,该病在各种类型养猪场普通存在,尤其是畜舍环境差、管理不到位的猪场最易发生,该病致死率不高,但感染率很高,猪场一旦发病,很难彻底消除病原,治疗上也会有一定的困难,给养殖场户造成的损...
1流行病学本病传染途径主要经消化道传染,感染犬是本病的主要传染源。自然条件下,对本病易感的动物主要是犬,3~4周龄犬感染后呈急性致死性心肌炎的为多。此外,无临床症状的带毒犬,也是危险的传染源。感染犬出现症状后一般第45天左右粪便排毒量最高,...
目前, 牛病毒性腹泻病呈全球性分布, 多数养牛国家均存在该病的发生与流行, 临床中多数以亚临床症状为主, 即主要表现为牛群生长缓慢, 其生产力和经济活力降低, 最终导致免疫抑制和隐性感染, 给该病的防控和净化增加了很大困难。...
酵母培养物(YC)是一种由酵母菌在特定的培养基上和特定工艺条件下,经过充分的厌氧发酵后形成的微生态制品,酵母培养物主要由少量已无活性的酵母细胞、变异的培养基及代谢产物所构成。代谢产物主要包括肽、有机酸、寡糖、氨基酸、核苷酸、增味物质和芳香...
1流行病学一般饲养环境下的猪群普遍存在肠道病毒,虽然病毒普遍存在,但通常无明显临床表现或仅呈少数散发状态,很少出现群体性暴发.猪是猪肠道病毒的唯一宿主.在普通猪群中可以同时流行几个血清型的肠道病毒.传播途径主要是通过粪-口途径,其次是气溶胶和飞...
非洲猪瘟缘起非洲, 据资料显示, 20世纪初, 东部非洲的肯尼亚首次确认非洲猪瘟疫情, 此后, 陆续蔓延至欧美。近年来, 疫情更是向亚洲侵袭, 毫不讳言, 对于非洲猪瘟, 人类若控制不力, 疫情还有向周边国家乃至全球扩张的趋势。...