
阴沟肠杆菌是存在于人和动物肠道的正常菌群,近年来已成为医院感染的重要致病菌之一。由于头孢菌素和喹诺酮等广谱抗菌药在临床上广泛使用,使阴沟肠杆菌在其选择性压力下不断发展耐药机制,造成日益严重的耐药问题,近几年情况尤其严重,对阴沟肠杆菌产超广谱β内酰胺酶(ESBLs)和高产AmpC酶的报道甚至超过60%[1].鉴于此,本研究选取2014年1~12月本院新生儿分离到的46例阴沟肠杆菌进行临床分布和耐药性检测,以了解本院阴沟肠杆菌产酶情况,从而指导临床合理用药。现将研究结果报道如下。
1资料与方法
1.1菌株来源选取2014年1~12月本院新生儿病房送检的血、尿、便、痰、咽拭子、脑脊液及脐带分泌物合格标本1 152例,其中分离出阴沟肠杆菌46例,除常规技术操作外,所有菌株鉴定及其药敏鉴定均采用VITEK2-compact系统鉴定(法国梅里埃公司),选用的GN细菌鉴定卡和GN-09药敏鉴定卡。
1.2结果判定耐药性结果判定及试验的质量控制采用美国药敏试验结果按美国临床和实验室标准协会(CLSI)2013年版判断标准对照质控菌株判断敏感、中介、耐药。
1.3 ESBLs检测纸片琼脂扩散法:药敏平板和菌液的制备方法与常规药敏试验相同,将菌液涂布于MH琼脂平板上,贴上药敏纸片5张,分别是亚胺培南、头孢噻肟/克拉维酸、头孢噻肟、头孢吡肟、头孢他啶/克拉维酸。
35 ℃孵育18~24h,按CLSI标准判断结果,头孢噻肟/克拉维酸、头孢噻肟的直径差不低于5mm,判断为ESBLs阳性[2].并用大肠埃希菌ATCC25922作为质控菌株,药敏纸片为英国OXID公司产品,MH琼脂购自北京天坛药物生物技术开发公司。
1.4 AmpC酶的检测采用纸片扩散法,用头孢西丁纸片检测受试菌株,根据CLSI标准,抑菌圈直径不超过17mm,提示耐药或中介者疑产AmpC酶[1].
1.5统计学处理采用WHONET5.6软件进行分析,百分率之间的比较采用χ2检验,P<0.05为差异有统计学意义。
2结果
2.1阴沟肠杆菌分布本院新生儿送检的血、尿、便、痰、咽拭子、脑脊液及脐带分泌物合格标本1 152例中分离出阴沟肠杆菌46例,阳 性 率 为3.99%(46/1 152),其 中,痰30例,占65.22%;咽拭子15例,占28.85%;尿1例,占2.17%.
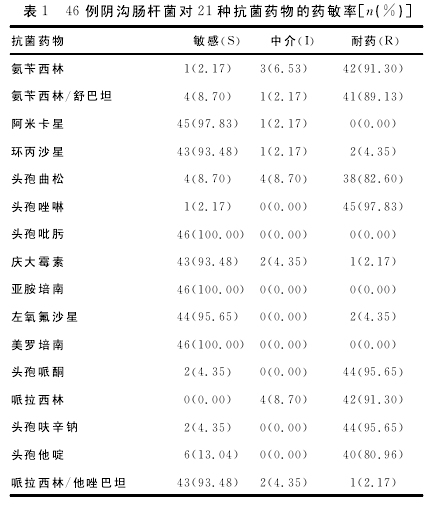
2.2耐药率情况46例阴沟肠杆菌对21种常见抗菌药物的耐情况,见表1.
2.3阴沟肠杆菌耐药机制情况46例中有13例单产ES-BLs,占28.26%;11例单产AmpC酶,占23.91%;6例既产ESBLs又 产AmpC酶,占13.04%;其 余16例 非 产 酶,占34.78%.
3讨论
阴沟肠杆菌是引起呼吸道和泌尿生殖道感染的常见条件致病菌,普遍存在于水、污水、土壤和蔬菜中,也寄居在人的皮肤、呼吸道和泌尿道等部位,可引起呼吸道、泌尿道、伤口感染及败血症等[2].随着第3、4代头孢菌素的广泛应用,这类细菌的耐药问题越来越受到人们的关注,成为院内感染不容忽视的条件致病菌,新生儿因其胎龄小,免疫力低,免疫机能不完善,在各种人为侵入性操作和护理不当的情况下,很容易感染阴沟肠杆菌,一旦感染,便成为临床医师棘手的问题。因此,监测 新生儿阴沟肠杆 菌 院 内 感 染 情 况 是 非 常 必要的。
本院2014年1~12月共收治1 152例新生儿患儿,其中感染阴沟肠杆菌46例,占3.99%.虽然在医院感染中所占比例小,但是由于阴沟肠杆菌属一类易产诱导酶的细菌,一旦爆发,其后果极其严重。阴沟肠杆菌通常情况下,只产生低水平AmpC酶,而三、四代头孢菌素和喹诺酮类药物是弱的诱导剂,不会直接导致细菌耐药[1].但是,当大量使用三、四代头孢菌素或喹诺酮类药物治疗这种细菌引发的感染时,该菌通过染色体自发突变持续高产AmpC酶和ESBLs酶,从而对多种β内酰胺类抗菌药物耐药,并迅速传播[3-5].本研究显示,阴沟肠杆菌对青霉素及第1、2、3代头孢的耐药性很强,与国内其他相关报道相近[2-4].值得注意的是,本研究在对此46株例菌进行ESBLs酶和AmpC酶检测后发现,分别产ESBLs、AmpC酶和产两种酶的阴沟肠杆菌菌株占65.21%,其中产两种酶的有6株例,占13.04%,这比与2006年及2011年的相关报道比较的有所增多[2-4],可见阴沟肠杆菌产诱导酶菌株,在逐年增加。另外,研究结果显示,哌拉西林/他唑巴坦的抗菌活性很好,优于氨苄西林/舒巴坦,这可能是因为哌拉西林本身对革兰阴性杆菌的抗菌活性强于氨苄西林所致,并且他唑巴坦与哌拉西林的协同作用优于氨苄西林/舒巴坦[6],因此哌拉西林/他唑巴坦稳定性优于氨苄西林/舒巴坦,同时,没有发现碳青霉烯类耐药菌株,这是因为碳青霉烯类的高抗菌活性和低耐药突变选择能力[7].研究还发现本院分离的阴沟肠杆菌对喹诺酮类药物还是很敏感的,这可能是因为喹诺酮类药物的不良反应限制了本院感染 患 儿 的 使 用,因 此 阴 沟 肠 杆 菌 没 有 被 诱 导 出 高 产AmpC酶。
总之,在治疗阴沟肠杆菌感染时,抗菌药物的选择应同时兼顾抗菌活性和对耐药突变的选择能力,以防止产ESBLs酶和高产AmpC酶突变株的产生和进一步蔓延。同时在针对新生儿这一特殊群体时,在没有药敏情况下的,建议临床医师可以暂时选择碳青霉烯类和哌拉西林/他唑巴坦治疗,待药敏结果出示后调整用药方案。
参考文献
[1] 许小敏,陈琳,赵伟和,等。阴沟肠杆菌耐药性的检测与分析[J].中华医院感染学杂志,2006,16(3):343-344.
[2] 刘石,郑国方。阴沟肠杆菌致新生儿感染17例分析[J].右江民族医学院学报,2007,17(2):183-185.
[3] 张永标,唐英春,张扣兴。阴沟肠杆菌感染的临床分布与耐药性[J].中华医院感染学杂志,2006,16(10):1174-1177.
[4] 聂川,张永,罗先琼,等。新生儿病房阴沟肠杆菌感染及药敏结果分析[J].临床儿科杂志,2011,29(9):825-828.
[5]National Committee for Clinical Laboratory Standards.M1002S11Perfermance standards for antimicrobial sus-ceptibility testing[S].Eleventh informational supple-ment.Pennsylvania:NCCLS,2001.
[6] 佘丹阳,刘又宁。β-内酰胺类抗菌药物对阴沟肠杆菌高产AmpC酶突 变 的 选 择 作 用 [J].中 华 医 院 感 染 学 杂 志,2003,13(4):15-18.
[7] 年华,褚云卓,王倩。医院感染大肠埃希菌耐药性变化分析[J].中华医院感染学杂志,2007,17(4):452-454.