摘 要: 喜树碱具有较强的抗肿瘤活性, 喜树碱E环的修饰主要目的是抑制内酯的水解, 从而提高E环的稳定性。在喜树碱的E环引入二硫键即可保护α-羟基内酯环又可增强其靶向性。本文以喜树碱 (CPT) 为原料, 与3, 3'-二硫代二丙酸在缩合剂的作用下, 发生部分O-酰化反应, 合成了喜树碱-20-O- (3, 3'-二硫代二丙酰) 单酯, 通过考察缩合剂、反应时间和反应温度对O-酰化反应的影响, 选定EDCI为缩合剂剂, 以DMAP为缩合活化剂, 室温下搅拌反应12小时, 经柱层析纯化, 产品收率可达62%。
关键词: 喜树碱; 缩合剂; 酰化反应;
喜树碱 (Camptothecin, CPT) 是从我国特有植物喜树中提取得到的生物碱。喜树碱具有较强的抗肿瘤活性, 对多种实体肿瘤以及白血病具有明显的抑制作用。喜树碱的构效关系研究证明, 喜树碱E环结构中闭合的α-羟基内酯环是抗肿瘤活性的必需结构, 但由于α-羟基内酯环在人体的生理环境内易水解开环形成羧酸盐, 这种开环形式与人血清蛋白结合就使喜树碱丧失了抗肿瘤活性。喜树碱E环的修饰主要目的是抑制内酯的水解, 从而提高E环的稳定性[1]。基于利用药物传递系统的专一性和靶向性, 将药物分子输送至特定的细胞的设计思路, Henne等人设计并合成了以叶酸为受体的小分子药物组合物[2], 利用二硫键、酰胺键和碳酸酯键将叶酸、单分散PEG和喜树碱连接到一个分子中, 取得了较好的抗肿瘤效果。为了克服喜树碱的毒副作用和低水溶性, Borrelli等人[3]通过二硫键将Squalene连接到喜树碱分子结构中, 合成了在水溶液中能够形成自主肿瘤装纳米粒, 进入细胞后能够释放出药物的喜树碱前药分子, 抗肿瘤活性增强约10倍。因此, 在喜树碱的E环引入二硫键即可保护α-羟基内酯环又可增强其靶向性。本文以喜树碱 (CPT) 为原料, 与3, 3'-二硫代二丙酸在缩合剂的作用下, 发生部分O-酰化反应, 合成了喜树碱-20-O- (3, 3'-二硫代二丙酰) 单酯, 研究其可行性及合适的反应条件, 为其工业化应用提供理论和实验依据。
1 、实验部分
1.1 、试剂与仪器
喜树碱 (97%, 西亚试剂) 3, 3'-二硫代二丙酸 (98%, 麦克林试剂) 、N, N'-二环己基碳酰亚胺 (DCC) 、1-乙基- (3-二甲基氨基丙基) 碳酰二亚胺盐酸盐 (EDCI) 、DMAP、DMF、二氯乙烷、二氯甲烷、甲醇等均为分析纯试剂。Bruker AVANCE-300MHz核磁共振仪, KH-2100法定型双波长薄层色谱扫描仪;硅胶H-CMC-Na薄层板。
1.2、 产品制备
将2.1克 (0.01摩尔) 3, 3'-二硫代二丙酸溶于50毫升DMF中, 依次加入1克二甲氨基吡啶、3.5克 (0.01摩尔) 喜树碱、3克N, N'-二环己基碳酰亚胺 (DCC) , 在室温下搅拌12小时, 向反应液中加入500毫升冰水, 静止过夜, 过滤, 水洗, 将滤饼用硅胶柱层析 (二氯甲烷:甲醇=20:1) , 得浅黄色喜树碱-20-O- (3, 3'-二硫代二丙酰) 单酯。结构鉴定:1HNMR (300MHz, DMSO-d6, ppm) :δ0.96 (3H, t, H-19) , 2.10 (2H, m, H-18) , 2.58-2.72 (4H, m, -OOCCH2CH2S-) , 2.87-2.99 (4H, m, -OOCCH2CH2S-) , 5.11 (2H, s, H-5) , 5.50 (2H, s, H-17) , 6.89 (1H, d, N-H) , 7.14 (H, s, H-14) , 7.72 (1H, q, H-10) , 7.87 (H, t, H-11) , 8.00 (1H, d, H-12) , 8.14 (1H, d, H-9) , 8.42 (1H, t, N-H) , 8.65 (1H, s, H-7) 。确定产品为喜树碱-20-O- (3, 3'-二硫代二丙酰) 单酯。
1.3 、合成条件优化
将0.21克 (0.001摩尔) 3, 3'-二硫代二丙酸溶于100毫升二氯乙烷中, 依次加入0.1克二甲氨基吡啶、0.35克 (0.001摩尔) 喜树碱、一定量的缩合剂, 搅拌反应, 每2小时取样, 利用TLCS法[4]测定反应液中喜树碱的含量并计算喜树碱的转化率。薄层条件如下:硅胶H-CMC-Na薄层板, 展开剂:二氯甲烷-甲醇 (20∶1, V/V) , 喜树碱Rf值0.45、喜树碱-20-O- (3, 3'-二硫代二丙酰) 单酯Rf值0.20, 单波长线性扫描, λs:360 nm。
2 、结果与讨论
2.1、 缩合剂的选择
羧酸能够与醇发生O-酰化反应生成酯, 由于喜树碱α-羟基内酯环为叔醇, 且3, 3'-二硫代二丙酸的酰化能力较弱, 所以喜树碱 (CPT) 与3, 3'-二硫代二丙酸必须在缩合剂的作用下, 才能发生部分O-酰化反应。目前, 常用的缩合剂主要有三种:二环己基碳二亚胺 (DCC) 、二异丙基碳二亚胺 (DIC) 和1- (3-二甲胺基丙基) -3-乙基碳二亚胺 (EDCI) 。DCC是使用频率最高的缩合剂, 廉价, 固体状, 方便实用。但是, 反应中生成的副产物DCU难于除去。DIC性质与DCC类似, 室温下为液态。EDCI副产物可以溶于水, 所以可以很容易被除去, 这是其最大的一个优点。因此常应用于医药品的工业合成中, 但是价格比DCC要昂贵。本文分别选用DCC和EDCI做缩合剂, 进行比较研究。
2.2 、反应时间对喜树碱转化率的影响
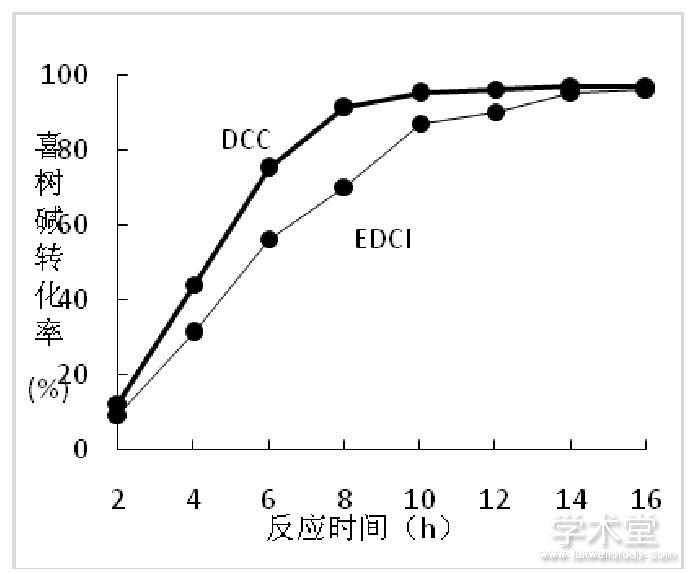
分别以DCC和EDCI做缩合剂, 以DMAP为缩合活化剂, 在室温下搅拌反应, 每2小时取样, 检测, 考察酰化反应时间对喜树碱转化率的影响, 实验结果 (见图1) 表明, 随酰化时间的延长, 喜树碱的转化率增加, DCC为缩合剂, 反应时间8小时左右喜树碱基本反应完全, 而EDCI为缩合剂则需14小时, 可见对于喜树碱-20-O- (3, 3'-二硫代二丙酰) 单酯的合成, DCC的催化活性较高。另外, 随着反应时间的延长, 副产物也随之增加, 故反应时间不宜过长。
2.3、 反应温度对喜树碱转化率的影响
分别以DCC和EDCI做缩合剂, 以DMAP为缩合活化剂, 在不同温度下搅拌反应4小时, 取样, 检测, 考察酰化反应温度对喜树碱转化率的影响, 实验结果 (见图2) 表明, DCC为缩合剂, 反应温度升高, 喜树碱转化率增加, 但增幅不显着, 但通过薄层色谱检测, 发现随着反应温度升高, 有较多副产物的生成。EDCI为缩合剂, 反应温度升高, 喜树碱的转化率先增加后降低, 这可能是EDCI在较高温度下发生分解反应, 失去了催化缩合功能。
考虑到成本和后处理的难度, 选定喜树碱-20-O- (3, 3'-二硫代二丙酰) 单酯的合成条件为EDCI为缩合剂, 室温下搅拌反应12小时, 经柱层析纯化, 产品收率可达62%。
3、 结论
为提高喜树碱E环的稳定性, 以喜树碱为原料, 与3, 3'-二硫代二丙酸在缩合剂EDCI的作用下, 以DMAP为缩合活化剂, 室温下搅拌反应12小时, 经柱层析纯化, 得喜树碱-20-O- (3, 3'-二硫代二丙酰) 单酯, 产品收率可达62%。该方法用于制备喜树碱-20-O- (3, 3'-二硫代二丙酰) 单酯, 反应条件简单, 产品纯化容易, 具有较好的实际应用价值。
图2 反应温度对喜树碱转化率的影响
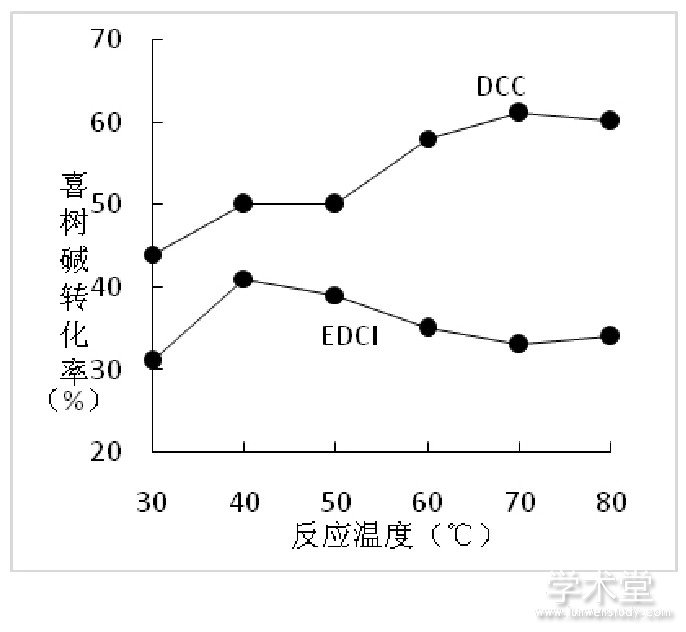
图1 反应时间对喜树碱转化率的影响
参考文献
[1]张磊, 张泽国, 王京.喜树碱衍生物的抗肿瘤研究进展[J].天然产物研究与开发, 2016, 28:1830-1837.
[2]Henne WA, et al. Synthesis and activity of a folate targetedmonodisperse PEG camptothecin conjugate[J].Bioorg MedChem Lett, 2013, 23:5810-5813.
[3]Borrelli S, et al. New class of squalene-based releasablenanoassemblies of paclitaxel, podophyllotoxin, camptothecinand epothilone A[J].Eur J Med Chem, 2014, 85:179-190.
[4]王立屏, 魏永巨.薄层荧光扫描法测定喜树果中喜树碱及10-羟基喜树碱[J].分析测试学报, 2012, 31:282-289.