摘 要: 目的 探讨细胞因子样基因家族3B(FAM3B)基因与疾病相关性的研究进展。方法 分析FAM3B基因与肿瘤、代谢、2型糖尿病、唐氏综合征等疾病的相关性及其作用机制。结果与结论 FAM3B在胃癌、口腔鳞状细胞癌、结肠癌等肿瘤中异常表达,可影响葡萄糖代谢,并与2型糖尿病、唐氏综合征等其他疾病密切相关。此类研究可为肿瘤治疗提供潜在的诊断与治疗靶点,为2型糖尿病等疾病的治疗拓展新方向。但FAM表达调控机制及在脂肪代谢等方面的新功能仍有待进一步研究。
关键词 : 细胞因子样基因家族3B; 2型糖尿病;肿瘤;代谢;唐氏综合征;相关性;
Abstract: Objective To investigate the research progress of the correlation between the cytokine-like factor family with sequence similarity 3,member B( FAM3 B) gene and the diseases. Methods The correlation between FAM3 B gene and tumor,metabolism,type 2 diabetes mellitus( T2 DM),Down's syndrome and its mechanism. Results and Conclusion The abnormal expression of FAM3 B in gastric cancer,oral squamous cell carcinoma,colon cancer and other tumors can affect glucose metabolism,and it is closely related to T2 DM,Down's syndrome and other diseases. This kind of research can provide potential diagnostic and therapeutic targets for tumor therapy,and expand new directions for the treatment of T2 DM and other diseases. However,the regulatory mechanism of FAM'S expression and its new function in fat metabolism still need to be further studied.
Keyword: cytokine-like factor family with sequence similarity 3,member B; type 2 diabetes mellitus; tumor; metabolism; Down's syndrome; correlation;
细胞因子是由多种细胞合成并分泌的,具有重要调节功能的肽类物质,如白细胞介素、γ干扰素、转化生长因子-β及促红细胞生成素等。有些细胞因子在一级结构上无同源性,但具有相似的二级结构。AURORA等[1]编制了名为“折叠的表面识别”(ORF)的计算机程序,原理是通过预测的蛋白质二级结构寻找具有同源结构的蛋白质。2002年,ZHU等[2]利用ORF程序从NCBI的基因库中寻找到4个同源性基因,这些基因被命名为细胞因子样基因家族3(FAM3)。这4个基因也分别被命名为FAM3A,FAM3B,FAM3C,FAM3D基因,其中FAM3B又称胰腺衍生因子(PANDER),属细胞因子。人的FAM3B基因定位于第21号染色体的短臂22号区间(21q22)。FAM3B和FAM3C都具有相似的β-β-α折叠,与经典的细胞因子如四螺旋束家族、肿瘤坏死因子(TNF)家族、β-三叶家族有显着不同。FAM3B和FAM3C代表了信号分子的新结构类别,与传统的四螺旋束细胞因子相比,作用方式不同[3]。在此,综述了FAM3B在肿瘤、代谢及其他疾病方面的研究进展。

1 、肿瘤方面
1.1、 FAM3B在肿瘤中异常表达
2002年邵勇等[4]通过互补脱氧核糖核酸(c DNA)微阵列与聚类分析,检测胃癌与非肿瘤胃组织的基因表达差异,结果发现,FAM3B基因在胃癌组织的表达水平低于非肿瘤胃组织。黄海力等[5]通过反转录聚合酶链反应(RT-PCR)分析也得到FAM3B基因在胃癌组织中表达水平降低的结果。SHIIBA等[6]筛选DNA芯片发现,与人正常口腔角质形成细胞(HNOK)相比,口腔鳞状细胞癌(OSCC)衍生的细胞系中FAM3B水平明显降低。为了测试mi RNA[7,8]是否会影响FAM3B的表达,对OSCC细胞系进行了mi RNA微阵列分析,结果显示,mi R-181a,mi R-181b,mi R-200b和mi R-200c的表达水平较高,表明FAM3B表达的降低可能受到这几个mi RNA的调控。然而,这些研究虽发现了FAM3B的异常表达,但并未研究其异常表达对肿瘤产生的影响。
1.2 、FAM3B影响肿瘤发展的机制
LI等[9]在研究结肠癌细胞系中FAM3B的表达时发现了编码258个氨基酸残基的FAM3B-258。有学者设计了小分子核糖核酸(RNA),检测了Slug基因的表达,因为Slug基因是一种转录抑制因子,能抑制E-钙黏蛋白(E-cadherin)的表达,从而诱导上皮间质化(EMT)的发生[10]。并发现FAM3B-258的过表达能促进结肠癌细胞的迁移和侵袭,增强Slug基因的表达,降低E-cadherin的表达;在si Slug的细胞系中发现,沉默Slug后E-cadherin的表达水平显着升高,同时减轻了对细胞的侵袭。在小鼠活体试验中发现,FAM3B-258可促进结肠癌细胞的转移[9]。以上研究表明,FAM3B促进结肠癌细胞的迁移和侵袭,与上调Slug的表达水平有很大关系。
MACIEL-SILVA等[11]研究发现,FAM3B在前列腺肿瘤中抗凋亡的B淋巴细胞瘤-2(bcl-2)基因和B淋巴细胞瘤-XL(bcl-XL)基因表达水平升高,促凋亡bcl-2相关X蛋白(Bax)基因的表达水平略有下降。为了研究FAM3B能否促进细胞增殖,通过RT-PCR法和免疫组化法分析切开的肿瘤样品的基因表达情况,确定了FAM3B的过表达不会诱导细胞增殖,而是通过上调bcl-2和bcl-XL抗凋亡基因及下调Bax促凋亡基因的表达来促进抗凋亡表型的发展。
ASHRAFIZADEH等[12]发现,肿瘤化学治疗常用药物顺铂的疗效受EMT的显着影响。SONG等[13]研究顺铂治疗胃癌时发现,FAM3B的过表达增加了胃癌细胞的耐药性。因为过表达的FAM3B通过上调转录抑制因子Snail进而诱导胃癌细胞的EMT,对Snail进行沉默处理后能逆转其诱发的胃癌细胞的耐药性。因此,对FAM3B与Snail的研究有望为治疗胃癌提供新的靶点。
1.3 、与FAM3B密切相关的p53信号通路
研究发现,FAM3B基因敲除后,p53表达水平明显升高,沉默p53则几乎可以完全逆转FAM3B表达抑制后诱导的Bax表达水平的升高,Bcl-2表达水平的降低,金属蛋白酶(caspases)-3、caspases-8、caspases-9的裂解和凋亡的细胞死亡,这表明p53信号通路在FAM3B沉默诱导的凋亡中起关键作用[14]。
HE等[15]在研究人食道鳞状细胞癌(ESCC)时发现,AKT-MDM2-p53信号通路和EMT中相关蛋白异常表达,western blot法分析结果显示,沉默FAM3B表达后p-AKT,MDM2,Snail,N-cadherin蛋白表达水平均显着降低,而p53和E-cadherin蛋白表达水平显着升高。过表达FAM3B则显示出相反的结果,p53表达水平降低能减少细胞的凋亡,Snail表达水平升高和E-cadherin表达水平降低能增加细胞的迁移和侵袭。磷酸化形式p-AKT和MDM2负调控p53,FAM3B过表达增加了p-AKT和MDM2的表达,故p53的表达被抑制,而p53是重要的肿瘤抑制因子,从而降低肿瘤细胞的凋亡率[16]。具体过程见图1。
2、 代谢方面
2.1、 对胰岛细胞的影响
FAM3B/PANDER主要表达于胰岛A细胞和B细胞[17,18]。葡萄糖、游离脂肪酸和促炎细胞因子能有效诱导胰腺B细胞中FAM3B基因的表达[19,20,21,22]。而过表达的FAM3B能诱导胰腺A细胞和B细胞凋亡[23]。FAM3B在胰岛B细胞中有调节或促进胰岛素分泌的潜在作用[24]。FAM3B在调节胰岛B细胞功能中具有双重作用,即促进生理条件下的胰岛素分泌,而异常升高的FAM3B在胰岛素抵抗条件下会对胰腺B细胞功能产生危害[25]。
2.2、 对葡萄糖代谢和2型糖尿病(T2DM)的影响
MOAK等[26]建立了纯种的FAM3B基因敲除小鼠,发现其与对照组相比表现出增强的代谢表型,尤其是在葡萄糖耐量方面。ROBERT-COOPERMAN等[27]发现,胰腺B细胞过度表达FAM3B会降低肝p-AMPK信号传导,从而减弱胰岛素对糖异生的抑制作用。FOXO1是控制糖异生基因表达和糖异生的关键转录因子之一,其通过控制肝细胞中两个关键的糖异生基因的表达在调节糖异生中起决定作用[28]。FAM3B可与FOXO1结合,FAM3B的过表达能增强FAM3B-FOXO1的相互作用,激活FOXO1以诱导糖原异生基因表达,并促进肝细胞糖异生[29]。控制糖异生是糖尿病治疗的重要步骤,因此FAM3B在治疗糖尿病方面有重要前景。
图1 FAM3B相关p53信号通路调控机制
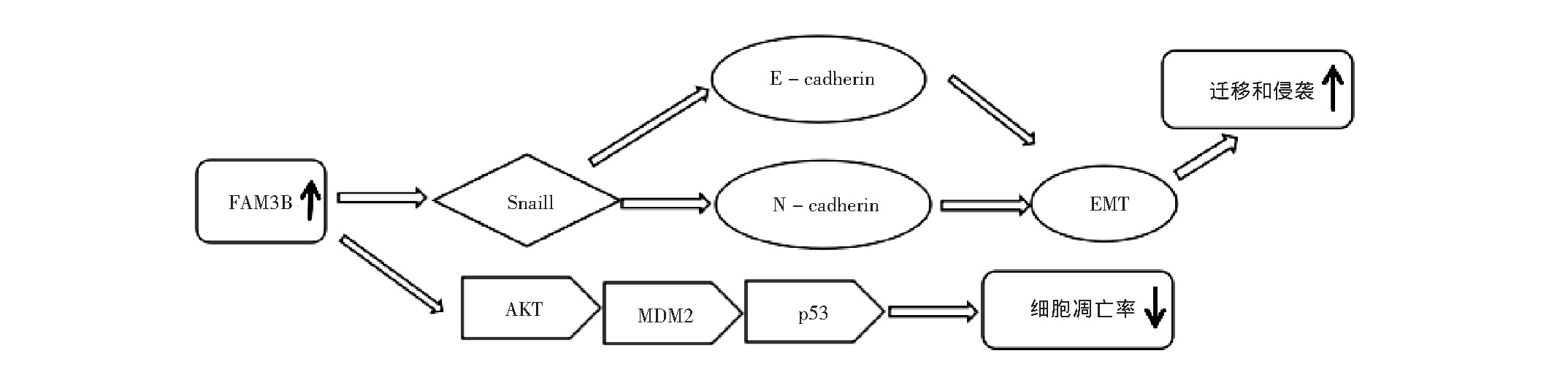
Fig.1 Regulation mechanism of FAM3B related p53 signaling pathway
通过对人体内循环FAM3B水平的研究发现,其与T2DM密切相关,其中糖化血红蛋白(Hb A1C)、空腹血糖(FBG)与FAM3B水平的升高呈中等线性相关[30]。代谢综合征患者的体内循环FAM3B水平升高,还可用于预测中国人群患T2DM的概率[31]。另一项临床报告证实,代谢综合征患者血清FAM3B水平升高,而循环FAM3B水平升高可被视为新发代谢综合征(Met S)及其进展的预测指标[32]。通过反复自交糖耐量降低的Wistar大鼠可建立T2DM模型,对其全基因组测序分析发现,FAM3B与模型大鼠的糖尿病密切相关[33]。而在妊娠期糖尿病(GDM)孕妇血清中的FAM3B水平明显高于正常孕妇,且与胰岛素、Hb A1C水平呈正相关[34]。以上研究表明,FAM3B能被确定为抗T2DM的新型治疗靶点[35,36]。
3 、其他疾病方面
FAM3B所在人的第21号染色体上Cbr1-Fam3b是唐氏综合征关键区域之一。研究发现,Cbr1-Fam3b与相关基因作用具有高度复杂性,决定了唐氏综合征的发育性认知缺陷表型[37,38]。在爱泼斯坦-巴尔病毒(EBV)阳性肿瘤中,FAM3B的甲基化程度显着增加[39]。FAM3B过表达抑制mi R-322-5表达,促进血管平滑肌细胞(VSMC)增殖和迁移,FAM3B可能成为治疗相关心血管疾病的新靶点[40]。ZHAO等[41]研究发现,FAM3B能负向调节肌肉细胞的分化。甲基转移酶家族成员SETD3可促进该分化,而mi R-322可抑制SETD3分化,并对成肌细胞的分化产生负面影响。但FAM3B可消除mi R-322的抑制作用,并促进肌肉细胞分化。
4 、展望
FAM3B最初在胰腺中被发现,其后,研究者对其与葡萄糖代谢的关系做了大量研究,鉴于其对糖原异生的促进作用,通过抑制其表达,可为T2DM的治疗拓展新方向。后续研究发现,FAM3B可促进上皮间质化及影响p53信号通路相关蛋白,在此基础上探讨其病理生理意义,为肿瘤治疗提供了潜在的诊断与靶向治疗靶点。然而,由于FAM3B对糖代谢与肿瘤发展等方面的作用及其机制差异巨大,对FAM3B表达调控机制仍有待进一步研究。此外,FAM3B对人体脂肪代谢也有一定影响,但缺乏更多明确的认识,继续研究可能会给心血管疾病治疗提供稳定靶点。随着研究的深入,有望发现FAM3B基因的新功能,拓展对其的认识。
参考文献
[1]AURORA R,ROSE GD .Seeking an ancient enzyme in Methanococcus jannaschi using ORF,a program based on predicted secondary structure comparisons[J].Proc Natl AcadSci U S A,1998,95(6):2818-2823.
[2]ZHU Y,XU G,PATEL A,et al.Cloning.expression, and initial characteriz ation of a novel cytokne-like gene family[J]. Genomics 2002 ,80(2)-144-150.
[3]JOHANSSON P,BERNSTRCM J,GORMAN T,et al.FAM3 BPANDER and FAM3C ILEI represent a distinct class of signaling molecules with a non-cytokine-like fold[J]. Structure,2013,21(2):306-313 .
[4]邵勇,杨少波,王孟薇,等.胃癌基因表达谱的c DNA微阵列与聚类分析[J] . 中华医学遗传学杂志, 2004,21(2):18-23 .
[5]黄海力,吴本俨,杨少波,等. PANDER基因在胃癌中的表达下调[J] .世界华人消化杂志,2008, 16(14):1513-1518。
[6]SHIIBA M,ISHIGE S,SAITO Y,et al.Down-regulated expression of family with sequence similarity 3,member B(FAM3B),in oral squamous cell carcinoma[J].Oral Sci Int,2012,9(1):9-16 .
[7]I0IO MV,CROCE CM.Micro RNAs in cancer:small molecules with a huge impact[J]J Clin Oncol,2009,27(34):5848-5856.
[8] LEE YS,DUTTAA.Micro RNAs in cancer[J] Annu Rev Pathol,2009,4:199-227.
[9]LI Z,MOU H,WANG T,et al.A non-secretory form of FAM3Bpromotes invasion andmetastasis of human colon cancer cells by upregulating Slug expression[]. Cancer Lett,2013,328<2):278-284 .
[10]PHIL LIPS S,KUPERWASSER C SLUG:Critical regulator of epithelial cell identity in breast development and cancer[J]. Cell Adh Migr,2014.8(6):578-587.
[11]MACIEL-SILVA P,CALDEIRA 1,DE ASSIS SANTOS l,et al.FAM3B/PANDER inhibits cell death and increases prostate tumor growth by modulating the expression of Bcl-2 and Bcl-XLcell survival genes[J] BMC Cancer,2018, 18(1):90.
[12]ASHRAFIZADEH M,ZARRABI A,HUSHMANDI K,et al. Association of the Epithelial-Mesenchymal Transition(EMT)with Cisplatin Resistance[J].Int J Mol Sci,2020,21(11):e400
[13] SONG C,DUAN CM. Upregulation of FAM3B Promotes Cisplatin Resistance in Gastric Cancer by Inducing Epithelal-Mesenchymal Transition[J] Med Sci Monit,2020,26:e921002.
[14]MOU H,LI Z,YAO P,et al.Knockdown of FAM3B triggers cell apoptosis through p53-dependent pathway[J] Int J Biochem Cell Biol,2013.,45(3)-684-691.
[15]HE SL,WANG WP,YANG YS,et al.FAM3B promotes progression of oesophageal carcinoma via regulating the AKT-MDM2-p53 signalling axis and the epithela-mesenchymal transition[J].J Cell Mol Med,2019,23<2):1375-1385 .
[16]SHU X,YANG Z,LI ZH,et al.Helicobacter pylori Infec tion Activates the Akt-Mdm2-p53 Signaling Pathway in Gastric Epithelial Cells[J].Dig Dis Sci,2015,60(4):876-886 .
[17]CAO XP,GAO ZY,ROBERT CE et al. Pancreatic-de rived factor(FAM3 B),a novel islet cytokine induces apoptosis of insulin-secreting beta-cells[J] Diabetes ,2003,52(9)-2296-2303.
[18]XU W,GAO Z,WU J,et al.Interferon-g-induced regulation of the pancreatic derived cytokine FAM3B in islets and insulinsecreting beta TC3 ells[J.Mol Cell Endocrinol,2005,240(1/2):74-81.
[19]BURKHARDT BR,COOK JR,YOUNG RA,et al.PDX-1 interactionand regulation of the Pancreatic Derived Factor(PANDER ,FAM3B)promoter[J] Biochim Biophys Acta,2008,1779(10):645-651.
[20]WANG OM,CAI K,PANG SS,et al.Mechanismsof glucose-induced expression of pancreatic-derived factor inpancreatic beta-cells[J] Endocrinology,2008, 149(2):672-680
[21]XIANG JN,CHEN DL,YANG LY Effect of PANDER inβTC6-cell lipoapoptosis and the protective role of exendin-4[J] Biochem Biophys Res Commun,2012,421(4).701-706.
[22]HOU X,WANG O,LI Z,et al.Upregulation of pancreatic derived factor(FAM3B)expressionin pancreatic beta-cells by MCP-1(CCL2)[J].Mol Cell Endocrinol,2011,343(1/2):18-2
[23]YANG J,GAO Z,ROBERT CE,et al. Structure-function studies of PANDER, an isletpecific cytokine inducing cell death of insulin-secretingbeta cells[J] Biochemistry,2005.44(34):11342-11352 .
[24]ROBERT-COOPERMAN CE, CARNEGIE JR,WIL SON CG,et al. Targeted disruption of pancreatic-derived factor(PANDER,FAM3B) impairs pancreatic beta-cell function[J].Diabees, 2010 ,59(9):2209-2218.
[25] ZHANG X,YANG W,WANG J,et al.FAM3 gene family:Apromising therapeutical target for NAFLD and type 2 diabetes[J].Metab Clin Exp,2018,81:71-82.
[26]MOAK SL,DOUGAN GC ,MARELIA CB,et al. Enhanced glucose tolerance in pancreatic-derived factor(PANDER)knockout C57BL/6 mice[J].Dis Model Mech,2014,7(11):1307-1315.
[27]ROBERT-COOPERMAN CE,DOUGAN GC,MOAK SL,et al.PANDER transgenic mice display fasting hyperglycemia and hepatic insulin resistance[J]J Endocrinol,2014,220(3):219-231.
[28]0-SULLIVAN I,ZHANG WW,WASSERMAN DH,et al.Fox 01 integrates direct and indirect effects of insulin on hepatic glucose production and glucose utilization[J] Nat Commun,2015,6:7079.
[29]CHI Y,MENG Y,WANG J,et al.FAM3B(PANDER) functions as a co-activator of FOXO1 to promote gluconeogenesis in hepatocytes[J]J Cell Mol Med,2019,23(3):1746-1758.
[30]MARELIA CB. KUEHL MN,SHEMWELL TA.et al. Circulating PANDER concentration is associated with increased Hb A1c and fasting blood glucose in Type 2 diabetic subjects[J].J Clin Transl Endocrinol,2018,11:26-30 .
[31]CAO X,YANG C,LAI F,et al. Elevated circulating level of a cytokine,pancreatic-derived factoris associated with metabolic syndrome components in a Chinese popultion[J].J Diabetes Investig,2016,7(4):58 1-586.
1.将微信二维码保存到相册

2.打开微信扫一扫从相册识别
1.点击下面按钮复制QQ号
3008635932
2.打开QQ→添加好友/群
粘贴QQ号,加我为好友