
�������������Ϊ�����Ľ�ʹ�Ļ���ҩ��֮һ�㷺�����ٴ����о�����������͵���Ѫ������ͨ���ͷ�һ������( NO) ���鵼����ȩ����ø 2( ALDH2)����������ø���ԣ����������ת������ NO ���˹ؼ����ã��� ALDH2 ���� Glu504Lys ��̬�ԣ��ᵼ��ALDH2 ������ø���������½���ʹ���������Ч������������( 14��9% vs 42��4% )�������飬AL-DH2 504Lys ��λ����Я����������������͡�
����ALDH2( 504Lys) ��λ������ŷ����Ⱥ��Я���ʼ��ͣ������й���Ⱥ��Я���ʽϸߣ�������ȺЯ���ʸߴ� 30%����ˣ����й���Ⱥ�м�� ALDH2( Glu504Lys) �����̬�Ծ��л�������ʵ���塣�����о������� ALDH2( Glu504Lys) �����̬�Լ�ⷽ�����������ٴ��������
����1 �������Լ�
����PCR �ǣ�Bioer TC-96 / G / H( b) �����ݲ��տƼ�����˾��; ���Ļ�( �ɸ� TGL-16GB �Ϻ���ͤ��ѧ������) ; ����ֹ��ȼ�( onedrop1000���Ϻ�ŵ����������˾) ; ������( GSM417��Affymetrix) ; ����оƬȫ�Զ��ӽ���( BR-526���Ϻ��ٰ��Ƽ��ɷ�����˾) ;����оƬʶ����( BE-2��0���Ϻ��ٰ��Ƽ��ɷ�����˾) ; ����оƬͼ���������( Arraydoctor 2��0���Ϻ��ٰ��Ƽ��ɷ�����˾) ; ������Ӿ�� ( PowerBC-600BC���Ϻ���������Ƽ�����˾) ����������ϵͳ( Bioshine Gelx 1520���Ϻ�Ÿ����������˾) ��
����DNA ��ȡ�Լ���( BST01051���Ϻ��ٰ��Ƽ��ɷ�����˾) ; �ӽ���ɫ�Լ���( BST03021���Ϻ��ٰ��Ƽ��ɷ�����˾) ; ȩ�����ε��ز�Ƭ( BSM03011���Ϻ��ٰ��Ƽ��ɷ�����˾) ; Ӧ�� Primer Premier 5��0�� �� �� �� һ �� �� ��: 5 �� Biotin - AAGACTTT-GGGGCAATACAG 3����3�� CTTCTCAGGCTTAAAAT GGG5��; �ʿعѺ�����: 5��Biotin -ACATCCTCTGGATGATGT-GAGACCATGCGGAGC CCCTCCACG 3 ����2 �����̽��: Ұ����5��( T) 16 CAGGCATACA CTGAAGTGAAAA3����ͻ �� �� 5 ��( T ) 16 GCAGGCATACACTAAAGTGAAAACT 3����1 ���ʿ�̽��: 5 �� NH2-( T) 16 GGTCTCACATCATCCAGAGGATGT 3��( �Ϻ��������﹤�̷�������˾) ; Taq ø��10 ×buffer����������Ƽ�( ����)����˾��; dNTP( �Ϻ��������﹤�̷�������˾) ; EDTA �������ܾ���Ѫ����( �Ϻ��е�һ����ҽԺ����) ; ������( CAS#35-65-4���Ϻ�ԴҶ��������˾) ; ���̴�( CAS#57-88-5��99%���Ϻ�����ʵҵ����˾) ; ��������( CAS#538-24-9���Ϻ�����ʵҵ����˾) ��
����2�� ��������
����2�� 1 �ٴ�����
����EDTA �������ܾ���Ѫ����( �Ϻ��е�һ����ҽԺ������ҽԺ������ҽԺ) �����ֲ��֡����Ŀ�ġ��Ա����䣬ֻҪ����˫������оƬ����������Ҫ����ѡ��
����2�� 2 ��������
������ EDTA �������ܾ���Ѫ���������� DNA �����Լ���( �Ϻ��ٰ��Ƽ��ɷ�����˾) ��ȡȫ������DNA��DNA Ũ��Ϊ 10 �� 60 ng·μl�� 1��A260/A280 �ı�ֵ��1��5 ��2��0��ȡ�Ѵ����� DNA 3��0 μl��Ϊ����ģ�壬������������( 10 pmol·μl�� 1) ����������( 3��3pmol·μl�� 1) ��1��0 μl��Taq ø( 2��5 U·μl�� 1) 1��0 μl��10 × buffer 2�� 5 μl��dNTP( ��2�� 5 mmol·L�� 1) 2��5 μl��˫��ˮ14 μl����Ӧ����� 25 μl��PCR ��Ӧ����Ϊ:50�� 5 min; 94�� 5 min; 94�� 25 s��60�� 25 s��72�� 30s��35 cycles; 72�� 5 min; PCR ���� 4�� ���档
����2�� 3 ALDH2 ����оƬ���Ʊ�
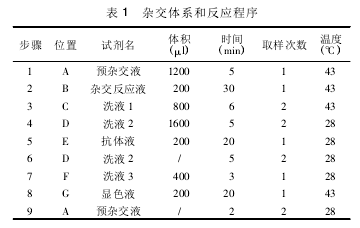
������̽����������ˮ�ܽ��Ʊ���Ũ����Һ���ֱ���2 × ��������Һ���Ƹ�̽��ĵ���Һ����������Һ����Ҫ�����μ��뵽 384 �װ��С�ʹ��ȩ�����λ�Ƭ��Ϊ ALDH2 �����̬�Լ��оƬ����Ĺ���֧������� GSM-417 ����оƬ�����ǣ�������Ƶ�����ͼ1 �ĵ����Ų������е��������������ں������й̶����ܹⱣ�档����ʱ�������¶��� 18-26�棬���ʪ��Ϊ45% ��65%��̽�����Ũ��Ϊ:5 μmol·L�� 1��
��������õ�оƬ�������¹�ҹ�̶���
����
����2�� 4 �ӽ����
������ BaiO�Le-Hyb ȫ�Զ��ӽ��ǰ��� 1 ���÷�Ӧ������Ҫ��������װ�ӽ���ɫ�Լ��и��Լ�����ȡ150 μl �ӽ�Һ���ֱ������������������λ������������10 μL�����ȡ��������Լ�����ָ��λ���ڣ����г����ӽ���ɫ��Ӧ�Զ����С��ӽ���ɺ�оƬ��ɫ��������ˮ����ϴ����ɣ���оƬ����BE-2�� 0����оƬʶ�����н���ɨ�裬��õ�оƬ�ӽ����ͼ���û���оƬͼ���������( Arraydoctor2�� 0���Ϻ��ٰ��Ƽ��ɷ�����˾) ��ȡ������ź�ǿ�ȣ�����������͵���ֵ���������������ݷ��������оƬ���Ļ����ͽ����
��
����2�� 5 ALDH2 ��ɫ����оƬ��������
����2�� 5�� 1 оƬ��������� ѡȡ��������֤ ALDH2������Ϊ Lys504Lys ����������ȡ������ DNA��Ũ�ȵ���Ϊ50 ng·μl�� 1�������ݶ�ϡ�͡���ÿ��ϡ�Ͷ�DNA ���� PCR ��������оƬ�ӽ������ظ����μ�����ͽ������ȷ����� DNA ��Ϊ����ޡ�������ȷ�������Ϊ5 ng ������ DNA��
����2�� 5�� 2 оƬ���ȷ�� ѡȡ 3 �� ALDH2 �����͵�Ũ��Ϊ50 ng·μl�� 1������ DNA���ֱ���� PCR ��������оƬ�ӽ������ 3 �ֻ������������������ȷ��
����2�� 5�� 3 оƬ��������� ȡ�㾫 DNA ϡ�����ӽ��������˻����� DNA ����Ũ��( 20 ng·μl�� 1) ��Ϊ���Զ��ս��� PCR ��������оƬ�ӽ��������Ϊ���ԡ�
����2�� 5�� 4 оƬ����ظ��� ѡȡ ALDH2 ������ΪLys504Lys ��Ũ��Ϊ 25 ng·μl�� 1������ DNA������PCR ��������оƬ�ӽ���ÿ�������ظ���� 10 �Ρ�10 �μ���������;�һ�¡�
����2�� 6 ALDH2 ��ɫ����оƬ����ʵ��
����ȡ2-8�汣�治����5d ������ ALDH2 �����ͱ�( ALDH2 Glu504Glu ���: H1; ALDH2 Glu504Lys ���: H2; ALDH2 Lys504Lys ���: H3) �� EDTA ��������ȫѪ������ÿ�������ֳ� 5 �ݣ�1 �ݲ��Ӹ�������Ϊ�հ���( ���: ��) ��1 �ݼ���3 000 mg·dl�� 1��������( ���: G) ��1 �ݼ���250 mg·dl�� 1���̴�( ���:Ch) ��1 �ݼ��� 20 mg·dl�� 1������( ���: Bi) ��1 ����ȫ��Ѫ( ���: He) ������ѪҺ������ DNA ��ȡ������ȡ��������ѪҺ������ DNA���� PCR ��������оƬ�ӽ��������ͣ�ÿ�������ظ� 2 �Σ�H3 �����͵����������٣�ֻ����1 �Ρ�
�����о������ʾ�����������������ʵ�Ѫ������DNA ��ȡ��DNA ��Ũ�Ⱥʹ����������հ�Ѫ����ȣ�û���������죬�� PCR ����������оƬ�ӽ���⣬�������������֪������һ�¡���� EDTA ����ȫѪ�����к��� 3 000 mg·dl�� 1���������ͣ�250 mg·dl�� 1���ܵ��̴���20 mg·dl�� 1�ĵ����أ��� ALDH2����оƬ�ⶨû��Ӱ�죬��ȫ��Ѫ�� EDTA ����ȫѪ�ԲⶨҲû��Ӱ�졣
����2�� 7 ALDH2 ��ɫ����оƬ���ܶ�ʵ��
����ѡ��3 �� ALDH2 ��������֪( ˫�����) ��������ÿ�������ֳ����ݣ��ֱ��������μ��ٴ�ʵ���ʵ�������걨�Լ��вⶨ��ÿ��ʵ���Ҳ����������ŵ��Լ��У�ÿ�������Լ���ÿ����Ʒ��ͬһʵ���ҵ���������Ա���ⶨ���Ρ�������ȷ�ⶨ���ռ�ܲⶨ����İٷ��ʼ����Լ��в�Ʒ�����ڣ����侫�ܶȺͲ��졣
�������ܶ�ʵ�鹲���243 ���������243 �����������֪�����;����ϡ��Զ��Խ�����ۣ�������������졣
����2�� 8 ALDH2 ��ɫ����оƬ�����ȶ�ʵ��
����������оƬ�������˫���������Ƚϣ����� ALDH2 ��ɫ����оƬ�����ٴ������ԡ�ѡ������ҽ�ƻ���ʵ���ң������ 1035 �������ٴ������ EDTA ����Ѫ������ѡȡ���ٴ����˼������һ��Ϊ����һ��ֱ���ͽ�ѡ���Ļ��������������������� DNA �� ALDH2 ����� Glu504Lys λ�����˫�����; һ�ݽ���оƬ��⡣оƬ������ɹ���������������
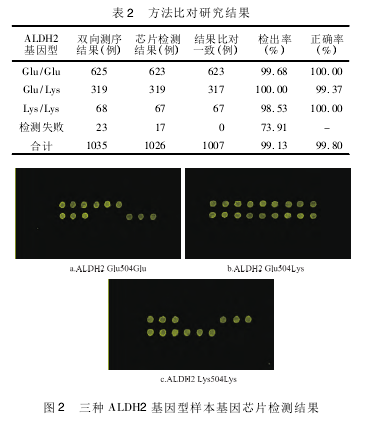
���������ȶ��о����ݼ���2�������1026 ������оƬ�������1012 ��˫����������������� 3 ��ALDH2 ��������ͼ 2 ��ʾ����ͳ���� 1009 ����������оƬ������ͻ�����������������ȶԷ�������1007 �ݻ����ͼ�������������ȫһ�£���2�����������һ�£�оƬ�����Ϊ ALDH2( G/G)�ͣ�������Ϊ( G/L) �͡���ʵ����������ܵ�ԭ�������� DNA ��ȡʧ�ܣ�Ũ�ȵ��ڼ�������¡�ͳ�ƽ����ʾ�������Լ����ٴ����ļ����Ϊ: 99��13%( 1026/1035) ; ��ȷ��Ϊ:99��80%( 1007/1009) ��
����
����2�� 9 ALDH2 ��ɫ����оƬ�ȶ���ʵ��
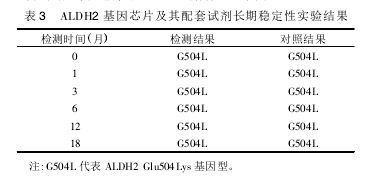
����ȡ�Ʊ��õ� ALDH2 ����оƬ 24 Ƭ������PCR �������ӽ���ɫ�Լ������� �� 20�� ���䳤�ڴ��棬�ֱ���0��1��3��6��12��18 ����ȡ��3 Ƭ�������� ED-TA ����Ѫ����ȡ��Ũ��ϡ���� 8 ng·μl�� 1���Ӻ�DNA ���� PCR ��������оƬ�ӽ�����������Ʊ���ALDH2 ����оƬ������ PCR �������ӽ���ɫ�Լ�������Ƚϡ�ʵ��������3��ALDH2 ��ɫ����оƬ���������Լ����� ��20�洢��18 ���£����������û�����Ա仯�����������ȶ��ԡ�
����3�� ����
����3�� 1 оƬ���
�����ټ��û���оƬ����ư���̽��ṹ�����; �ʿ�̽��Ŀ���; ̽��Ũ�ȵ�ѡ��; �����Ų�����Ƶȡ���̽��ṹ����ϣ�Ϊ����̽��̶���ȩ����Ƭ�ϣ�̽���5���˽��а�������; Ϊ��֤̽�������������ӽ���Ӧ�ij���ԣ���С��Ӧ�Ŀռ�λ�裬��̽���백��֮�仹������һ�� 5 ��25 �۵ľ����������ᡣ
�����ʿ�̽�������Ӧ���Դﵽ��������Ŀ��Ϊԭ��
�������о�����оƬ���õ��ʿ�̽�����ͬʱ�������ʿ�̽��ͻ�ѧ����̽������á���̽������̽��һ��ֻ������5���������Σ��ڻ�Ƭ�ϵĹ̶�Ч�����Է�ӳ̽����������; ͬʱ��̽��ֻ�뷴Ӧ��ϵ����ӵĴ��������ر�ǵİб�( �ʿعѺ�����) �����������ӽ���Ӧ���÷�Ӧֻ���ӽ�������أ��ʿ����ڼ���ӽ����̵�����������оƬ��������Ⱦɫ������⣬���Բ��������Զ���̽����ڶ���̽�롣ʹ�ñ�оƬʱ���������Զ���Ʒ�����Զ���Ʒ�����ϸ�Ӧ�������������ظ�����ʵ��������оƬ�ӽ��������ԡ�����оƬ���е���ƣ����뿼�������ڿ˷�������ʵ��ƫ������Զ��������ʱ���ܳ������еĸ��ֿ��ܡ�ͨ�������Զ���̽�밴һ�������Ų������������Զ������еĶ�λ��Ѱ�㡢�ɼ��źš�ÿ��̽�����ظ�������ò����� 3 �Σ�ȡƽ��ֵ�ɿ˷����������о�ÿ��̽���ظ� 6 �Σ��������У��������ڿ˷����������ɷ�������ʵ��ƫ��µ��źŲ����ȷֲ����µ����С�
����3�� 2 оƬ��������
��������оƬ��⼼��������㡢�ɿ��١�ȷ����ͨ���ķ�������ǧ�ƵĻ�������Ϣ���dz��ʺ��ڳ����ٴ����顣���ۻ���оƬ���ܵķ�����ָ�������ʵ��Ӧ�����Ӧ���ٴ�������ĵ�����ָ����Ҫ����: ȷ�ԡ������ԡ������ԡ��ظ��ԡ��������ԡ��ȶ��Եȡ���������ָ��ʱ��Ӧ��ʹ����ʵ���ٴ���������������ʹ�������������Ȼ�����С�ܶ࣬�Ƚϴ�������������ʵ��������ܴ�������������ʱ����ѡ���Ӻ���������ͬ��Ũ�����봿������ȣ��Ӻ���������λ����Ŀ��������룬��������Ӱ����������ظ���ʱ��ѡ���е�Ũ�� DNA ���д����ԡ�
����3�� 3 �ⶨ�������
�������ױ�����ALDH2 504Lys ��λ������ŷ����Ⱥ��Я���ʼ��ͣ������й�������Ⱥ�е�Я���� 17%�� 36% ���ȡ����о��������ʾ������λ����Я����Ϊ22�� 4%�������ױ���һ�¡����������Ϊ�Ľ�ʹ����ҩ�ʹ����Ч������������غ����
������Я�� ALDH2 504Lys ��λ���������������Ч���ʴ��������������ٴ���չ���� ALDH2 �����������ҩָ������ҽ�ƻ���ҩ�¹����涨���ٴ�ҩʦΪ�ٴ���չ���廯��ҩָ����Ҫ�����ٴ�ҩѧʵ���Ҷ��Ŵ�������ⷽ��ȱ�����飬���Զ������������ȷ�������ȶ��ɿ��Ļ����⼼������ǿ�ҡ����о���������ɫ����оƬ��ⷽ�����Զ����̶ȸߣ�������㣬���ȷ�������ٴ��������������ƹ㡣