
乳腺癌是全球女性最高发恶性肿瘤,死亡率仅次于肺癌,位居第二[1].无论国内、国外,每年激素受体阳性乳腺癌患者的比例均占全部乳腺癌患者的一半以上.针对此类患者的首要治疗是内分泌治疗.然而,在内分泌治疗过程中,原发的内分泌治疗抵抗以及药物使用时间过长产生的获得性耐药,严重影响了乳腺癌患者的远期治疗效果.因此,对内分泌耐药的研究已引起越来越多学者的关注,成为当今肿瘤研究的热点之一.疏肝益肾方是我科几代中医名家总结出来的治疗激素依赖性乳腺癌的有效方剂,由柴胡、女贞子等合 "理冲汤"组成,具有疏肝益肾,调理冲任之血 ( 活血) 的功能,攻补兼施,祛邪不伤正的作用.本实验就疏肝益肾方对人乳腺癌 TAM 耐药细胞株 ( MCF-7 TAM-R) 的作用及作用机制进行了初步探索.
1 材料与方法
1. 1 细胞株 MCF -7 TAM -R: 对三苯氧胺耐药的乳腺癌 MCF-7 细胞,由 Georgetown University MedicalCenter 的 Clarke 博士惠赠.
1. 2 实验药物 疏肝益肾方药物组成: 黄芪、白术、山药、三棱、莪术、柴胡、白芍、女贞子、仙灵脾、海藻、甘草、山慈姑、穿山甲、全蝎、蒲公英、紫草、白花蛇舌草.药品购自广安门医院 ( 各药样品均需经品种鉴定,注明学名,用药部位、采集地点和季节) ,水煎剂由广安门医院煎药室制备.枸橼酸他莫昔芬片购自扬子江药业集团有限公司( H31021545) ,由广安门医院西药房提供.
1. 3 实验动物 成年 SPF 级雌性同种 SD 大鼠 ( 体重 230g 左右) 30 只,购自北京维通利华实验动物技术有限公司,动物许可证号: SCXK ( 京) 2012 ~0001,于我院动物中心饲养,清洁级.
1. 4 实验试剂与设备 PBS 缓冲液、Cell CountingKit-8 试剂盒 ( 碧云天) ; DMEM 无酚红高糖培养基、胎牛血清、三苯氧胺 ( 4-hydroxytamoxifen) 、0. 25%+ 0. 02EDTA 胰酶消化液 ( 美国 Hyclone) ; 牛胰岛素、二甲基亚砜 ( DMSO) ( 美国 Sigma) .基因芯片依托上海其明信息技术有限公司代为检测.恒温微孔板快速振荡器由江苏海门其林贝尔仪器制造有限公司生产; 多功能酶标仪由美国 Biotek 公司生产.
2 实验方法
2. 1 细胞培养 将 MCF - 7 TAM - R 细胞用无酚红DMEM 培养液 ( 含 10% 胎牛血清,青霉素、链霉素分别 为 100mg /L、0. 01mg/ml 胰 岛 素、10-7mol / LTAM 溶液) 中,在 37℃ ,5% CO2,饱和湿度条件下培养.倒置显微镜下观察细胞贴壁情况,生长状态良好,待其铺满瓶底 70% ~ 80% 时,以 0. 25% 胰蛋白酶消化传代,隔日换液.
2. 2 大鼠含药血清制备 ①雌性 SD 大鼠去势: 大鼠常规饲养一周后,称重,水合氯醛腹腔注射麻醉,剂量为 0. 35ml/100g.于大鼠背部切除卵巢, ( 手术方法参考李仪奎 《中药药理实验方法学》[2]) 缝合后,颈部皮下注射青霉素,并在术后 3 天连续皮下注射青霉素,防止感染.术后大鼠恢复 1 周,开始灌胃.②将大鼠随机分为疏肝益肾方高、中、低组、TAM 组以及空白组 5 个组,每组 6 只.中药组以成人给药的等效剂量的 4、2、1 倍来进行灌胃,TAM组以成人的等效剂量灌胃,阴性对照组以等量生理盐水灌胃,连续5 天.于第5 天最后一次灌胃后 1 小时,经腹主动脉取血,常规离心制备血清,56℃、灭活 30 分钟,过滤分装后,-80℃保存备用[3].
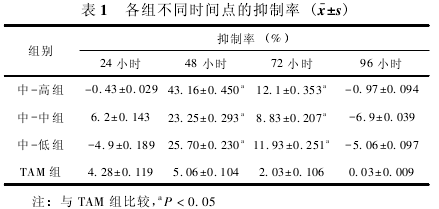
2. 3 CCK8 检测细胞抑制率 以对数生长期细胞 6 ×10^4个/ml 铺 96 孔细胞培养板,24 小时后,将各组血清作用于细胞,以上各组的浓度均有 DMEM 培养液稀释获得,每组设 6 个平行孔,3 个调零孔,每孔200μl.分别在加药后 24 小时、48 小时、72 小时、96 小时,每孔加入 20μl 的 CCK8 培养 1 小时,用酶标仪检测各孔450 吸光度值 ( OD) ,按以下公式计算乳腺癌 MCF-7 TAM-R 细胞在各实验条件、不同培养时间细胞抑制率,细胞死亡率 = ( 1 - 实验组OD450 平均值 / 空白对照组 OD450 平均值) ×100% .结果如表 1.
2. 4 基因芯片检测疏肝益肾方对 MCF-7 TAM-R 细胞的作用机制 根据2. 3 的实验结果,提取加药处理后 48 小时的 MCF-7 TAM-R 细胞的总 RNA,依托上海其明信息技术有限公司代为检测.
2. 5 统计学方法 采用 SPSS 17. 0 软件进行数据分析.结果采用 ( x-±s) 表示,组间比较用方差分析.P < 0. 05 为差异有统计学意义.
3 结 果
3. 1 CCK8 检测含药血清培养细胞后各组抑制率结果显示: 与 TAM 组相比,疏肝益肾方三个剂量组对 TAM 耐药细胞 48 小时,72 小时具有不同的抑制作用 ( P < 0. 05) ,尤以疏肝益肾方高剂量组 48 小时抑制作用最强 ( P < 0. 05) .见表 1.
3. 2 疏肝益肾方逆转 TAM 耐药的机制 疏肝益肾方对 TAM 耐药细胞 MCF-7 TAM-R 有一定的作用,能够抑制耐药细胞的生长.为了明确疏肝益肾方对于MCF-7 TAM-R 产生这些变化的原理和机制,并结合中医复方多靶点作用的特点,我们选择基因芯片倍数法筛选差异基因的方法,对其进行研究.基因芯片结果共筛选出 1867 个差异基因,其中,表达上调的有 1436 个基因,基因表达下调的有 931 个基因.
对上调差异基因进行显着性功能分析,结果发现疏肝益肾方参与血液凝固及蛋白转运等113 项过程,对下调的差异基因进行显着性功能分析,结果发现疏肝益肾方参与免疫应答及细胞凋亡的调控等 85 项过程; 而对上调差异基因进行 Pathway 分析,发现疏肝益肾方参与细胞周期调节以及核苷酸切除修复等 27项过程; 而对下调差异基因进行 Pathway 分析,发现疏肝益肾方参与 MAPK signaling pathway、VEGF sig-naling pathway 等 21 条通路的调节.
4 讨 论
乳腺癌内分泌治疗耐药性的发生,严重影响着乳腺癌治疗的远期疗效.因此探讨乳腺癌内分泌治疗耐药的相关机制和延迟/逆转乳腺癌内分泌治疗耐药的有效方法将具有重要的现实意义.
大量临床前研究表明: 信号转导抑制剂与内分泌药物联合使用可延迟或逆转耐药的发生,故而耐药逆转剂联合内分泌治疗将会成为未来治疗的方向[4].很多靶向药相继开发进入临床前研究,但在实际临床中并未取得预想的效果.究其原因,主要是一: 耐药的靶点、通路、网络盘根错节,患者个体差异,非一两个靶向药的联合能解决所有问题,而多靶点联合在实际操作因其昂贵的价格和难以估计的副反应使可行性不强; 二: 耐药通路、靶点仍未全部清楚,需进一步探索.
目前大量研究发现 MAPK 信号转导通路与乳腺癌耐药有一定的关系,其作用的机制可能是调控与耐药相关的基因和蛋白表达,使其通过对该通路进行干预,提高肿瘤治疗敏感性,从而逆转耐药.如Nguyen TV[5]等发现作用 β1 整合素及其下游效应器JNK 能够抑制索拉非尼在三阴乳腺癌中耐药性的发生.胡会永等[6]发现黄荆子的乙酸乙酯提取物 EVN-50 能够抑制 MCF-7 和 MCF-7 TAM-R 细胞株的生长并诱导细胞凋亡,其作用机制可能与 AKT 和MAPK 信号通路的下调相关.马小俞等[7]研究发现三苯氧胺耐药细胞有较高的自噬水平,MAPK 信号通路参与了三苯氧胺耐药.曾少波等[8]以 P38MAPK特异性抑制剂处理乳腺癌耐药细胞 MCF-7/ADM 后,发现 P38MAPK 信号转导途径与乳腺癌耐药密切相关,其机制可能为 P38MAPK 保护人乳腺癌耐药细胞逃避细胞凋亡.本实验采用疏肝益肾方作用乳腺癌TAM-R 细胞,发现 MAPK 信号通路的下调,这可能是其作用机制之一.
此外,VEGF 是刺激血管生成的因子中最具有代表性的细胞因子,影响着乳腺癌的侵袭、转移等进程,同时与乳腺癌耐药性的关系密切.宋玉仙等[9]研究表明,灵芝孢子油抑制人乳腺癌 MCF-7 细胞增殖和迁移,促进细胞调亡的作用机制可能与下调VEGF 和 Be 1 -2 / Bax 的比值有关.Soo Jin Oh 等[10]研究发现,TAM 耐药乳腺癌细胞 MCF-7 TAM-R 的耐药机制可能和 VEGF 的生成增加导致血管生成增加有关,而槲皮素通过抑制 MCF-7 TAM-R 细胞 VEGF的升高和 PIN1 ( 肽脯氨酰异构酶) 的表达,可能成为治疗 TAM 耐药乳腺癌的有效药物; 进一步研究发现: PIN1 是 VEGF 介导的血管生成的主要调节因子,Kim J[11]报道了山葡萄提取的化合物之一的去氢黄柏苷 G 可以阻断 MCF-7 TAM-R 细胞中 PIN1 介导的VEGF 基因的转录,从而提示去氢黄柏苷 G 治疗TAM 耐药乳腺癌的治疗潜力.我们实验发现,疏肝益肾方作用 TAM-R 耐药细胞后,VEGF 通路的表达下降,提示 VEGF 通路可能是疏肝益肾方逆转耐药作用的另一机制之一.
中药具有毒性小、安全有效、多靶点、药理作用广泛等优势,在逆转乳腺癌内分泌治疗耐药的研究中正受到越来越广泛的关注.我们课题组前期临床实践证明疏肝益肾方联合内分泌治疗可以提高内分泌治疗的疗效,推迟进行化疗的时间,减轻潮热、骨痛等副反应,分层显示其使最易耐药的 LuminalB( ER+/PR+,HER2+) 型乳腺癌患者无进展生存期延长[12].实验结果证实: 疏肝益肾方对他莫昔芬耐药乳腺癌 MCF-7 TAM-R 细胞有抑制增殖的作用,其作用机制的发生可能与抑制 MAPK 通路、VEGF 通路等通路的表达有关.但因逆转耐药机制的复杂性及中医药的多靶点的作用特点,疏肝益肾方抑制MAPK 通路、VEGF 通路的机制需进一步验证.
参考文献
[1] Siegel R,Naishadham D,Jemal A. Cancer statistics,2012[J]. CA Cancer J Clin,2012,62: 10 ~29
[2] 李仪奎. 中药药理实验方法学 [M]. 上海: 上海科学技术出版社,2006: 575
[3] 李仪奎,吴健宇. 血清药理实验中采血时间的通法方案[J]. 中国药理学通报,1999,( 06) : 93 ~94
[4] Schiavon G,Tomini G. Hormone-biological therapy in breastcancer: preclinical evidences,clinical studies and future directions [J].Curr Cancer Drug Target,2010,10 ( 1) : 3 ~ 18
[5] Nguyen TV,Sleiman M,Moriarty T,et al. Sorafenib resist-ance and JNK signaling in carcinoma during extracellular matrix stiffening[J]. Biomaterials,Available online,2014 ( 4) : 13
[6] 胡会永,周俊,万芳,等. Evn 对人乳腺癌 MCF-7 耐三苯氧胺细胞株生长和凋亡的影响 [J]. 浙江大学学报 ( 医学版) ,2012,41 ( 5) : 498 ~ 505
[7] 马小俞,刘哲斌,喻三见,等. 三苯氧胺诱导人乳腺癌MCF-7 细胞株耐药及自噬的关系研究 [J]. 中国癌症杂志,2011,21 ( 6) : 421 ~ 425
[8] 曾少波,兰明银,菅志远,等. 乳腺癌细胞耐药过程中活性与细胞凋亡的关系 [J]. 中华乳腺病杂志: 电子版,2009,3 ( 1) :46 ~ 52
[9] 宋玉仙,窦环,刘贤钦,等. 灵芝孢子油对 MCF-7 细胞凋亡及迁移的影响 [J]. 中医药信息,2011 ( 02) : 91 ~94
[10] Oh S J,Kim O,Lec J S,et al. Inhibition of angiogencsi sby quercclin in lamoxi fcn - rosistanl breast canccr cells [J]. Food andChemical Toxicology,2010,48 ( 11) : 3227 ~ 3234
[11] Kim J,Kim M R,Kim O,ct al. Amurensin G inhibits an-giogenesis and tumor growth of tamoxi fen-resistant breast cancer via Pinl in-hibition [J]. Food and Chemical Toxicology,2012
[12] 卢雯平,姜翠红,李向上. 疏肝益肾方治疗 226 例激素依赖性乳腺癌的前瞻性研究 [J]. 国际中医中药杂志,2011,33( 5) : 389 ~393
林丽珠教授是广州中医药大学第一附属医院大肿瘤科主任,博士研究生导师。林教授认为,邪热犯肺、肝郁痰凝是鼻咽癌的主要病机,因此治疗应从肺、肝论治,采用宣肺化痰、疏肝理气的治疗原则,临床上取得了满意的疗效。兹介绍林师经验如下。1病机首责邪热犯...
电磁场由相互依存的电磁和磁场的总和构成的一种物理...
肺癌已成为危害生命健康的主要疾病之一,其发病率与死亡率逐年上升.2012年美国死于肺癌人数约16.0万,新增肺癌患者约22.6万.在我国城市中,肺癌死亡人数由原来的第4位上升为第1位,农村上升最快的死亡人数也是肺癌患者.调查显示在过去30年间,肺癌死亡率在我...