称取 10. 0 g 硅胶置于 250 mL 圆底烧瓶中,加入 100 mL 20% (体积分数)盐酸,超声分散均匀,于110 ℃ 油浴中回流 8 h.水洗至中性,用乙醇和丙酮各洗 3 次,于 120 ℃真空干燥。取 3. 0 g 活化硅胶置于圆底烧瓶中,加 50 mL 无水甲苯,超声分散均匀。在 N2保护下缓慢滴加 5. 20 mL 3-氨基丙基三乙氧基硅烷,于110 ℃反应24 h.用甲苯、丙酮各洗3 次,于 60 ℃ 真空干燥,即得到 Silica-NH2.
1.2.2 2-溴异丁酰溴氨丙基硅胶(Silica-Br)的制备。
冰浴条件下,将 3. 0 g 氨丙基硅胶分散于 30mL 无水四氢呋喃中,搅拌 1 h,加入 2. 3 mL 三乙胺,再逐滴加入 1. 5 mL 2-溴异丁酰溴,混合物在0 ℃ 下搅拌 30 min,室温反应 24 h.用四氢呋喃、甲醇和水依次洗涤,于 60 ℃真空干燥,即得到 Silica-Br.
1.2.3 釆用 SI-ATRP 在硅胶内表面接枝甲基丙烯酸十八烷基酯。
圆底烧瓶中加入 3. 0 g 溴代硅胶作为引发剂,加入 143 mg CuBr 和 312 mg 2,2-联吡啶。另一圆底烧瓶中加 20 mL 无水甲苯和 20 mL 甲基丙烯酸十八烷基酯,采用真空惰性气体操作管线装置,充氮除氧 30 min,在 N2保护下于 60 ℃反应 24 h,分别用异丙醇、二次蒸馏水、0. 2 mol/ L 乙二胺四乙酸二钠水溶液、水和乙醇洗涤,于 60 ℃真空干燥,即得到Silica-Br-C18.
1.2.4 釆用 SI-ATRP 在硅胶外表面接枝 GMA 链。
圆底烧瓶中加入 3. 0 g 接枝 C18的溴代引发剂硅胶、0. 40 g CuBr 和 1. 28 g 2,2-联吡啶。另一圆底烧瓶加入 100 mL 异丙醇和 10 mL GMA,超声分散均匀。采用真空惰性气体操作管线装置,充氮除氧 30 min.在 N2保护下于 40 ℃反应 24 h,通入空气终止反应,依次用异丙醇、甲醇、水、0. 2 mol/ L 乙二胺四乙酸二钠水溶液、水和丙酮洗涤,于 60 ℃真空干燥,即得到 Silica-Br-C18-GMA.
1.2.5 GMA 链水解。
所得产物(Silica-Br-C18-GMA)置于 100 mL 圆底烧瓶中,加入 60 mL 0. 1 mol/ L 硫酸,60 ℃水解12 h,反应完毕后,水洗至中性,于 40 ℃ 真空干燥,即得到新型反相限进材料(Silica-Br-C18-GMMA)。
1.3 Silica-Br-C18-GMMA 限进行为的评价。
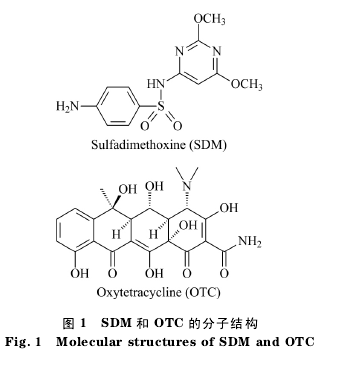
为体现新型反相限进材料的限进特点,选择BSA 作为排阻蛋白质大分子模型来评价其外表面的亲水性特点。BSA 是相对分子质量约为 68 kDa的疏水性蛋白质,经常用于模拟生物环境实验。选择结构不同的 SDM 和 OTC 作为小分子模型(见图1)来评价其内表面十八烷基链的萃取能力,通过静态吸附实验研究该新型反相限进材料对小分子的萃取能力。
1.3.1 Silica-Br-C18-GMMA 对 BSA 的排阻。
在 6 mL 固相萃取(SPE)小柱内分别填充 200mg Silica-Br-C18-GMMA 和 200 mg Silica-Br-C18,使柱床体积为 2 mL,柱上下两端用多孔性的聚四氟乙烯筛板,使小柱装填均匀且空隙较少。装填完成后,用 1 mL 甲醇和 3 mL 水平衡小柱,注入 3 mL 1g / L BSA 溶液,收集流出液,用紫外分光光度计在280 nm 处检测不保留的 BSA 的吸光度。再用 2mL 水淋洗,用 2 mL 甲醇洗净小柱。