摘 要: 本文以高磷鲕状赤铁矿为原料, 通过探讨焙烧条件、酸浸条件以及水解沉淀方法、煅烧条件等对制备氧化铁红的影响, 推荐湿法制备氧化铁红的生产工艺。试验表明, 高磷鲕状赤铁矿通过还原焙烧得到金属Fe精矿更容易酸浸, 得到的FeSO4溶液经过除杂、水解沉淀、洗涤、干燥煅烧等工序后, 可得到纯度为99.5%的氧化铁红, 达到开发利用高磷鲕状赤铁矿的目的。
关键词: 高磷鲕状赤铁矿; 氧化铁红; 焙烧; 酸浸; 沉淀;

Abstract: In the paper, by using the high phosphorus oolitic hematite as the raw materials, the influence of roasting, acid leaching condition, hydrolysis precipitation method and calcination condition one the preparation of iron oxide red were discussed, recommending wet production technology for preparation of iron oxide red. The results showed that the Fe concentrate was more easily obtained by reductive roasting of the high phosphorus oolitic hematite. The produced concentration can obtain the purity of 99.5% of iron oxide red by the process of removing impurity, hydrolysis precipitation, washing, drying and calcining, achieving the goal of development and utilization of high phosphorus oolitic hematite.
Keyword: High phosphorus oolitic hematite; Iron oxide red; Roasting; Acid leaching; Precipitation;
高磷鲕状赤铁矿是我国一种重要的沉积型铁矿资源, 总储量约有37.2亿t[1], 远景储存量达到100亿t以上[2]。高磷鲕状赤铁矿矿物组成复杂、杂质含量高、铁矿物嵌布粒度较细、易泥化, 特别是大部分铁矿物与磷矿物致密伴生难以分离, 严重影响后续钢铁冶炼的质量[3]。
试验以高磷鲕状赤铁矿为原料进行研究, 尝试避开高磷鲕状矿的选矿难点, 制备纯度较高的氧化铁红, 达到开发利用高磷鲕状赤铁矿的目的。
1、 试验部分
1.1、 原矿分析
试验原料来至鄂西某高磷鲕状赤铁矿, 样品进行多元素分析结果见表1。
表1 矿样的多元素分析结果/%Table 1 Analysis results of multi-elements of ore samples
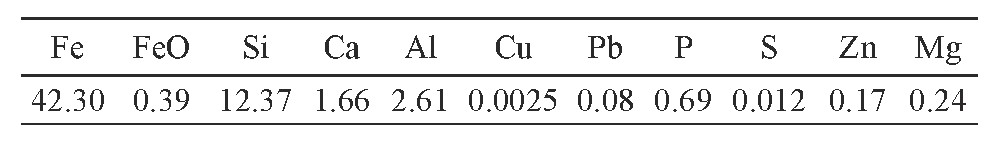
从表1可以看出, 原料主要成分主要是铁元素, 主要杂质为Si, 还有较高的Al、Ca、P和少量的Zn、Mg。
1.2、 试验原理和试验方案
铁及铁氧化物与硫酸常温 (25℃) 下浸出反应的标准吉布斯自由能为下:

从热力学的角度来看, 铁氧化物价态越低越容易与酸反应, 且除氧化铁外, 在常温下都能自发进行。故先将三氧化二铁还原成低价态的铁氧化物有利于浸出反应的进行;酸浸后溶液中的铁离子通过氨水调pH水解沉淀, 氢氧化物沉淀时, 几种金属离子Mn+的平衡pH值 (25℃) 见表2。
表2 几种主要金属离子的平衡p H值Table 2 PH balance value of main metal ions of several acid leaching solution

从表2中可知, Fe3+水解沉淀时, 会有部分Al3+也会水解沉淀, 其他离子不会沉淀;而Fe2+沉淀时, Al3+不会沉淀, 其他离子都会沉淀。Fe3+水解沉淀时的pH值小于Fe2+水解沉淀时的pH值, 即Fe3+比Fe2+更容易水解沉淀。影响Fe3+沉淀物纯度的主要离子为Al3+, 可使溶液中的铁先以二价存在, 调pH值为5~6, 使Al沉淀出来, 然后过滤除去, 再加氧化剂使Fe3+全部氧化成Fe2+, 最后调pH为4~5, 即可得到杂质较少的铁沉淀物。沉淀通过滤、洗涤、干燥、煅烧即可得到氧化铁红, 具体流程如图1。
图1 铁红制备流程Fig.1 Flow chart of the preparation of iron oxide
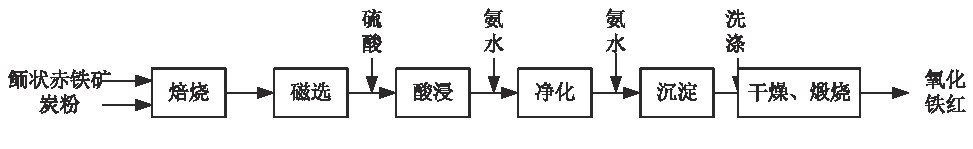
2、 结果与讨论
2.1、 原矿处理
高磷鲕状赤铁矿品位较低, 杂质含量较高, 利用焙烧-磁选进行抛尾, 除去部分杂质, 减少后续酸浸成本。焙烧所用炭粉含碳为47.60%。原矿在焙烧温度800℃、炭矿比0.3、焙烧时间1 h时磁化焙烧效果最好;在直接还原温度1000℃、炭矿比0.5、焙烧时间3h时直接还原效果最好。对两种焙烧矿, 在入选粒度-74μm90%、磁场强度1.3T时磁选得到磁选精矿。对磁选精矿进行多元素分析和XRD分析, 分别见表3, 图2。
表3 两种条件焙烧产物磁选后铁精矿分析结果%Table 3 Analysis results of iron concentrate after roasting magnetic separation in the two kinds of conditions
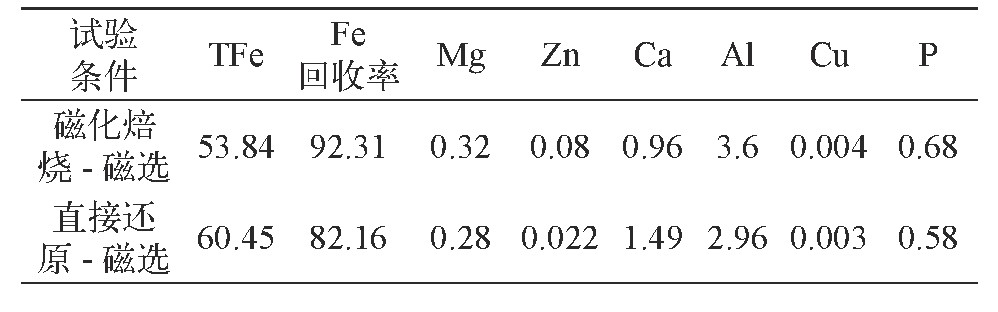
从表3可以看出, 直接还原-磁选得到的铁精矿与磁化焙烧-磁选相比, 铁品位较高, 回收率较低, 除了Ca含量稍高外, Mg、Al、P等杂质含量都较低。
图2 两种铁精矿的XRD分析结果Fig.2 XRD analysis results of two kinds of iron concentrate
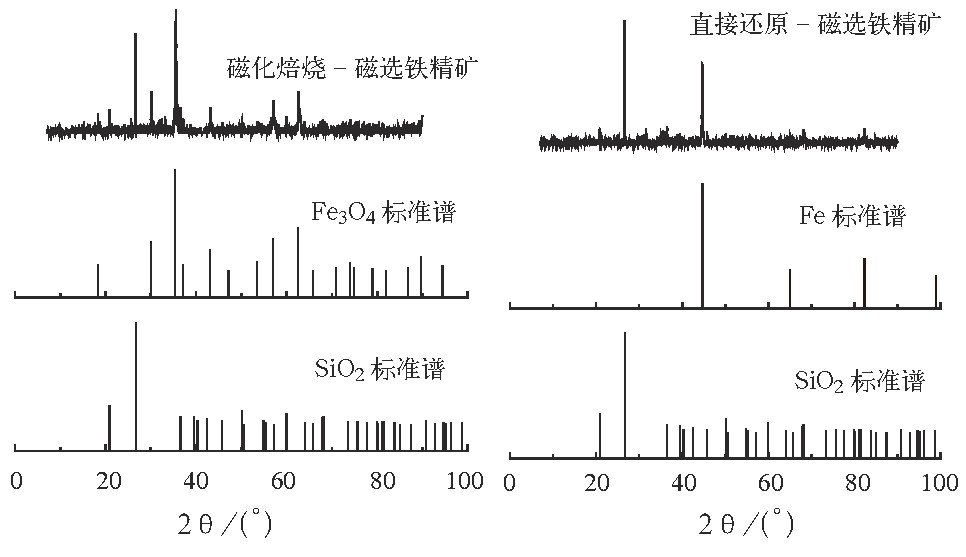
从图2分析结果可知, 磁化焙烧-磁选精矿中的铁是以四氧化三铁的形式存在的, 直接还原焙烧-磁选中的铁是以金属铁的形式存在的, 两种铁精矿中的主要杂质都是二氧化硅。
2.2、 酸浸试验
对Fe3O4精矿和Fe精矿进行酸浸试验, 试验用酸为硫酸。影响酸浸的主要原因有酸的浓度、液固比、酸浸温度、酸浸时间、搅拌速度、铁精矿的细度等。试验表明两种条件下的铁精矿较佳浸出条件见表4。
图2 两种铁精矿的XRD分析结果Fig.2 XRD analysis results of two kinds of iron concentrate
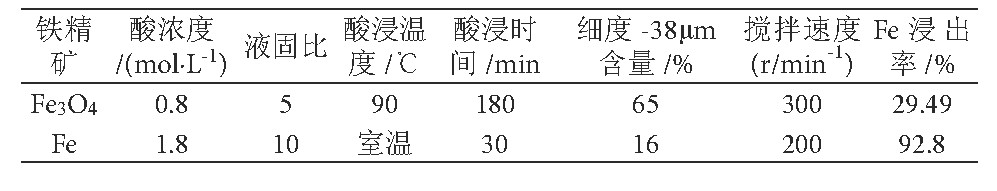
酸浸温度和精矿细度对Fe3O4的浸出有较大影响, 对Fe的影响较小。虽然提高浸出温度有利于Fe精矿的浸出, 但浸出率提高幅度不大, 且升温会加大能耗, 故推荐在常温下进行。适当的减小细度也有利于Fe精矿的浸出, 但浸出率提高的幅度也不是很大, 而铁精矿磨细也会加大成本, 故推荐Fe精矿不磨矿, 直接浸出。从表4结果可看出, Fe精矿浸出所需的时间远远低于Fe3O4精矿的浸出时间, Fe精矿的铁浸出率要远远高于Fe3O4精矿的铁浸出率, 说明Fe3O4精矿很难浸出。Fe3O4精矿难以浸出的原因可能是鲕状矿中铁氧化物经高温煅烧, 使其铁氧化物结构致密而活性降低, 与硫酸反应的速度很慢[4]。由表3、4可知, Fe精矿金属杂质比Fe3O4精矿少;Fe的酸浸效果远远好于Fe3O4, Fe的酸浸在室温下就有较高回收率, 不需要磨矿, 且酸浸速度快, 即Fe精矿的酸浸条件更好。综合考虑推荐的焙烧方式为还原焙烧, 即将原矿中的铁矿物氧化为金属铁。
2.3、 酸浸液的净化与沉淀
为了便于试验, 将Fe精矿在最佳酸浸条件下得到的酸浸液即FeSO4溶液配成铁离子浓度为0.4mol/L左右的溶液。动力学研究表明, Fe2+在空气中氧化时, 氧化速度随pH值的升高而升高, 当pH<1时, 氧化速度很慢[5]。当配成铁离子浓度为0.4 mol/L左右的溶液时, 测得溶液的pH值为0.56, 并且配好的溶液马上密封保存, 溶液中Fe3+含量很少。配好的FeSO4溶液中主要离子浓度见表5。
表5 Fe SO4溶液中主要的离子浓度Table 5 The main ion concentration in FeSO4 solution

从表5可知, 溶液中主要的杂质离子为Al3+、Mg2+、Ca2+和Si。在硫酸亚铁溶液Si一般是以硅酸胶体形式存在, 非常细微。
2.3.1、 酸浸液的净化
酸浸后的溶液中还有一些杂质, 如果不除去会影响最终铁红产品的纯度。为考察除铝效果, 进行除铝得到铁红的对比试验, 试验方法如下:
条件a:取100 ml溶液加过量H2O2 (1 mol/L H2O225 ml) , 将Fe2+氧化成Fe3+, 然后加氨水调pH值为3.5得到棕黄沉淀;
条件b:取100 ml溶液先调pH值为5.5, 得到淡黄沉淀, 过滤后得到的橙黄滤液加过量H2O2氧化, 最后调pH值到3.5得到棕黄沉淀;
两种条件下的沉淀在800℃煅烧1 h, 得到的铁红分析结果见表6。
表6 铁红分析结果/%Table 6 Results of iron oxide red
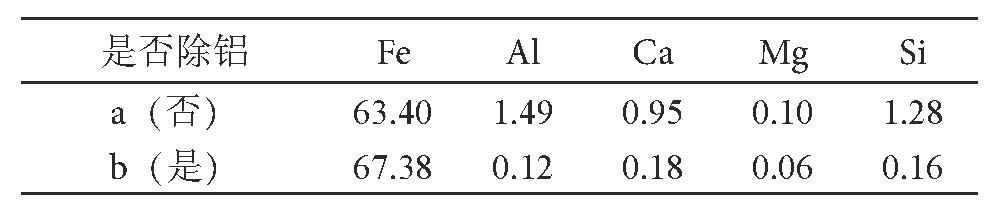
从表7试验结果可以看出, 溶液经除铝处理之后得到的铁红纯度较高, 铁红中的Al明显减少, 且Mg、Ca等杂质元素也相应减少。除铝试验得到的沉淀物 (铝渣) 分析结果见表7。
表7 铝渣分析结果Table 7 Analysis results of aluminum slag
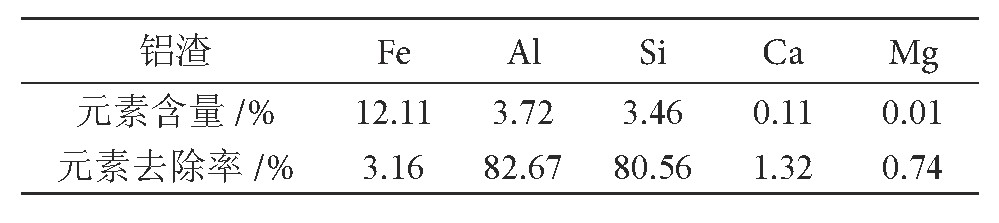
由表7可知, 除铝的同时可以除去大量的Si, 还会少量地除去Mg、Ca等杂质, 也带走了少量铁。这是因为在调溶液pH值除铝的过程中, 形成的Al (OH) 3胶体沉淀具有较强的吸附性, 会吸附其他离子, 且Al (OH) 3胶体沉淀在溶液中一般带正电, 会优先捕集吸附带负电的硅酸溶胶。因此除铝的过程会除去大部分硅和一些杂质金属。虽然除铝的过程中会带走少量的Fe, 但可以除去大量杂质, 大幅度提高铁红的品位, 因此水解沉淀前进行除铝是很有必要的。
2.3.2、 中和沉淀
考虑到将Fe2+氧化成Fe3+, 使用的氧化剂不能带入额外的杂质进入到溶液中, 而且要使Fe2+完全氧化成Fe3+, 氧化剂可用O2或空气、H2O2等。为方便试验的进行, 在试验过程中采用H2O2 (生产中可采用O2或空气) 。沉淀的反应机理如下:
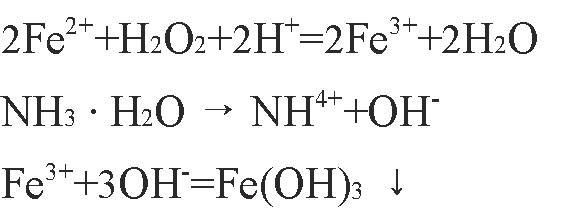
试验发现FeSO4溶液的初始浓度越低, 越有利于得到较为纯净的沉淀。然而, 单纯依靠稀释溶液的浓度是不可取的, 这会严重降低沉淀过程的生产效率, 变相提高了生产成本。实践过程中, 先保持铁离子为Fe2+, 调pH值到Fe3+完全水解沉淀的范围3.5~5, 然后缓慢加氧化剂将Fe2+氧化成Fe3+, 使Fe3+始终保持低浓度。
通过沉淀的反应机理可看出, 随着水解沉淀的不断进行, 溶液中的H+不断增多即pH值不断下降。调pH值为4后进行试验, 反应过程中不再添加氨水;随着沉淀反应的进行, 当反应10 min后溶液中的pH值降为2.56, 溶液中的沉淀也很少。因此, 在试验过程中要不断添加氨水, 使溶液中的pH值始终保持在4。
在中和沉淀过程中, 温度是影响水解沉淀的一个重要因素。升温有利于得到杂质含量少的沉淀:一方面吸附使放热过程, 升温不利于沉淀表面杂质的吸附;另一方面升温有利得到粗颗粒。为研究温度对沉淀的影响, 在室温 (25℃) 和90℃两种温度下, 进行沉淀温度对比试验, 得到的铁红产品分析结果见表8。
表8 温度对水解沉淀的影响/%Table 8 Effect of temperature on hydrolysis precipitation
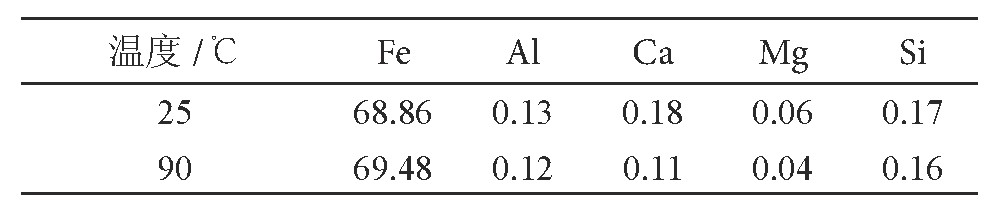
由表8可知, 升温有利于得到较纯铁红。室温下得到的沉淀为棕黄胶状物, 在90℃得到的沉淀物为橙黄晶体, 更容易过滤。
2.3.3、 沉淀的洗涤
水解沉淀得到的沉淀物一般都会吸附溶液中的粒子, 从而影响沉淀物的纯度。沉淀物的洗涤试验结果见表9。
表9 沉淀物洗涤试验结果Table 9 Results of sediment washing test
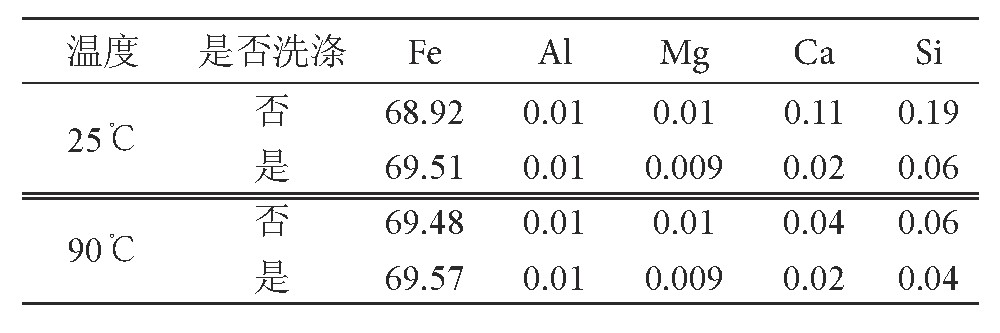
试验证明, 沉淀物的洗涤可以小幅度提高铁红产品的纯度, 且晶体沉淀物 (如90℃) 通过洗涤铁红纯度提高的幅度要小于胶体沉淀物通过洗涤后铁红提高的幅度, 这也证明了胶体沉淀吸附了大量杂质。通过洗涤胶体沉淀物与晶体沉淀物铁品位相差不大, 在不考虑固液分离的情况下推荐室温下进行水解沉淀试验。
2.4、 沉淀煅烧
通过试验可确定沉淀物的煅烧温度为800℃, 锻烧时间1 h, 可得到不含结晶水的氧化铁红。最终氧化铁红产品的分析结果见表10。
表1 0 最终铁红产品分析结果/%Table 10 Analysis results of the final iron oxide product

3、 结论
(1) 高磷鲕状赤铁矿制备铁红的方法为:先将铁矿物还原焙烧为Fe, 通过磨矿磁选抛掉大量尾矿;磁选精矿在硫酸浓度为1.8 mol/L、液固比10的条件下, 室温搅拌浸出30 min, 过滤得到FeSO4溶液;FeSO4溶液通过氨水调pH值除去溶液中的杂质, 除去杂质的滤液在室温下调pH值为4, 缓慢加入H2O2氧化, 得到棕黄色沉淀, 沉淀洗涤干燥后在温度为800℃煅烧1 h, 即可得到较纯净的氧化铁红。
(2) Fe精矿的浸出效果远远好于Fe3O2精矿, 且得到的FeSO2溶液有利于后续的溶液净化和水解沉淀过程。
(3) 中和试验前FeSO2溶液的除杂, 以及中和试验后得到沉淀的洗涤都有利于得到纯净的氧化铁红。
(4) 试验证明, 以高磷鲕状赤铁矿为原料可以制备出纯度为99.5%的氧化铁红。
参考文献:
[1]孙永升, 韩跃新, 高鹏, 等.高磷鲕状赤铁矿石工艺矿物学研究[J].东北大学学报:自然科学版, 2013, 34 (12) :1773-1777.
[2]邵广全, 向松林, 叶德全.鄂西高磷鲕状赤铁矿资源开发应用技术选矿工业试验[C]//全国矿产资源综合利用学术会议, 2013.
[3]陆俊.超细氧化铁红的制备[D].杭州:浙江大学, 2006.
[4]郑雅杰, 陈白珍, 龚竹青, 等.硫铁矿烧渣的熟化及机理[J].中国有色金属学报, 2001, 11 (1) :144-147.
[5]李洪桂.湿法冶金学[M].长沙:中南大学出版社, 2002.
铬渣是焙烧生产铬盐的过程中产生的一种固体有毒废弃物,主要成份为铬、铁、铝、钙、镁、硅的氧化物或碱性复合盐,铬化合物对人体的危害与其价态及水溶性有关。金属铬及三价铬对人体无害;六价铬毒性最强主要以四水铬酸钠、铬酸钙、铬铝酸钙和碱式铬酸铁等形...