����ժ Ҫ�����������ʻ�����Ϊһ�ֲ�����ķ��������,����༲����˥��������ء��йص������ʻ����ĸ����о���������ͷ�ȡ��͵���Ч�ʼ���ѧ��Բ��ȶ��Զ���չ�������������ĵ�������ѧ���������Ľ���,ʹ�������ʻ����Ĺ�ģ���о���Ϊ����,����Ϊ�������ʻ�������ص���ͨ·�о��ṩ������֧�š������������˵������ʻ����ĸ��;������ⷽʽ,���ص�����˵�����ѧ����Ӧ���ڵ������ʻ��������Ľ�չ��
�����ؼ��ʣ�������Ӧ��; �������ʻ���; ��������ѧ;
����Abstract����Protein carbonylation,an irreversible post-translational modification,is closely related to many diseases and aging.The analysis of protein carbonylation is a challenge due to its low abundance,low ionization efficiency and relative chemical instability.Advances in mass spectrometry-based proteomics have made it possible to conduct large-scale studies on protein carbonylation,providing in turn the data support for the study of related regulatory pathways of protein carbonylation.The concept,pathways and analysis methods of protein carbonylation are presented in this review,and the advances in proteomic analysis of protein carbonylation are highlighted.
����Keyword����oxidative stress; protein carbonylation; proteomics;
����1�� ����Ӧ���뵰�����ʻ���
���������������������������벻������,������ߵ��������������л�ȹ����������[1,2]�����������ڴ�л�м��塢ø�ͷ��������²���������(Reactive oxygen species,ROS),�����������������¶�ϸ����л�ĵ��ط�����������Ҫ������[3]��Ȼ��,��������ROS������������Դ�Կ����������Ļ�������,���������Ϳ�������֮��IJ�ƽ�ⱻ����ʱ,������������ԭ�ź�����ƻ��Ƶ��ƻ���/���������[4],��������Ӧ��ЧӦ(Oxidative stress,OS),��������֬�ʡ�DNA/RNA�͵����ʵ���Ҫ�������е��ߵĹ������𡣵���������Ӧ������ʱ,���Ե����ʡ�DNA��RNA�����������ɲ���������,����ɵ���ø�����ø�彵���������˵����ʵ���������,ʹϸ����������,�������ϸ������[5,6]������Ӧ���쳣��˥�Ϲ����Լ����ּ����ķ����������,������������Ӳ�������������������ĺ�Ĭ��������ɭ�����������Լ���[7]��
�����������ʻ���(Protein carbonylation,PCO)��ָ������������Ӧ��״̬�²���ȩ��ͪ���������Ȼ����ʻ�������[8]��PCO��Σ�������ĵ����ʷ��������֮һ,����ɵ����ʽṹ�IJ��ȶ����ܵIJ���������[9]���йص������ʻ������о�ʼ��20����80�����,���������������о�Ժ(National Institutes of Health,NIH)��Stadtmanʵ���ҿ���[10]���������ʻ�������Ϊ����Ӧ���������־��,��ϸ������֯������˥���е������ܵ��ر��ע[11]��Levine��Stadtman����������ʻ���ˮƽ�������������������,�Դ�֧��ϸ����������ˮƽ��˥�ϵ����ɻ�(����Ӧ��)����[12,13,14,15],�ʵ������ʻ�������˥����ص���Ҫ��ѡ�����־�ͬʱ,�������ʻ�������ص�����,����Ӱ������ź�ת������,��ɼ�����ص����ʹ��ܵIJ���������[16]�����,�ʻ������ڵ����ʹ��ܵķ��Ӿ���������Ҫ�ĵ�������,ʵ�ֵ������ʻ����ı���,�����ṩ����Ӧ����ص�����������,Ϊ��ؼ����ķ��ӻ����о��ṩ��Ҫ��Ϣ[17]��

����2 ���������ʻ���;��
�����������ʻ������ڳ���35����ʽ[18],�����������ʽ��Ҫ��Ϊ����4��[10](ͼ1)��
����ͼ1 �������ʻ�������Ҫ;��
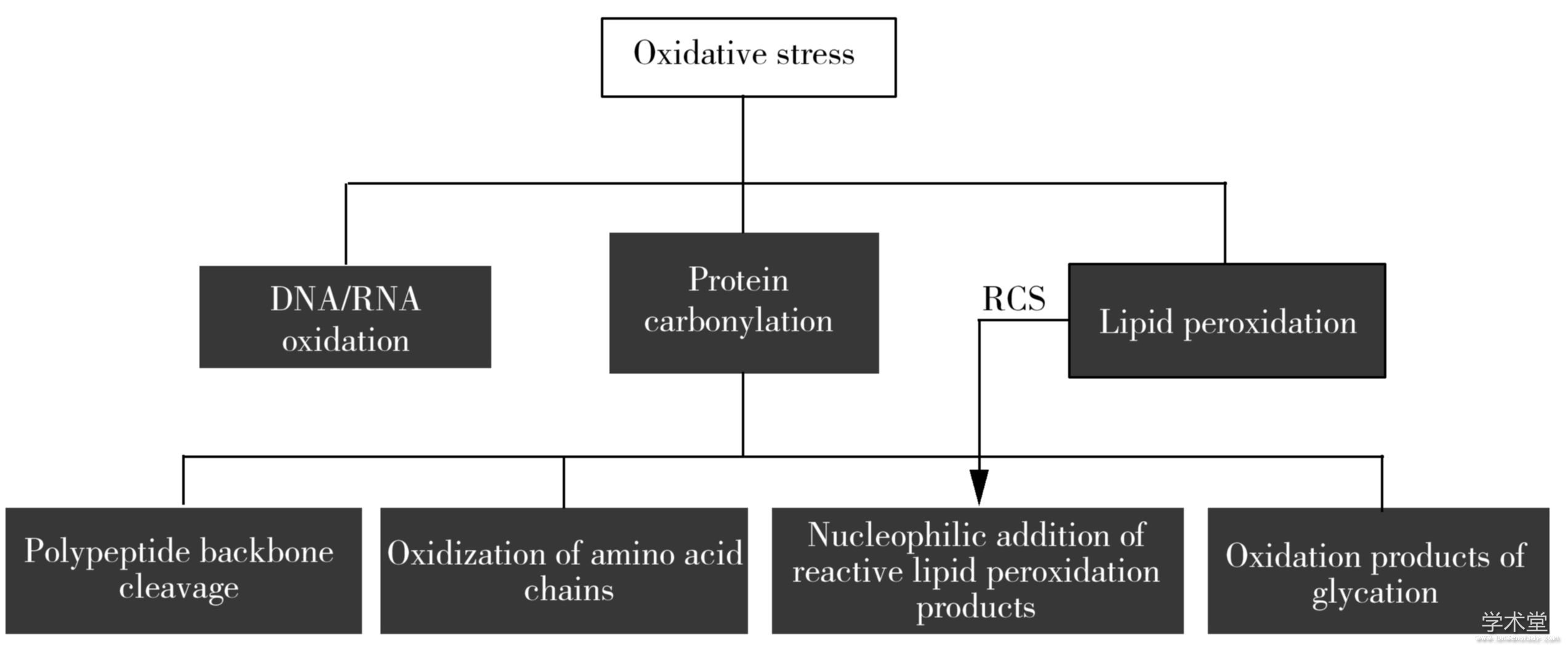
����Fig.1 Main protein carbonylation pathways
����2.1�� �����ʡ����������Ǽܵ��ѽ�
���������ʵĶ��ĹǼ��а������α-̼ԭ�ӿɱ�ROS����,�γ����������ɻ�,�����α-�������������;���ѽ⡣ǰ�ߵļ����ѷ��������ɻ���ʼλ���N-ĩ��һ��,ʹ���Ե�����N-ĩ�˲��ֵĶ���Ƭ�δ���C-ĩ������,�����Ե�����C-ĩ�˲��ֵĶ���N-ĩ�˾���N-α-ͪ����;���ߵĹǼ��ѽ���α-̼��ʼλ���C-ĩ�˲�ļ���������,ʹ���Ե�����N-ĩ�˲��ֵ��¶��ĵ�C-ĩ���γɶ�����,�����Ե����ʵ�C-ĩ�˲��ֵĶ���N-ĩ�˲��������������š�
����2.2�� �����ʰ��������������
����ROS��ͨ��ֱ�ӹ����հ��ᡢ�����ᡢ�����ᡢ������IJ���,��������ʻ�����������Ϊ��,�ǻ����ɻ��������������C6λ�ö�ȡ��,�γ���̼Ϊ���ĵ����ɻ������ɽ������ӽ���̼���ɻ��ŵ��ӶԺ�,�����������ǰ�,���ͨ���ͷ�������Է�ˮ��ɰ����������ȩ(AAS)�����Ƶ�,�����������ɹȰ����ȩ(GGS),�հ���������2-����-3-ͪ����,�����������õ�GGS��2-������ͪ��
����2.3�� ֬�ʹ���������Ե�����λ��ļӳ�
����ROS��֬�ʵĽ�������֬�ʹ�����(Lipid peroxidation),����α,β-������ȩ����ȩ��ͪȩ�ȱ���Ϊ�����ʻ�����(Reactive carbonyl spices,RCS)�Ĵ�л����(�ֳ�Lipid-derived electrophiles,LDEs,��֬���������Լ�),���ϩȩ(Acrolein,ACR)������ȩ(MDA)��4-�ǻ�-2-��ϩȩ(4-Hydroxy-2-nonenal,HNE)�ȡ���Щ�����ʻ����ʿ���ͨ�����˶��ӳɻ�����ϯ������ʽ�Ӻϵ��˰�����(�����װ��ᡢ�鰱���������)����������ʻ����о�������������ò����ܹ��������Ի�ѧ�źŵĵ��ػ���,���Ҷ�Ŀǰҩ�ﻯѧ�������ŵİ������Ƽ�����������Ҫ�ο���ֵ��
����2.4�� �ǻ�����������
����������ͻ�ԭ��֮�䷢������Ϊ�����·�Ӧ�ķ�ø�ٷ�Ӧ,��һϵ�л�ѧ����֮��,�����ڵ����ʲ�����������ʻ�������֮��,�ǽͽ��м��彵�������С����ȩ��,���Ҷ�ȩ(MG)�����Ҷ�ȩ(MGO)��3-��������ȩͪ(3-DG)Ҳ���ԼӺ��ڵ������ϴӶ���������ʻ���
����3�� �������ʻ����ĸ�����ⷽ��
����Ŀǰ,�������ʻ����ļ����Ͷ���������Ҫ��Ϊ����3��:(1)�ֹ��ȷ���ɫ���ⶨ�ܵ������ʻ�����;(2)���ﻯѧ������ѧ����,������ӡ����ELISA(Enzyme-linked immunosorbent assay ,ø�����������ⶨ��),�ṩ�й����ε����ʻ���ˮƽ��ȫ������Ϣ;(3)��������(MS)���ʻ�����⼼��,���ڼ��������ʵ�����λ���Լ������ʽ�ϵ��ʻ����������Զ���[19]���������������������Ȼ�ܹ��������ȼ���������ε�����,ȴ�����ṩ���ε����������Լ����α����Ļ�ѧ���ʺ�λ�����Ϣ���������ĵ�������ѧ�Ľ���,ʹ�������ʻ����Ĺ�ģ���о���Ϊ����,����Ϊ�������ʻ�������ص���ͨ·�о��ṩ������֧��[19]��Ŀǰ���õĵ�������ѧ������Ҫ��Ϊ������Ӿ���������Ӿ������ϵ(ͼ2)��
����ͼ2 �������ʻ���������ѧ��������
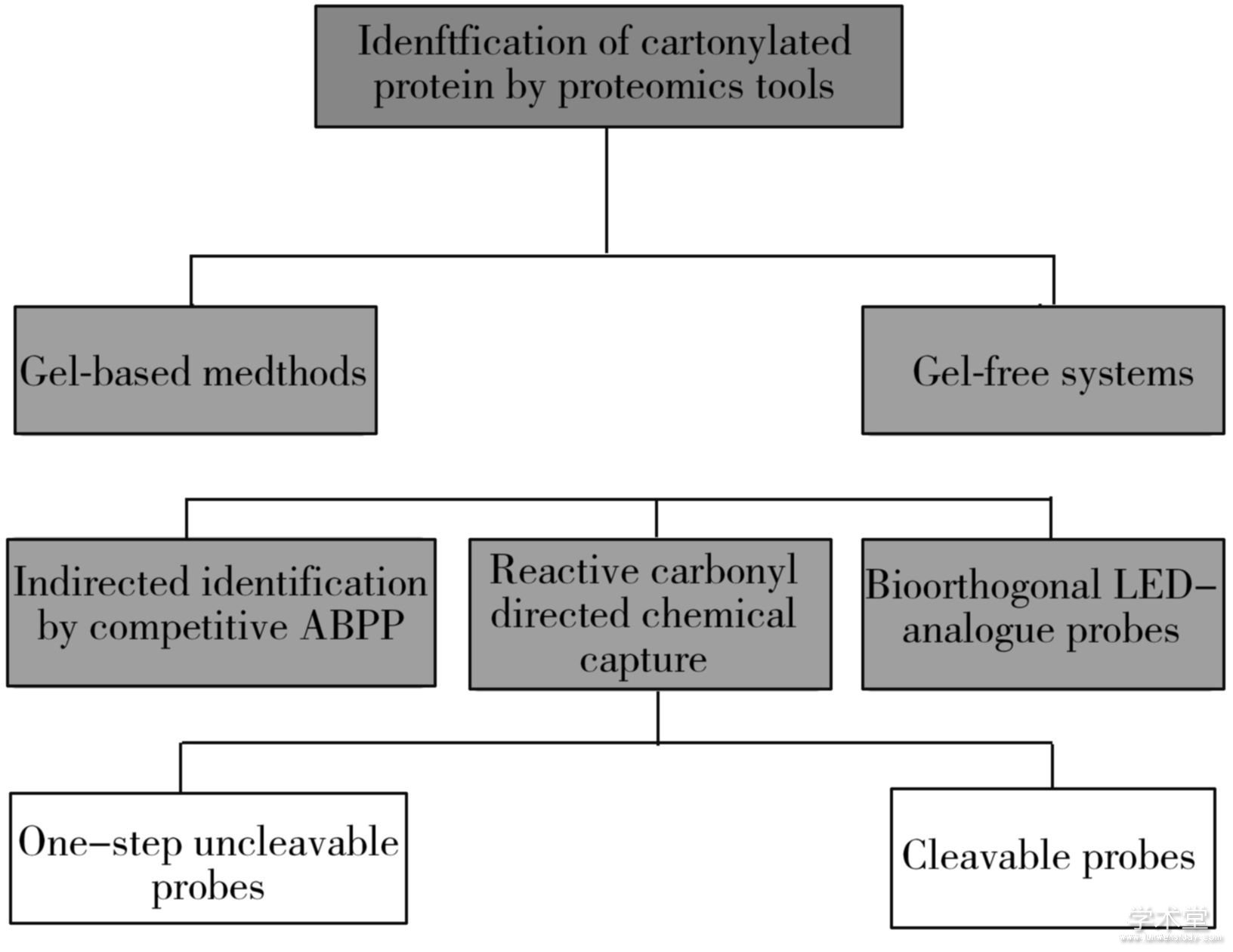
����Fig.2 Proteomics analysis methods of carbonylated protein
����3.1�� ������Ӿ��ϵ
������ά(2D)������Ӿ�ѱ��㷺���ڸ�����Ʒ���ʻ��������ʵļ�����������Է�ȵ͡���ѧ�ȶ��Բȱ���ض���������ѧ����(�����ջ�ӫ��),�ʻ���������ͨ����ֱ�Ӽ��,����Ͷ�����Ҫʹ���ض��Ļ�ѧ̽�����������[15]��
����2,4-����������(2,4-Dintrophenylhydrazide,DNPH)��������ʻ���Ӧ,�γ��ȶ���2,4-����������,�����չ�����365��375 nm�������������շ塣Levine��[20]����ʹ��DNPH,ͨ��DNP(2,4-����������)������360 nm������������ⶨ�ʻ����̶ȡ���һ˼·����չΪ“oxyblot”����Ӧ���ڵ�����ӡ����,������DNP�����ʻ�����Ʒ,��ʹ�ÿ�DNP������м��[21,22],������ͨ������������������������ʻ�������λ����м�����
�������»��ſ���������ʻ���Ӧ�γ���Ӻ���,�京�еIJ��ȶ��ǰ���,�ɱ�������⻯�������Ի�ԭ������,���»�����������ֹ�����(�������ء���ػƶ��պ�������ż���ĸ���ӫ�⻯�����)�������ʻ���Ӧ,���������ػƶ���-�����������ʻ����Կ���ػƶ��տ�����м��,����������-��������������ӫ���ر�ǵ����ؼ�⡣ӫ���������������ӫ��������������Stadtman��[23]������һά�����м���ʻ�;Regnier��[24]���������ػ�������-��������ӫ����(Biotinylation and avidin-fluorescein isothiocyanate,FITC)��Ⱦɫ��,�����˶�ά��Ӿ���ʻ������ļ�ⷽ��,���ù�������̼���Ľ�ĸ���������м�����20���ʻ��������ʡ�2D������Ӿ�����ڸ����������������ڲ�����������ʵļ���,���������Ƚϵ�,�����ͷ�ȵĵ�����,���������Ҳ�������ͨ�����[25]��
����3.2�� ��������Ӿ��ϵ
���������ǵ�������ѧ�����ڼ���������,������PTM(Post-translational modification,���������)��������ͨ�ü�����ʹ�������������������Ѿ���Ϊ�о��������ʻ������������������������ʻ����ĸ����о���������ͷ�ȡ��͵���Ч�ʡ����ܲ�����������Լ�������ڼ���ڵ�����������ķ�Ӧ�ԡ������������֮ǰ,�����ʻ����ĺ͵����ʵĸ�������ͨ���DZ����[26]��
����3.2.1�� ���ھ����Է�Ӧ���Զ��װ����ʻ������εļ�Ӽ���
����֬�ʹ�������������������ε����ʵİ��װ���Ȼ���λ��,����Ӱ�쵰���ʵĹ��ܡ�����ͨ����Ӧ�Ի�ѧ̽����δ�����εİ��װ������λ��,��ϵ����ʶ�����ѧ����,���ʵ������ʻ��������ʵ��P����λ��ļ�����Cravatt��[27]���ھ�����isoTOP-ABPP(Isotopic tandem orthogonal proteolysis-activity-based protein profiling,ͬλ�ش�����������ˮ��-���ڻ��Եĵ�������)����,ʹ��LDE(��������ʻ�����)��DMSO(Dimethylsulfoxide,��������)������������,������Ӧ�Ե�������(Iodoacetamide,IAM)-Ȳ̽����,ͨ��CuI���ĵ�������-Ȳ�����ӳɷ�Ӧ(�����ѧ)���Ͽ��и�ġ�ͬλ�ر�ǵ������ر�ǩ,����ù�����鸻��,����ø��õ�̽�����Ķ�,����LC-MS/MS�����Ͷ������ò����ܹ�ͨ�����װ��ᷴӦ�Ե�������-Ȳ(IA)̽�붨������������LDE���ε�1000������װ���λ�㡣���ڶ��װ����LDE���ο��Ծ����Ե������IA-Ȳ�����,DMSO������(��)��LDE������(��)�ź�֮��Ķ�������ȷ�ط�ӳ�˶��װ���LDE���εij̶ȡ��÷�������LDE�͵��������̽����װ������λ��ľ�������,��Чʵ����LDE��ص����ɸѡ,����ȡ����Ӧ�ĵ���λ����Ϣ��Ȼ��,�÷���ֻ�ܼ�ӻ�ȡLDE�Ե������а��װ���л�������λ����Ϣ,����ȡLDE���鰱�������������λ����Ϣ��
����3.2.2�� ͨ����������LDE-������̽����ض��ʻ������ͽ��м�����
��������ھ������õļ���ʻ�����ⷽ�����,ʵ������λ���ֱ�Ӽ������и��ߵ�������,������Ч���ټ����Ը��š�Marnett��[28]��ƺϳ��˴��е�����Ȳ����4-�ǻ�-2-��ϩȩ(HNE)������,��������뵽RKOϸ��(Human colon adenocarcinomacells,�˽᳦�ٰ�ϸ��)��,ʹRKOϸ���ае��ײ����ʻ�������,�ټ������Ӧ�Ľ���Ȳ����������ŵ�������,���õ����ѧ��Ӧ��������ػ��е���,�������ù�������ʹ����������ù���ؽ�Ϸ������Ե������Լ������ر�ǩӰ������������,Porter��[29]������ʹ���-���·������,������һ�ֿ��ɹ��ѽ�ĵ���-�����ر�ǩ,����ʵ����ù���ز�����HNE-Ȳ��̽��Ӻϵ����ʻ��Ķε��������ͷ�,����֬���������Լ�HNE��4-����-2-��ϩȩ(4-oxo-2-Nonenal,ONE)��Ȳ�������������һϵ�ж����Ӻ������ʵ��[30]���ڴ˻�����,Liebler��[31]������һ����λ��Ϊ���ĵĶ�����ѧ��������ѧ����,����������ڹ���и�������������Լ��н�������ͬλ�ر��,��Ч����˼���λ��Ŀ��Ŷ�,ʵ���˶�Լ400��HNE����λ��Ĵ��ģ��ԭλ��λ�������Լ����Ͷ�����
��������������������ֻ�ܼ����ض����͵��ʻ�������,���ܲ����������������͵��ʻ������ε��ס��ϳ��ض�LDE������̽��ɱ��ϸߡ���������,����,��LDE�Ͻ���Ȳ�������������ܻ�ı����ǵ������ͻ�ѧ����,�������ֻ�Ӱ������һЩ��Ȼ�е�������á�
����3.2.3�� ��������ʻ��Ļ�ѧ��������
����(1)“һ�廯”������̽��
��������ijЩ��ѧ���ſ��Կ��ٶ���ѧ�������Խ�ϻ����ʻ��γ��ȶ��Ĺ��ۼӺ��������,����������������Ϊ̽��,��ʹ�����ؽ��в���,����ʵ���������ʻ�������/�Ķεĸ�Ч����������ʹ����㷺��������������(Biotin hydrazide,BHZ)̽��[32]��
����Yang��[33]��BHZ����Ʒ���ʻ�������Ӧ�����ǰ�,����������⻯�������Ի�ԭ�ǰ��ȶ�����,����ù�����鲶�������ػ�����,����ϴ�ӡ���ԭ���������ա�ø���,ȡø������Һ����LC-MS/MS��⡣���о��ڵ���LC-MS/MSʵ�����ܹ���������С���е�����100���ʻ��������ʡ�
�������ؿ��ڹ㷺��pHֵ��Χ���Էdz��ߵ�������������ػ�����,ʹЯ��λ����Ϣ���Ķ����Դ������ͷ�,������õ�����Ӧ���������ʻ������εľ���λ�㡣������Ϊ�˸��������������Ӧ�����»���֯���˺���ɥʧ��ԭ��ͻ���,����Ϊ�������������Ŷ�,���������������е�����λ�㶼�DZ�Ҫ�ġ����ڴ�,Regnier��[34]���������������Ĺ̶����������ع���������,���ϲ���������ػ�������ʹ��2 mmol/L�����ػ�0.1 mol/L�ʰ���[18]ϴ������,�Ӷ���ú����ʻ���λ����ĶΡ�Regnier��[35]��������ͨ������Һ��ɫ��(Reversed-phase liquid chromatography,RPLC)��C8���Ͻ�һ����������ʻ���������,���״α����˻��ڵ�������ѧ����Ѫ�����������ļ����ͱ���[36]��
������Դ�����ػ�������,�Լ�ͨ����ˮ��(��)��������������ط������Խ�ϵĵ����ʺ��Ķ�,��������̽�뷨�����ʻ���������Ҫ����Դ[19]��Ϊ����Ч���������Դ����ĵ�������ֲ����˵��������Ա���������,Griffin��[37]���ʹ�����ĵ������ȶ�ͬλ�ر�ǡ��÷�������˵������ʻ������������±�ǡ������Ͳ���������iTRAQ(Isobaric tag for relative absolute quantitation,ͬλ�ر����Ժ;��Զ���)�Լ��ȶ�ͬλ�ر�ǵȷ���,��������������������������ʹ��������ײ����(PQD)����,���������õ�200�����ʻ������ס���֮���Ƶ�ͬλ�ر�Ƿ����ѱ��㷺Ӧ��������Ѫ��[38]����Ѫ��[39]��RCS���ε�����[40,41,42]���ʻ����ļ�����
���������ǰ�������ʻ����ɲ����뿼�(Keq>108 M-1)�������·�Ӧ���ɲ�������(KeqԼΪ104��106 M-1)�ȶ��ö�[43],ARP(Aldehyde-reactive probe,ȩ��Ӧ��̽��)��Ϊ�ʼ������DNA���μ��������ػ��ǰ�������,����Ҫ����Ļ�ԭ����,����Ϊ�㷺Ӧ�õ�һ���������������Ʒ[44,45,46,47]��
�����������»��ǰ������ػ�̽��ĸ�������,�ܹ�ʵ�ֶ�����Դ���ʻ��������ʵĸ�Ч����,��ͨ����������ѧ����ʵ�ֶ���������Դ���ʻ�����ֱ�Ӽ�����Ȼ��,����ȱ����Ч���ѳ��ֶ�,�Ӵ�������ػ���������MS�����������ʻ��������е����Ѻͼ���Ч��,�����߳��������ز�����Ƭ�λ�ʹ��������ø��Ӹ��ӡ��������“һ��ʽ”̽����������λ�����Ч�ʵ͵�����,ʵ���ʻ��������Ķοɿ��ͷų�Ϊ�о����ȵ㡣
����(2)“����ʽ”�ɿ��ͷ�̽��
����Griffin��[48]���һ�ֻ��ڹ�������(SPH)�Լ��������ޱ�Dz���,ͨ���γɹ��ۿ�������,�������°����IJ������ϲ���HNE������,���ڽϸ��¶�(60 ��)�͵�pHֵ(10%������������)��ϴ���ͷš����Ƶ�,����Affi-gel������Ĺ���ɫ�������¶��ϵĵ�������ѧ�����еõ��ܺõ�Ӧ��,Ʃ��������鸻����Ҳ��Ӧ�����ǻ������ε��о�[49]��Maier��[42]��������Զ�����d0/d4-��������-�İ���Ƿ��������ڲ���֬�ʹ���������-�������Affi-gel�����鸻���������,ʵ�����ʻ�������/�Ķεĸ����Ͷ���������Prokai��[40]ͨ����ԭ�������HNE-���ε��Ľ��ж������,ʹ�ù������»�ѧ�����ʻ����Ķ�,��������ͷŻ��ա�����������Ϊ�ص�Ķ��������ڱ��������ʹ��ܵİ���仯,���ҿ��ṩ�йط����źŴ������Ƶ���Ҫ��Ϣ,�����������Ӧ����ص�ϸ�����̵�����,���Ǹ÷������ͷŵ������ȽϿ���,����Ȼ�����ͷŲ���ȫ�����⡣
����GPR(Girard preagent:1-(2-hydrazino-2-oxoethyl) pyridinium chloride,1-(2-�»�-2-�����һ�)����f�Ȼ���)��������������������ܽ���̴���ϵ���Լ���һ����[50],�����»��������ʻ���Ӧ,����炙�����������������ʺ�����������ɡ�Regnier��[51]��GRP���ʻ��������ʷ�Ӧ,��ԭ��ø�����SCX(Strong cation exchange,ǿ�����ӽ���)ɫ������������,����ͬλ����ʽ��GPR�Լ������������ͱ�����ĸ��ȡ���е������ʻ���λ��[52]�����������ͬ��֮�����,Lu��[53]�����˻��ڷ���������FSPE(Fluorous solidphase extraction,��������ȡ)���·���,����ǵ��������������Խ������HNE�����ĸ������÷������ŵ��Ƿ���ǩ������MS�����ڼ���ǿHNE�����ĵ�ǿ��,�Ӷ������ڼ���HNE-���ε���,���ٽ����������Ķε�MS/MSƬ�λ���
����AminoxyTMT(Aminoxy tandem mass tag,�ǰ�����������ǩ)�Ǵ���������ǩ(Tandem mass tag,TMT)ͬ����λ����Լ���������,Griffin��[54]�������ǰ��������Ź��۱�ǵ������еĻ����ʻ���ʵ���˸�����Lu��[55]���������ͬ����λ����ʹ���(SiLAP)����,ʹ��aminoxyTMT����Լ��Ϳ�TMT������֬ͬʱʵ��HNE���ε���ѡ���Ը�����������λ���ȷ����,������2 257�ֶ��ص�HNE�����ĺ�1 121��HNE���ε��ס�
����Wang��[56]�ϳ������������ĺ�Ȳ������̽��(HZyne)���ǰ�����̽��(Ayyne),���������Dz���HNE���εĵ����ʺͲ���λ���Խ���MS����������,ͨ�����ڶ�����ǵ�RD-ABPP(Reductive dimethylation-ABPP,��ԭ�Ͷ������-ABPP)����,������4 000���HNE���ε���ϸ���ѽ���;ͨ��TOP-ABPP(Tandem orthogonal proteolysis-ABPP,������������ˮ��-ABPP)���Լ�����Լ400���߿��Ŷȵ�HNE�Ӻ�λ�㡣Yang��[57]ʹ��ǰ��HZyne̽��,�������������ĹǼ������γɵ�ȫ�ֺ�λ�������Ե����ӵ����ʽ�����,��������N-������������һ�µ��ʻ������ֵ��ע�����,Yang�ἰ�˽�������ѧ��������ѧ�뿪��ʽ�����������ϵ�DZ��Ӧ��ǰ����Wang��[58]������һ�ֱ���������̽��,�����ABPP���Է���������(ferroptosis)�е��ʻ�������,������400������Դ���ʻ������ε����ʺ�20����л�λ�㡣Wang��[59]������̽�����ڼ�����ϩȩ(ACR)����λ��,������2 300���ֵ����ʺ�500����ɱ�ϩȩ����İ��װ���λ�㡣
������Щ���ڿɿ��ͷ�˼·����������̽��,�����������ʻ���������λ��ļ�������������,�ƶ��˵������ʻ������о�����,����������������Ϊ����,�Ķ�Я����ǩ��Ȼ�ϴ�,������迪���µĸ��õķ�������������⡣����,Aye����T-REX[60](Targetable reactive electrophiles and oxidants,������������ʺͻ�����)�����Ͽ�����G-REX[61]����,����ϸ������λ����HaloTag����,�õ��������Խ�Ϲ���װRES(Reactive electrophilic specie,����������,����������RCS)ǰ�塣�ڵ�������������,���ڿɿ��ͷ�RES,��5 min��ϸ�������ͷų�5 μmol/L HNE-Ȳ��,�������˴�ǰ�о�����������¶��صĶ���/�Ѱ�ЧӦ,������������������ʻ���λ��Ŀɿ��ԡ�����Ԥ��G-REX���о�����Ӧ��,�ر���RES��صĵ������ʻ�������ľ�DZ����ĿǰG-REX�յ��õ���HNE���ε�����Ȼʹ����ù���ص��/�����������ķ�������ǰ������,�����������˸ü����ĸ���ЧӦ�á�������ΪӦ�������µĻ�ѧ��Ӧ,�������Ϳ�����������̽��,��Ӧ����:�ٸ�Ч��������ʻ��������,���������ʻ����;���ܹ�����Ч�ظ�������;�����ʻ������Ľ��Ӧ���ǿ����,�Է�����ͷŸ�������/�Ķ�,��ȡ�ʻ���λ����Ϣ;���������,��̽��Ӧ����G-REX�������ݡ�G-ERX����������̽�븻������������ʹ��,�ؽ������ƶ��������ʻ����о��Ľ��̡�
����4 ���� ��
������ѧ����ѧ�����Ŀ��ٷ�չΪ�������ʻ����ĸ����ṩ�˸������������,���������ķ�չ��Ϊ�������ʻ����ṩ�˼���ֶ�,���ߵĽ�ϼ�����ƶ��˵������ʻ������о���չ��Ȼ��,�������ʻ������и߶ȶ�̬��,���Ҵ�����Ŀ�����������ʽ,ʵ�ֲ�ͬ�����ʻ�����ͬʱ�������Ҫ��������⼼���Ľ�һ������,������Ҫ�������������Ϣѧ�����ķ�չ��������ؼ����Ľ�һ����չ,�������ʻ������о��ؽ���Ϊ����,����Ϊ��������Ӧ���Ļ����ṩ����֧�š�
���������
����[1] Davies K J A.Biochem.Soc.Symp.,1995,61:1-31.
����[2] Davies K J A.Arch.Biochem.Biophys.,2016,595(1):28-32.
����[3] Bachi A,Dalle-Donne I,Scaloni A.Chem.Rev.,2013,113(1):596-698.
����[4] Fink G.Encyclopedia of Stress.2nd Ed.Amsterdam:Elsevier,2007:45-48.
����[5] Griesser E,Vemula V,Raulien N,Wagner U,Reeg S,Grune T,Fedorova M.Redox Biol.,2017,11:438-455.
����[6] Mullineaux P M,Baker N R.Plant Physiol.,2010,154(2):521-525.
����[7] Dalle-Donne I,Scaloni A,Butterfield D A.Redox Proteomics:From Protein Modifications to Cellular Dysfunction and Diseases.United States of America:Wiley-Interscience,2006:123-168.
����[8] Colombo G,Clerici M,Garavaglia M E,Giustarini D,Rossi R,Milzani A,Dalle-Donne I.J.Chromatogr.B,2016,1019:178-190.
����[9] Bollineniab R C,Fedorovaab M,Hoffmann R.Analyst,2013,138:5081-5088.
����[10] Ros J.Protein Carbonylation:Principles,Analysis,and Biological Implications.1st Edition.Hoboken,NJ:John Wiley & Sons,Inc.,2017:27-48.
����[11] Dalle-Donne I,Rossi R,Giustarini D,Milzani A,Colombo R.Clin.Chim.Acta,2003,329(1/2):23-38.
����[12] Stadtman E R.Science,1992,257:1220-1224.
����[13] Stadtman E R,Berlett B S.Drug Metabol.Rev.,1998,30(2):225-243.
����[14] Stadtman E R.Free Radical Res.,2006,40(12):1250-1258.
����[15] Levine R L,Stadtman E R.Exp.Gerontol.,2001,36(9):1495-1502.
����[16] Yan L J,Forster M J.J.Chromatogr.B,2011,879(17/18):1308-1315.
����[17] Fritz K S,Petersen D R.Chem.Res.Toxicol.,2011,24(9):1411-1419.
����[18] Madian A G,Regnier F E.J.Proteome Res.,2010,9(8):3766-3780.
����[19] Fedorova M,Bollineni R C,Hoffmann R.Mass Spectrom.Rev.,2014,33:79-97.
����[20] Levine R L,Garland D,Oliver C N,Amici A,Climent I,Lenz A-G,Ahn B-W,Shaltiel S,Stadtman E R.Methods Enzymol.,1990,186 :464-478.
����[21] Goto S,Nakamura A,Radak Z,Nakamoto H,Takahashi R,Yasuda K,Sakurai Y,Ishii N.Mech.Age.Dev.,1999,(107):245-253.
����[22] Shacter E,Williams J A,Lim M,Levine R L.Free Radical Biol.Med.,1994,17:429-437.
����[23] Rhee B A S G,Stadtman E R.Anal.Biochem.,1987,161(2):245-257.
����[24] Yoo B S,Regnier F E.Electrophoresis,2004,25:1334-1341.
����[25] Tamarit E,Ros J.Mass Spectrom.Rev.,2014,33:21-48.
����[26] Bollineni R C,Fedorova M,Hoffmann R.J.Proteomics,2011,74(11):2351-2359.
����[27] Wang C,Weerapana E,Blewett M M,Cravatt B F.Nat.Methods,2014,11:79-85.
����[28] Vila A,Tallman K A,Jacobs A T,Liebler D C,Porter N A,Marnett L J.Chem.Res.Toxicol.,2008,21(2):432-444.
����[29] Kim H H,Tallman K A,Liebler D C,Porter N A.Mol.Cell.Proteomics,2009,8(9):2080-2089.
����[30] Codreanu S G,Ullery J C,Zhu J,Tallman K A,Beavers W N,Porter N A,Marnett L J,Zhang B,Liebler D C.Mol.Cell.Proteomics,2014,13(3):849-859.
����[31] Yang J,Tallman K A,Porter N A,Liebler D C.Anal.Chem.,2015,87(5):2535-2541.
����[32] Chen Y,Qin W,Wang C.Curr.Opin.Chem.Biol.,2016,30:37-45.
����[33] Soreghan B A,Yang F,Thomas S N,Hsu J,Yang A J.Pharm.Res.,2003,20:1713-1720.
����[34] Mirzaei H,Regnier F.Anal.Chem.,2005,77(8):2386-2392.
����[35] Mirzaei H,Regnier F.J.Chromatogr.A,2007,1141(1):22-31.
����[36] Madian A G,Regnier F.J.Proteome Res.,2010,9(3):1330-1343.
����[37] Meany D L,Xie H W,Thompson L D V,Arriaga E A,Griffin T J.Proteomics,2007,7:1150-1163.
����[38] Madian A G,Diaz-Maldonado N,Gao Q,Regnier F E.J.Proteomics,2011,74(11):2395-2416.
����[39] Madian A G,Myracle A D,Diaz-Maldonado N,Rochelle N S,Janle E M,Regnier F E.J.Proteome Res.,2011,10(9):3959-3972.
����[40] Prokai N R L.J.Mass Spectrom.,2011,46:976-985.
����[41] Han B,Stevens J F,Maier C S.Anal.Chem.,2007,79(9):3342-3354.
����[42] Han B,Hare M,Wickramasekara S,Fang Y,Maier C S.J.Proteomics,2012,75(18):5724-5733.
����[43] Dirksen A,Dawson P E.Bioconjugate Chem.,2008,19:2543-2548.
����[44] Chavez J,Wu J Y ,Han B,Chung W G,Maier C S.Anal.Chem.,2006,78(19):6847-6854.
����[45] Griesser E,Vemula V,Raulien N,Wagner U,Reeg S,Grune T,Fedorova M.Redox Biol.,2017,11:438-455.
����[46] Bollineni R C,Fedorova M,Blüher M,Hoffmann R.J.Proteome Res.,2014,13(11):5081-5093.
����[47] Chavez J D,Wu J Y,Bisson W,Maier C S.J.Proteomics,2011,74(11):2417-2429.
����[48] Roe M R,Xie H W,Bandhakavi S,Griffin T J.Anal.Chem.,2007,79(10):3747-3756.
����[49] You X,Yao Y T,Mao J W,Qin H Q,Liang X M,Wang L M,Ye M L.Anal.Chem.,2018,90(21):12714-12722.
����[50] Bray B M.Analyst,1952,77:426-429.
����[51] Mirzaei H,Regnier F.Anal.Chem.,2006,78(3):770-778.
����[52] Mirzaei H,Regnier F.J.Chromatogr.A,2006,1134(1/2):122-133.
����[53] Yuan W J,Zhang Y,Xiong Y,Tao T ,Wang Y,Yao J,Zhang L,Yan G Q,Bao H M,Lu H J.Anal.Chem.,2017,89(5):3093-3100.
����[54] Afiuni-Zadeh S,Rogers J C,Snovida S I,Bomgarden R D,Griffin T J.BioTechniques,2016,60(4):186-196.
����[55] Zhang S W,Fang C Y,Yuan W J ,Zhang Y,Yan G Q,Zhang L,Di Y,Cai Y,Lu H J.Anal.Chem.,2019,91(8):5235-5243.
����[56] Chen Y,Cong Y,Quan B Y,Lan T,Chu X Y,Ye Z,Hou X M,Wang C.Redox Biol.,2017,12:712-718.
����[57] Tian C P,Liu K K,Sun R,Fu L,Yang J.Anal.Chem.,2018,90(1):794-800.
����[58] Chen Y,Liu Y,Lan T,Qin W,Zhu Y T,Qin K,Gao J J,Wang H B,Hou X M,Chen N,Friedmann J P A,Conrad M,Wang C.J.Am.Chem.Soc.,2018,140(13):4712-4720.
����[59] Chen Y,Liu Y,Hou X M,Ye Z,Wang C.Chem.Res.Toxicol.,2019,32(3):467-473.
����[60] Long M J C,Poganik J R,Aye Y.J.Am.Chem.Soc.,2016,138(11):3610-3622.
����[61] Zhao Y,Long M J C,Wang Y,Zhang S,Aye Y.ACS Cent.Sci.,2018,4(2):246-259.
��������ѧ�о�����Ҫ���ݰ����ڵ�����ˮƽ�ϴ��ģ�ط�����֯ϸ���ĵ����ʱ���ˮƽ����������Ρ������ʼ������õ�,�Ӷ���ʾ�����ʵĹ���,��������ɸѡ��ָ�����ơ��ٴ�ҩ�↑����Ԥ���жϵ���������Ҫ���á�...
����������ָһ��ϸ������֯����һ�������������ȫ�������ʡ�����ڴ�ͳ�ĵ������о�����������ѧ�����ڴ��ģˮƽ��һ���Լ�����ǧ�����ֵ����ʵı���ˮƽ������ˮƽ����õȣ��Ӷ���ʾ�����ʲ�������������á�...
����Ĥ��Ҫ����֬˫���Ӳ����Ƕ���������ϵĵ����ʹ��ɡ����ֲ�������ͨ������һ�ֻ����Ĥϵͳ��ϸ����Ĥ (��Ĥ) ����Ϊ������һ��Ĥϵͳ�������ϸ���ʺ���������������Χ�����ָ������������뻷���������ʺ����źš�...
2010-2013���й���������ѧ�����ķ�չ����
��2003���й����൰��������֯(Chinahumanproteomeorganization,CNHUPO)��������,�й��ĵ�������ѧ�о�������ʮ���ķ�չ,���ֳ��ټ��������ٻ���ŵľ���.���й���ѧ������������൰������ƻ�(humanliverproteomeproject,HLPP)֮��,2014...