摘 要: 人工腰椎间盘置换术是治疗椎间盘退行性病变、缓解腰背痛的有效方式。球窝型人工腰椎间盘是最常用的假体类型。本文回顾了球窝型人工腰椎间盘假体的历史,综述了金属—聚合物、金属—金属和聚合物—聚合物不同组合配副的球窝型人工腰椎间盘假体产品现状。结合最新研究进展,分析球窝型人工腰椎间盘假体结构设计因素及影响,并对球窝型人工腰椎间盘假体未来的发展加以展望,以期为设计球窝型人工腰椎间盘假体提供更加全面系统的理论参考。
关键词: 人工腰椎间盘; 球窝型; 假体; 现状;
Abstract: Total lumbar disc replacement is an alternative to interbody fusion for the effective treatment of symptomatic degenerative disc disease. This paper reviewed the history of ball-on-socket type artificial lumbar disc(ALD)prosthesis, which is a typical ALD prosthesis and summarized the ALD prosthesis research progress, according to different materials such as metal-on-metal, metal-on-polymer, and polymer-on-polymer prosthesis. The structural design factors of ball-on-socket type ALD prosthesis were analyzed and its prospect of development was also presented. The purpose of this paper is to provide a theoretical reference for the design of the ball-on-socket ALD prosthesis by reviewing the current state of ball-on-socket type ALD prosthesis.
Keyword: artificial lumbar disc; ball-on-socket; prosthesis; current state;
引言
腰背痛(low back pain,LBP)是导致人类残疾的主要原因[1]。据美国疾病控制和预防中心的一项调查显示,约有28.0%的成年人患有LBP[2]。LBP的主要原因是由于腰部的椎间盘退行性病变(degenerative disk disease,DDD)[3,4]。天然腰椎间盘能够传递和缓冲腰椎载荷,承受剪应力、局部压应力和拉伸应力等,同时具有局部扭转功能,但在长期疲劳的情况下就会发生DDD[5]。轻度DDD可采用保守治疗,经过六个月保守治疗无效者和重度DDD患者均需要采取手术治疗。长期以来,腰椎融合术是治疗DDD的首选手术治疗方式,能够有效减轻患者疼痛,但术后患者的腰椎运动范围被限制,活动不便,而且长期临床效果研究显示,腰椎融合术会增加腰椎手术节段邻近节段退变的风险,这些缺点促使脊柱外科医生在不断努力寻找一种可以替代腰椎融合的手术方式[6]。人工腰椎间盘置换术(lumbar total disc replacement,LTDR)的出现使得代替融合术治疗DDD变为可能。从理论上讲,LTDR是一种理想的治疗方案,既可以取代天然的腰椎间盘,恢复腰椎间盘的高度,重建生理功能和生物力学性能,又能减轻患者疼痛,降低邻近节段DDD导致的再手术率[5,7,8]。因此,人工腰椎间盘假体的研发变得十分迫切。临床上应用的人工腰椎间盘假体主要有粘弹性一体型结构和球窝关节型结构两种形式,由于大部分人工腰椎间盘假体采用的是球窝关节结构,因此,本文主要综述球窝型人工腰椎间盘假体的研究现状。

1、 球窝型人工腰椎间盘假体的历史与发展
人工腰椎间盘假体的设计需满足腰椎生物力学的要求,具体包括:能够承受腰椎负载且不发生变形或断裂;尽量减少摩擦和磨损的影响;能够长期保持腰椎正常的运动范围等。LTDR设计理念的提出几乎与Charnley髋关节假体的报道是同时的,并非源于髋膝关节置换术。最初,一种由单一金属球组成的人工腰椎间盘假体于19世纪50年代晚期被Fernstr?m植入人体,但手术终因人工腰椎间盘假体终板沉陷而宣告失败。随后,Fassio又设计了第一款具备一定弹性的人工腰椎间盘假体,中间部分是结构类似Fernstr?m钢球但具有减震功能的硅橡胶。Kostuik也曾设计了一款依靠铰链链接的人工腰椎间盘假体,中间装有弹簧,具有减震功能。Lee设计了一种带有羟基磷灰石涂层的弹性人工腰椎间盘衬垫假体,但这些设计均未见成功应用于临床的报道[7,9]。
直到1982年,Kurt Schellnack和Büttner-Janz设计了Charité型人工腰椎间盘假体,一种由超高分子量聚乙烯(ultrahigh molecular weight polyethylene,UHMWPE)作为髓核,两个高度抛光的不锈钢金属作为终板,且髓核可以在终板之间滑动的椎间盘假体[5]。这种金属—聚合物配副具有摩擦系数低、磨损率小的优点。1984年9月,SB CharitéⅠ型假体首先在德国柏林洪堡大学附属Charité医学院第一次被成功植入人体,用以治疗严重的DDD。1985年,下一代SB CharitéⅡ型假体经过改进,两侧设有两翼来防止人工腰椎间盘假体下沉。这两款人工腰椎间盘假体均由German Democratic Republic制造,当时仅仅应用于Charité医学院,并没有进行商业化推广。1987年,SB CharitéⅢ转由LINK公司生产制造,金属终板改由钴铬(CoCr)合金制造,表面带有生物涂层,于2004年获得美国食品与药物监督管理局(Food and Drug Administration,FDA)批准,开始大规模应用于临床。
2、 球窝型人工腰椎间盘假体的产品现状
目前,国际上球窝型人工腰椎间盘假体较多,主要研发地点在美国,少数产品的研发在德国、南非等国家。其中被美国FDA批准的只有3种。人工腰椎间盘假体按照材料配对情况分为金属—聚合物(metal-on-polymer,MoP)型、金属—金属(metal-on-metal,MoM)型和聚合物—聚合物(polymer-on-polymer,Po P)型,具体情况如表1[10,11,12]所示。
2.1、 金属—聚合物型
2.1.1、 Charité
自1984年SB Charité型人工腰椎间盘假体开始应用于临床以来,国外LTDR已达数千例之多。Charité假体目前归DePuy Synthes公司所有,是一种非限制型假体,具有5个自由度。Charité假体具有独特的移动聚合物UHMWPE髓核,从而能够再现类似天然脊柱的运动形式。与天然腰椎间盘相似,活动的UHMWPE髓核在弯曲时向背侧移动,在伸展时向腹侧移动。这样的结构对产品植入的位置要求并不严格,能够减低外科医生的手术难度,但其缺点在于对上下关节面及小关节会造成很大的应力。
通常,临床上患者的术后疼痛程度由视觉模拟评分法(visual analog scale,VAS)评估,腰椎功能恢复情况由功能障碍指数(oswestry disability index,ODI)评估。Lu等[13]在2015年对使用Charité假体的35例患者进行了平均11年的随访,其中2例患者进行了再手术,VAS和ODI均显着改善,但腰椎运动范围明显减少,3例患者假体下沉。2017年继续对此35例患者进行随访,发现假体下沉率增加。van Ooij等[14]对26例患者进行为期91个月的随访研究,其中有14例患者邻近关节退化,16例患者假体出现下沉,还有11例患者椎体小关节面退化,12例患者假体材料UHMWPE明显磨损,有2例患者Charité假体被移除,重新进行融合手术,预计随着时间的推移,手术的成功率将会越来越低。最终,Charité假体由于在长期使用过程中出现较多并发症,晚期并发症主要有下沉、邻近节段退化、关节面退化和假体移位等,导致进行融合再手术,于2012年退出国际市场[10,15,16]。目前此产品已改进,且更名为INMOTION人工腰椎间盘假体。2.1.2 ProDisc-L ProDisc-L假体是由Thierry Marnay在19世纪80年代末研发的,1998年以后ProDisc-L经历了两代改进,并于2006年获得美国FDA批准,现属于DePuy Synthes公司。ProDisc-L假体仍然采用CoCr合金和UHMWPE配副,但与Charité假体不同的是,UHMWPE镶嵌在CoCr合金下终板上,转轴固定,属于半限制型结构。终板中间有脊骨,起到主要固定的作用,钛涂层可以进行二次固定。ProDisc-L假体能够保持腰椎原始运动功能,减少腰椎关节面的压力,但对外科医生的手术技术要求比Charité假体高。
表1 人工腰椎间盘假体产品现状
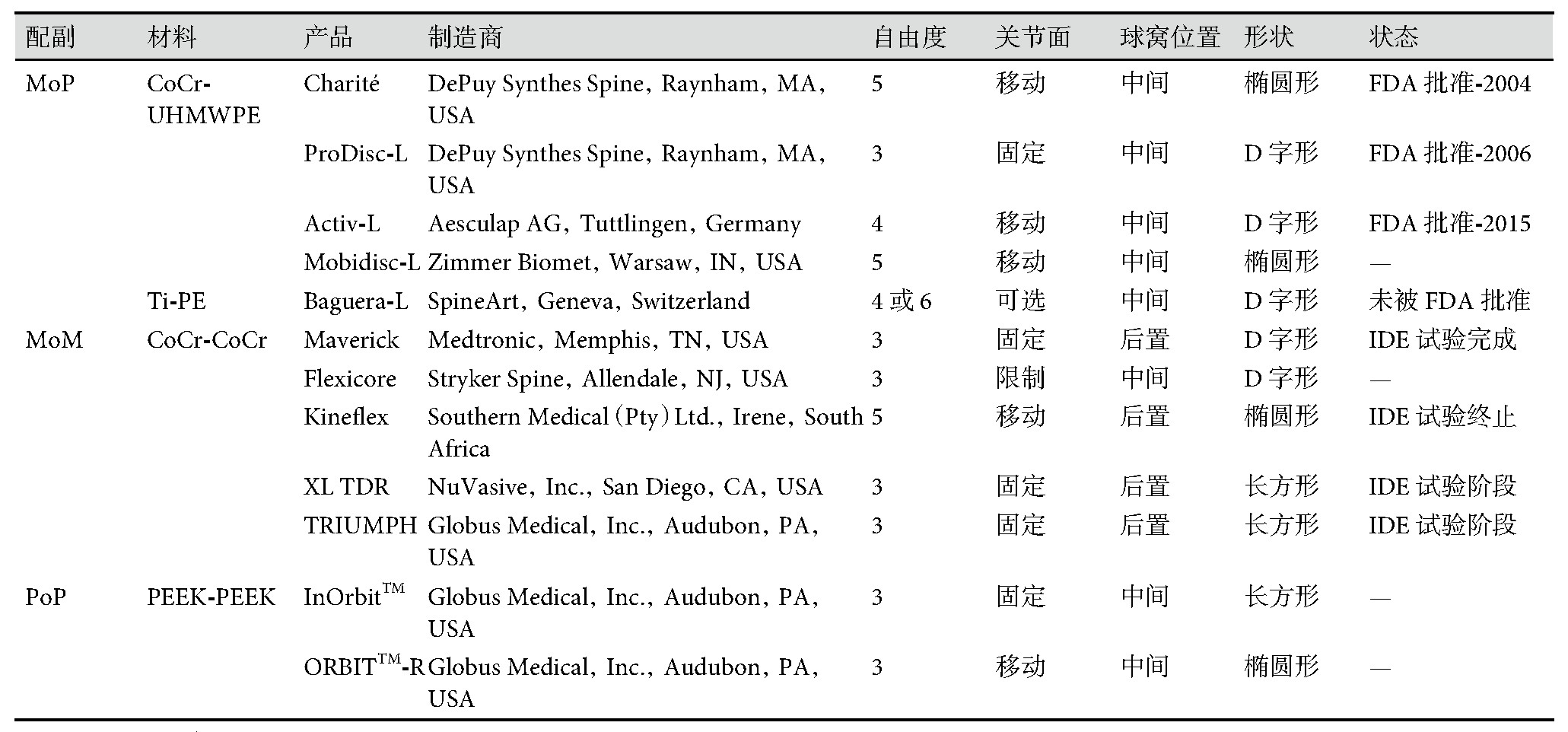
注:IDE:医疗器械研究性试验豁免(investigational device exemption);PEEK:聚醚醚酮(polyetheretherketone)
ProDisc-L假体在治疗DDD方面具有恢复时间快、保留运动功能、手术时间短等优点,优于融合术。许多研究Pro Disc-L假体的工作仍在进行[17],对患者进行随访发现,术后VAS和ODI指数均显着改善,手术成功率和患者满意度均较高。
2.1.3、 Activ-L
Activ-L是被美国FDA最新批准的一种人工腰椎间盘假体,也是半限制型结构[18]。与ProDisc-L不同的是,Activ-L假体的聚合物髓核可以在移动槽内沿着一个方向微小移动,在另一个方向上无法移动,转轴不固定。Activ-L假体表面具有适合骨生长的微孔钛和磷酸钙涂层,其设计更好地匹配了腰椎生理结构。
Girardi等[19]对Activ-L假体进行短期随访研究表明,使用Activ-L假体是一种安全有效的腰椎融合替代疗法,但仍需要进行长期的临床随访和生物力学研究。Yue等[18]对比之前两种FDA批准的Charité和ProDisc-L假体,Activ-L假体采取特定的设计改进以及合适的活动范围,可以更好地重建腰椎生理活动,具有更好的临床效果。
2.1.4、 Mobidisc-L
Mobidisc-L是一种新型MoP假体,在Activ-L假体基础上增加了一个自由度,UHMWPE髓核的外周设有停止控制结构,使其能够限制在生理范围内移动,其活动自由度和Charité假体相同,有助于恢复腰椎的生理活动,同时减少假体内应力。Mobidisc-L上下终板通过固定嵌片进行终板与椎体骨的固定,其固定嵌片设计为前方和侧方,假体可以通过中线或靠近中线位置入路植入,这取决于患者的生理解剖结构,可以最大限度地减小创伤。
2.1.5、 Baguera-L
Baguera-L假体金属终板采用钛合金材料,该材料的低伪影特性可有效降低金属对核磁影像的干扰。为避免摩擦和磨损,钛合金表面沉积了DIAMOLITH涂层,该涂层是一种采用等离子体增强化学气相沉积技术形成的类金刚石薄膜,硬度高,耐磨损。髓核与下终板的接触处留有一定的空隙,可以起到进一步的缓冲作用,因此Baguera-L假体要比其他假体多一个自由度。假体与椎体骨的接触表面涂有多孔钛涂层,可促进骨的生长。Baguera-L假体提供两种髓核可供选择,分别为固定髓核和移动髓核。
2.2、 金属—金属型
2.2.1、 Maverick
Maverick假体是由Mathews等设计,2002年在欧洲首次使用,属于半限制型MoM结构,耐磨损性能好,采取偏后旋转中心的结构设计,减少了上下小关节面的负载[12,20]。MoM配副结构可以减少UHMWPE产生的磨损碎片颗粒的刺激及其对骨的吸收,有效减少疼痛,提高生活质量。对患者的长期随访显示,VAS和ODI指数均有显着改善,手术恢复情况良好,术后并发症在可接受范围内,是治疗DDD安全有效的方式[21]。Bastien等[22]对345例患者进行为期2年的随访发现,81%患者表现良好,并且没有出现严重的并发症。
2.2.2、 Flexicore
Flexicore也是一种MoM型人工腰椎间盘假体,采用CoCr合金,旋转中心放在端板的中央,直径为13 mm。该假体为一体化假体,医生在植入之前已经装配好,没有设置前凸角度,医生抓取后可直接植入腰椎间隙,其卡扣结构能自行调节角度,并适应椎体弧度,避免因椎体弧度与假体型号不匹配而造成的假体松动、应力集中等情况。
2.2.3、 Kineflex
Kineflex是一种由一个可以移动的CoCr合金髓核和两个CoCr合金终板组成的MoM型人工腰椎间盘假体,相关临床报道表明,它能够有效治疗单节段DDD,已被证实在临床上是成功的。CoCr合金终板具有钛等离子体喷涂表面以促进骨融合,采用后置旋转中心。此假体具有不同的高度,按照其相对于髓核中心线的厚度来定义,组合尺寸从10 mm到13.75 mm不等,且具有5°、10°和15°的前倾角可供选择。由于经济和商业原因,Kineflex假体的IDE实验终止。研究结果显示Kineflex假体的失败率要少于Charité假体和Maverick假体,是一种有效的治疗DDD的方式[23]。血清离子水平分析发现,任何随访点的最大平均值都低于FDA推荐的用于监测髋关节置换术患者水平最小值的20%[24]。
2.2.4、 XL TDR
XL TDR假体目前还是一种试验阶段的人工腰椎间盘假体,通过腰椎侧入路植入。采用CoCr合金材料,椎间盘切除术后可植入。临床效果显示XL TDR侧入路植入是一种可行的手术方式,术后能够有效保护邻近节段,患者VAS和ODI指数均有显着改善[25,26,27]。
2.2.5、 TRIUMPH
TRIUMPH假体是第一个可以通过后侧入路植入的人工腰椎间盘假体,由两个CoCr合金终板组成,带有的多孔涂层可帮助其固定,独特的设计使得无论插入角度如何,都能进行合适的生理范围运动。IDE研究始于2007年,目前仍在进行中,但不再招聘志愿者。
2.3、 聚合物—聚合物型
ORBITTM-R是第一个结合生理运动和成像兼容性的人工腰椎间盘聚合物假体。由于采用PEEK材料,因而不存在干扰影像的问题,同时PEEK的生物相容性较好,有利于体内长期植入。InOrbit TM同ORBITTM-R材料相同,但采用从侧入路植入,可最大限度地减少对包括前纵韧带在内等结构的破坏,创伤小。由于目前尚处于试验阶段,所得临床数据有限。
3、 球窝型人工腰椎间盘假体的设计因素
3.1、 材料配副种类
如表1所示,人工腰椎间盘假体材料主要分为MoP、MoM和PoP三种。目前,虽然人工关节产品可使用陶瓷材料,但由于陶瓷的脆性,为避免腰椎神经的伤害,市场上仍对陶瓷配副作为人工腰椎间盘材料保持较为谨慎的态度。对于MoP假体,除Baguera-L假体采用钛合金外,其余4种人工腰椎间盘假体均采用CoCr合金与UHMWPE配副组合,且髓核均放置在终板中心,UHMWPE髓核与CoCr合金的相对运动如表2所示,ProDisc-L、Activ-L和Mobidisc-L假体运动自由度依次增多,Charité和Mobidisc-L运动自由度相同。
这三种材料配副的优缺点如表3所示。Co Cr合金与UHMWPE配副组合具有良好的摩擦学性能。Po P配副假体目前只有PEEK-PEEK材料,PEEK-PEEK具有良好的生物相容性和摩擦学性能。使用聚合物可以缓冲吸振,减少对椎骨的冲击,但长期恶劣的力学环境使得聚合物容易磨损,发生边缘破裂[28],而聚合物的磨屑则会引起骨溶解,导致手术失败。
表2 CoCr-UHMWPE材料配副假体不同的髓核固定方式

表3 不同材料配副的优缺点

由于腰椎的受力情况恶劣,Baguera-L假体采用的钛合金必须进行类金刚石涂层以防止磨损严重。采用CoCr合金能够防止过重的磨损和假体破坏,由于CoCr合金良好的耐磨损性能和力学性能,MoM型假体设计者常采用后置球窝位置以减小小关节面的压力,但后置之后,增大了球窝关节面应力,这也是MoP配副结构不采取后置球窝位置的主要原因之一。CoCr合金可以承受后置之后的受力环境,但也会存在MoM配副金属离子释放引起炎症等不良反应问题,影响了MoM配副人工腰椎间盘假体的长期寿命[29,30]。
3.2 、产品设计规格
如表1所示,人工腰椎间盘假体外形分为椭圆形、D字形和长方形。长方形由于宽度较小,大多是为了采用侧入植入方式以减小手术创伤和恢复时间。XL TDR、TRIUMPH、InOrbit TM均为长方形,剩余假体为椭圆形或D字形。
图1 人工腰椎间盘假体尺寸标注示意图
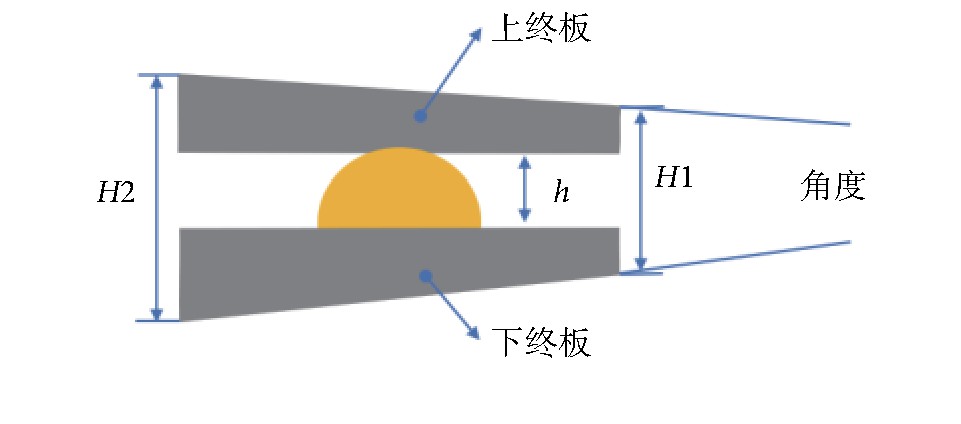
Fig.1 Size labeling schematic diagram of artificial lumbar disc prosthesis
表4所示为人工腰椎间盘假体的产品尺寸设计规格,不同产品生产商的测量规则不同,如图1所示,H1代表总后高,H2代表总前高,h代表内高,角度是两个终板上下表面的总角度。
由于不同节段腰椎间盘的角度不同,通常从L1到S1的角度逐渐增大,较大角度是为了L5-S1阶段准备,这个腰椎节段受力严重也最容易出现问题。由于一些假体处于试验阶段或退出市场,目前只能查到以上5种假体的参数。
3.3、 表面生物涂层和固定方式
如表5所示,假体生物涂层大体分为3种,分别为多孔钛、磷酸钙和羟基磷灰石;终板与椎体固定方式分为3种,分别为脊骨、尖齿和固定嵌片。
其中脊骨和尖齿固定方式使用较多,仅有Mobidisc-L假体使用固定嵌片,脊骨的固定效果好,不容易发生移位,但需要剔除的骨组织较多。尖齿的固定效果差,但可保留较多的骨组织。
3.4 、其他参数
关于假体自由度,较多的自由度会增加小关节面的应力,但会减少假体内部应力。关于球窝关节面,固定的关节面结构会增加球窝表面的应力,一般金属材料可采取固定的关节面,聚合物材料一般采用移动关节面以保护聚合物。同时,MoM型假体可进一步采用后置的固定关节面,有利于减小腰椎小关节应力。关于球体半径和径向间隙,根据赫兹接触理论可以计算所得最大接触压力与径向间隙和球体半径的关系[31],更小的径向间隙和更小的球体半径具有更小的最大接触应力,从而减小磨损。Moghadas等[32]对球半径10、12、14、16 mm的CoCr-CoCr型人工腰椎间盘假体进行磨损测试,实验结果展示半径越小摩擦系数越低。
表4 人工腰椎间盘假体产品设计尺寸规格
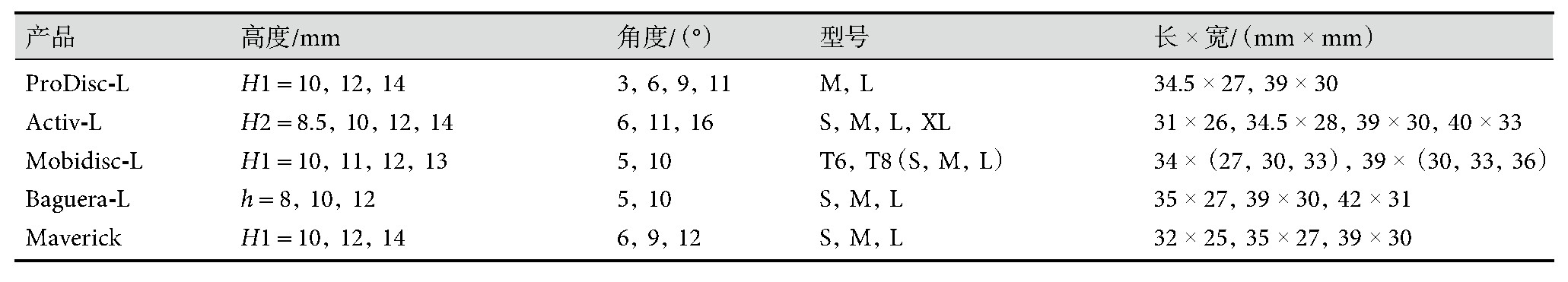
表5 人工腰椎间盘假体产品表面生物涂层和固定方式

4、 总结与展望
从Kurt Schellnack和Büttner-Janz设计Charité腰椎间盘假体成功应用于临床开始,球窝型人工腰椎间盘假体已经走过30多年的历史,人工腰椎间盘假体在结构方面越来越符合天然椎间盘的生理结构,在材料方面逐渐强化材料的性能并加以改性,在涂层、手术方式等方面均有较大改进,LTDR因此也得到的较大的发展,但目前人工腰椎间盘假体还存在诸多不足与技术瓶颈[33]。
首先,术后疼痛、终板下沉或移位、小关节面退化等诸多术后并发症发生率仍然较高。这是由于CoCr合金的弹性模量与人体骨的弹性模量不匹配导致的,可考虑从个性化治疗方面探索解决方案,如采用金属三维(three-dimensional,3D)打印技术使得人工腰椎间盘假体终板和椎骨形状完全贴合,从而防止下沉。Mróz等[34,35]通过有限元分析得出采用金属3D打印技术生产的个性化人工腰椎间盘假体是有潜力的。金属3D打印技术可以打印适合细胞生长的多孔梯度结构贴合骨表面以促进骨长入,进一步减小假体下沉风险[36]。其次,MoM配副金属离子释放目前仍然是一个焦点问题,可通过耐磨涂层加以强化,因而耐磨涂层的研发是未来发展方向之一。另外,LTDR更加长期的随访有待进一步进行。
目前,已经实现国产化的人工腰椎间盘假体数量几乎为零,该领域仍然被国外所垄断。2014年四川大学华西医院首次将自主研发的一款人工颈椎间盘应用于临床,此举具有重要意义,若后续临床随访能证明产品的有效性,该产品将打破欧美在颈椎外科领域的垄断。而今,人工腰椎间盘假体国产化仍需努力,以期早日打破国外垄断。
利益冲突声明:本文全体作者均声明不存在利益冲突。
参考文献
[1] Vos T, Barber R M, Bell B, et al. Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990–2013:a systematic analysis for the global burden of disease study 2013.Lancet, 2015, 386(9995):743-800.
[2] Blackwell D L, Lucas J W, Clarke T C. Summary health statistics for U.S. adults:National Health Interview Survey, 2012. Vital Health Stat, 2014, 260(260):1-171.
[3] Song Jian, Liao Zhenhua, Shi Hongyu, et al. Fretting wear study of PEEK-based composites for bio-implant application. Tribol Lett,2017, 65(4):Article number 150.
[4] Formica M, Divano S, Cavagnaro L, et al. Lumbar total disc arthroplasty:outdated surgery or here to stay procedure? A systematic review of current literature. J Orthopaed Traumatol,2017, 18(3):197-215.
[5] Salzmann S N, Plais N, Shue J, et al. Lumbar disc replacement surgery—successes and obstacles to widespread adoption. Curr Rev Musculoskelet Med, 2017, 10(2):153-159.
[6] Radcliff K, Spivak J, Darden B N, et al. Five-year reoperation rates of 2-level lumbar total disk replacement versus fusion:results of a prospective, randomized clinical trial. Clinical Spine Surg, 2018,31(1):37-42.
[7] 张振军,李阳,廖振华,等.有限元法在腰椎生物力学应用中的研究进展和展望.生物医学工程学杂志, 2016, 33(6):1196-1202.
[8] Yue J J, Garcia R, Blumenthal S, et al. Five-year results of a randomized controlled trial for lumbar artificial discs in singlelevel degenerative disc disease. Spine(Phila Pa 1976), 2019:1.
[9] Bono C M, Garfin S R. History and evolution of disc replacement.Spine J, 2004, 4(6 Suppl):S145-S150.
[10] Abi-Hanna D, Kerferd J, Phan K, et al. Lumbar disk arthroplasty for degenerative disk disease:literature review. World Neurosurg,2018, 109:188-196.
[11] Reeks J, Liang H. Materials and their failure mechanisms in total disc replacement. Lubricants, 2015, 3(2):346-364.
[12] Veruva S Y, Steinbeck M J, Toth J, et al. Which design and biomaterial factors affect clinical wear performance of total disc replacements? A systematic review. Clin Orthop Relat Res, 2014,472(12):3759-3769.
[13] Lu S, Hai Y, Kong C, et al. An 11-year minimum follow-up of the Charite III lumbar disc replacement for the treatment of symptomatic degenerative disc disease. Eur Spine J, 2015, 24(9):2056-2064.
[14] van Ooij A, Oner F C, Verbout A J. Complications of artificial disc replacement:A report of 27 patients with the SB Charitédisc. J Spinal Disord Tech, 2003, 16(4):369-383.
[15] Punt I M, Visser V M, van Rhijn L W, et al. Complications and reoperations of the SB Charite lumbar disc prosthesis:experience in 75 patients. Eur Spine J, 2008, 17(1):36-43.
[16] Choi J I, Kim S H, Lim D J, et al. Biomechanical changes in disc pressure and facet strain after lumbar spinal arthroplasty with CHARITETM in the human cadaveric spine under physiologic compressive follower preload. Turk Neurosurg, 2017, 27(2):252-258.
[17] Siepe C J, Heider F, Wiechert K, et al. Mid-to long-term results of total lumbar disc replacement:a prospective analysis with 5-to 10-year follow-up. Spine J, 2014, 14(8):1417-1431.
[18] Yue J J, Garcia R J, Miller L E. The activL?Artificial Disc:a nextgeneration motion-preserving implant for chronic lumbar discogenic pain. Med Dev(Auckl), 2016, 9:75-84.
[19] Girardi F, Shein D, Shue J. Evaluation of aesculap implant systems activ-L artificial disc for the treatment of degenerative disc disease.Expert Rev Med Dev, 2016, 13(12):1069-1072.
[20] Mathews H H, LeHuec J, Friesem T, et al. Design rationale and biomechanics of Maverick total disc arthroplasty with early clinical results. Spine J, 2004, 4(6):S268-S275.
[21] Assaker R, Ritter-Lang K, Vardon D, et al. Maverick total disc replacement in a real-world patient population:A prospective,multicentre, observational study. Eur Spine J, 2015, 24(9):2047-2055.
[22] Bastien J, Lecomte Y, Willems S. A retrospective review of 345patients with lumbar tdr in two years follow-up over 10 years of practice in one belgian clinical center:Results. Acta Orthopaedica Belgica, 2016, 82(3):440-455.
[23] Pettine K, Ryu R, Techy F. Why lumbar artificial disk replacements(LADRS)fail. Clin Spine Surg, 2017, 30(6):E743-E747..
[24] Guyer R D, Pettine K, Roh J S, et al. Five-year follow-up of a prospective, randomized trial comparing two lumbar total disc replacements. Spine(Phila Pa 1976), 2016, 41(1):3-8.
[25] Malham G M, Parker R M. Early experience with lateral lumbar total disc replacement:Utility, complications and revision strategies. J Clin Neurosci, 2017, 39:176-183.
[26] Yue J J, Garcia R. Five-year results of a randomized controlled trial for lumbar artificial discs in single-level degenerative disc disease.Spine J, 2017, 17(10):S70.
[27] Pokorny G, Marchi L, Amaral R, et al. Lumbar total disc replacement by the lateral approach-up to 10 years follow-up.World Neurosurg, 2019, 122:e325-e333..
[28] Grupp T M, Yue J J, Jr R G, et al. Evaluation of impingement behaviour in lumbar spinal disc arthroplasty. Eur Spine J, 2015,24(9):2033-2046.
[29] Eckold D G, Dearn K D, Shepherd D E T. The evolution of polymer wear debris from total disc arthroplasty. Biotribology,2015, 1:42-50.
[30] Hyde P J, Fisher J, Hall R M. Wear characteristics of an unconstrained lumbar total disc replacement under a range of in vitro test conditions. J Biomed Mater Res Part B Appl Biomater,2017, 105(1):46-52.
[31] Wenzel S A, Shepherd D E. Contact stresses in lumbar total disc arthroplasty. Biomed Mater Eng, 2007, 17(3):169-173.
[32] Moghadas P, Mahomed A, Hukins D W L, et al. Friction in metalon-metal total disc arthroplasty:Effect of ball radius. J Biomech,2012, 45(3):504-509.
[33] Hart R A, DePasse J M, Daniels A H. Failure to launch:what the rejection of lumbar total disk replacement tells us about American spine surgery. Clin Spine Surg, 2017, 30(6):E759-E764.
[34] Mróz A, Skalski K, Walczyk W. New lumbar disc endoprosthesis applied to the patient's anatomic features. Acta Bioeng Biomech,2015, 17(2):25-34.
[35] Mróz A, Wi?niewski T, Skalski K. Effect of selective laser melting technology on the tribological properties of the prototype of intervertebral disc endoprothesis. In?ynieria Powierzchni, 2016, 2:24-30.
[36] Mróz A B, Lapaj L, Wisniewski T, et al. Friction and wear of the intervertebral disc endoprosthesis manufactured with use of selective laser melting process. Rapid Prototyping J, 2017, 23(6):1032-1042.
引言在髋关节需求量越来越大的现实情况下,作为医疗器械质量检验机构,必须严把上市髋关节产品的质量关。髋关节产品的质量检验项目主要包括材料分析(化学成分、力学性能(抗拉强度、延伸率、断面收缩率、规定非比例延伸强度)、显微组织、耐腐蚀性、内部...