
����
���������������ڹ̶������߹ǹ����������ڷ����š��߹ǽ��ʸ�λ���Ϻͻ������ڻ�����ٷβ�����֢�ͻ��Σ����ָܻ��ã�Ч�����ŵõ��˹㷺���Ͽɺ��ƹ㡣�����ڶԹ����߹ǽ���ѧ�۲⣬�Լ����߹ǹ��������������Ťת��������ѧ���Խ��з����Ļ����ϣ�������һ�� AZ31B þ�Ͻ�������߹����ڶ����ֶ���������ѧ���Խ��в��ԣ������ٴ�ʹ�õĽ��ھ���������������߹����ڶ����бȽϷ������������¡�
����
���������뷽��
����
����1��AZ31B þ�Ͻ�������߹����ڶ������
����AZ31B þ�Ͻ�������߹����ڶ��� ר��������CN201894668U�� ,Ϊһʹ�� AZ31B ������þ�Ͻ�����Ļ��α�ƽ����ṹ����������Ϊ 35mm,ǰ��Ϊ״��ͷ��������� 2mm,����Ϊ 3mm; ����������������������£�ķ������̣��������һ���Ŀ����ԣ����ҿ������ڽ������գ����������ٴ�ȡ����������ʹ�ó�����е���������������� ��ͼ 1 ~4�� .
����
����2��ģ���Ʊ�
����������ίԱ��ͬ�⣬�ɼ� 30 �� 20 ~ 50 �����忪�����м��µij�Լ 15cm �����ʵ� 5 �߹Dz��߱걾��������飬���������걾�����걾�ϸ��ŵļ��⼰��������֯���������߹ǵ������ԣ���������ˮ��ʪ��ɴ����������걾���ڹ������߹��жιǼ������Ƴɲ���Ҹ���ߴ��߹ǹ���ģ�ͣ����ֲ���Ա𣬽��߹������þۼ���ϩ���֬��������ʵ��걾����������������ֳ� 3 �顣ʵ���飨 AZ31B �飩 : �����������Ƶ� AZ31B þ�Ͻ�������߹����ڶ��̶������������������߹����ڶ����˷ֱ�����߹Ƕ϶��� 1/2 �߹Ƕ��������ĺ�£��ɹ̶���ʹ������������߹ǹ���ǻ�����߹���Ϊһ�塣ʵ���飨 PLLA �飩 : ���þ���������������߹����ڶ����ӣ� PLLA�� �ڹ̶�������ͬ AZ31B �顣�����飺 Ϊ�������߹ǡ����б걾�����ù�ˮ��̶�ƽ�����Ա��ڼ��أ���֤���龫�ȡ�
����3����ѧ����ģ��
�������߹��Լ������� WE-100B ������Һѹ����������ϣ����걾�������Ƶļо��ڣ��ȴ�����Ȼ����λ������أ����������������DZ������߹�ȥ���ɳۡ�����ʱ��ЧӦӰ�죬ʹʵ�鴦����������״̬���� 5mm/min �ļ����ٶȶ�����ʩ����أ����������������飬�����ƻ�������Զ������������غɡ������ء����Ӧ�������Ӧ�������ݡ�Ťת������ͬ��������ʩ��Ť�ء����Բ�ͬ�ڹ̶����ͽ�������γ����顣ʵ����Ϊ���ֱ걾����״̬���ڸ���ʱ��������ˮ������
����4�����ݴ���
�����������ʵ�����ݣ����� SPSS 11. 0 ������ SPSS��˾�������� ���з��������������� x�� ± s ��ʾ��������ȫ������鵥���ط���������������ݷ������������ t ����� 3 ��ʵ�����ݽ��бȽϣ�P < 0. 05 Ϊ���������������塣
����
������ ��
����
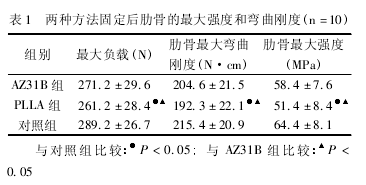
����1����������ʵ������ �� 1��2���� �������ƻ�����������ʵ��ʱ������ء����ǿ�Ⱥ������նȣ�AZ31B �顢PLLA ��ֱ��������Ƚϣ�AZ31B ���������Ƚ��������Բ��죬P >0. 05; PLLA ���������Ƚ��������Բ��죬P <0. 05,PLLA ���� AZ31B ��Ƚ��������Բ��죬P <0. 05.
�����ڷ��ƻ�����������ʵ��ʱ����¼��������������ͬλ�ƾ���������������С����λ�� 2mm ʱ 3��Ƚ������Ų��죻 ��λ�� 4mm ʱ AZ31B ���������Ƚ��������Բ��죬P > 0. 05,PLLA ���������Ƚ��������Բ��죬P < 0. 05,PLLA ���� AZ31B��Ƚ��������Բ��죬P < 0. 05; ��λ�� 6mm ʱAZ31B ���������Ƚ��������Բ��죬P > 0. 05,PLLA ���������Ƚ��������Բ��죬P < 0. 05,PL-LA ���� AZ31B ��Ƚ��������Բ��죬P < 0. 05.
����2��Ťת����ʵ������ �� 3����
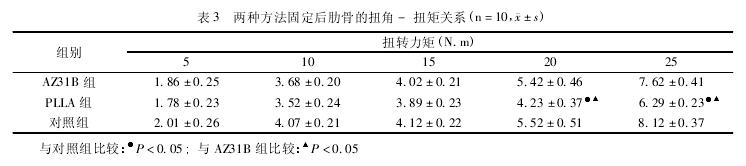
�����ɱ� 3 �ɼ������� AZ31B ����С�ڶ������Ť�أ����������Բ��죬PLLA �鵱Ť��≥20° ʱ��AZ31B ��Ͷ�����Ƚ��������Բ��죬P < 0. 05.
����3������γ�ʵ������ �� 4����
�����������Ƚϣ�
������P < 0. 05; �� AZ31B ��� �ϣ�
������P <0. 05�ɱ� 4 �ɼ���ʵ��������������غɺ������������С�ڶ����飬�Ƚ��������Բ��죬P <0. 05; PLLA ����������غɺ������������С�� AZ31B �飬�Ƚ��������Բ��죬P <0. 05.
����
��������
����
����Ŀǰ���ٴ����ѳɹ�Ӧ�����߹ǹ����ڹ̶�������������Ҫ�д��ѡ����Ѽ���Ͻ��߹ǻ����ӹǰ�ͽ��ھ���������������߹����ڶ������ʸְ�ȡ����ڽ����ӹǰ�ĵ���ģ�����Ƥ�ʼ�ľ���죬��ʹ�������Ӧ���ڵ����ã�ʹ����ǿ�Ƚ��͡����ϳٻ��� �� X ��Ƭ���ʱֲ�����ڵ�Ӱ��۲���������ͬʱ��Щ����������Ħ������ĥм�Լ���ʴ�����ж����ӣ���ɾֲ�������Ӧ������֢���������������ԡ����⣬��Щ����Ϊ���ɽ�����ϣ���������֯���ָܻ�֮����ͨ����������ȡ�������ӻ��ߵ�ʹ�༰ҽ�Ʒ��ø�����������߹ǹ����ڹ̶�����Ӧ�þ߱��� �� 1�� �����õ����������ԣ���ԭ�ԣ����ųⷴӦ�� �� 2�� ���°����»��ԣ��������ã� �� 3�� ���㹻����ѧǿ�ȣ��ܹ���������ڹ̶��������ѧҪ��ͬʱ������̫�ߵĵ���ģ������������̶���λ��Ӧ���ڵ��� �� 4�� �������ܹ����Ⲣ�������գ� �� 5�� �������͡����������棻 �� 6�� ����������ԣ��ܴٽ��������ϡ�
����þ�Ͻ�������˹�����ĵ���ģ���� �˹ǵ���ģ��Ϊ 25GPa,þ�Ͻ�Ϊ 45GPa ���ң� ,���������õ����������ԣ� ����Ҫ����þ�Ͻ���������ڻ����н��⣬�ܹ��������������ͬʱ��������ܴٽ��������ϣ�����ʺ�����Ϊ�����ڹ̶����ϡ����������˶�ʱ���伡�����߹��������˶����������������¾���ǰ�����Ҿ������� �����˶�ʱ�������������෴�� �߹�ͷ���߽�������������˶���Χ�����ؽ������°ڶ����߹Ƿ���������Ťת�˶�����˿����߹��ڹ̶���е��������ѧ���ܣ�����俹���������Ϳ�Ťת�������в��ԡ��������Ƶ�þ�Ͻ��߹����ڶ�ҪӦ�����ٴ�������������߽ӽ������߹��ڹ̶����������������������߹����ڶ��������ﵽ����ѧ�������Ա����齫�������Ƶ�þ�Ͻ��߹����ڶ����������߹ǹ���ģ�ͺ��������߹ǵ�������ѧ�������˶Ա��о���������������ʹ���������Ƶ�þ�Ͻ��߹����ڶ��̶����۵��߹Ǻ���ǿ�ȡ��նȡ���Ťת������γ�ʵ���Ͼ��������ھ���������������߹����ڶ����ڹ̶����������߹���ӽ�������������������߹����ڶ����ӣ���Ϊ�ٴ�ʹ�ö���Ľ��ڳ����Ʒ�����ʱ�����ѧ���Ա����ӽ������Ƥ�ʡ�
�������Ǿ����ᣨ PLA�� �����Ҵ��ᣨ PGA�� �ȿ����ո߷��Ӳ��Ͻ����ٶ����Կ��ƣ����������ˮ�Բ ϸ�������������� ������������֢�����γɣ����ʼ��ѧ���ܲ�����������ڹ̶���Ҫ��ͬʱ��еǿ�Ȳ����� ��������Χ��֯����ά�������߷�Ӧ�ȣ����Ҳ�Ʒ�������ڣ��۸�AZ31B þ�Ͻ�������߹����ڶ�������ֲ������ϲ��㣬�������ϲ����˻��α�������ƣ���������߹ǽ�������������ǻ��Բ�ε�����������Ч�����غɲ�����Ӧ���ֲ����ȵ����⣬��ƽ״ʹ��ֲ���߹ǹ���ǻ�ھ��п�Ťת���á���һ���ص��Ƕ���������������������£�ķ������̣�ʹ��ֲ���߹ǹ���ǻ�ں���н��߹Ƕ϶�������ǣ������ֹ���ѵ����ã�ͬʱ����Ħ������Ťת���ý�һ����ǿ��
������ʵ����� AZ31B þ�Ͻ�������߹����ڶ�����ѧ�������ڸ��ӵ�һ�����Ϳ������߹��ڹ̶����ϡ����ܹ������б�����þ�Ͻ�֧��ֲ��ŮӤ���ڣ������˷ζ�����խ������δ�Ի�����ɲ���Ӱ�죬����þ�Ͻ���Ϊһ��������������ڹ�����δ�������ٴ����顣AZ31B þ�Ͻ�������߹����ڶ��д��ڽ�һ���Ķ���ʵ����и�ȫ����������Ա�Ըò�������ȫ������ۡ�
����
�������ο����ס�
����[1] Nirula R,Diaz JJ Jr,Trunkey DD,et al. Rib fracture repair:indications,technical issues,and future directions[J].World J Surg,2009,33�� 1�� : 14 - 22.
����[2] Alkan A,Metin M,Ozden B,et al. Biomechanical compari-son of plating techniques for fractures of the mandibularcondyle[J]. Br J Oral Maxillofac Surg,2007,45 �� 2�� : 145- 149.
����[3] Jukkala PK,Pohjonen T,Laitinen O,et al. Biodegradationand strength retention of poly L lactide screws in vivo: anexperimental long term study in sheep [J]. Ann ChirGynaecol,2001,90�� 3�� : 219.
����[4] Staigera MP,Pietaka AM. Magnesium and its alloys as or-thopedic biomaterials: a review[J]. Biomaterials,2006,27�� 9�� : 1728 -1734.
����[5] Ullmann B,Reifenrath J,Seitz JM,et al. Influence of thegrain size on the in vivo degradation behaviour of the mag-nesium alloy LAE442[J]. Proc Inst Mech Eng H,2013,227�� 3�� : 317 - 326.
����[6] Kubásek J,Vojt��ch D,Lipov J,et al. Structure,mechanicalproperties,corrosion behavior and cytotoxicity of biode-gradable Mg - X �� X = Sn,Ga,In�� alloys[J]. Mater SciEng C Mater Biol Appl,2013,33�� 4�� : 2421 - 2432.
����[7] Viano DC,Lau IV,Asbury C,et al. Biomechanics of the hu-man chest,abdomen,and pelvis in lateral impact[J]. AccidAnal Prev,1998,21�� 6�� : 553 - 574
����[8] Lee JB,Park HN,Ko WK,et al. Poly�� L - lactic acid�� /hydroxyapatite nanocylinders as nanofibrous structure forbone tissue engineering scaffolds[J]. J Biomed Nanotechn-ol,2013,9�� 3�� : 424 - 429.
����[9] Zartner P,Cesnjevar R,Singer H,et al. First successful im-plantation of a biodegradable metal stent into the left pul-monary artery of a preterm baby[J]. Catheter CardiovascInterv,2005,66�� 4�� : 590 - 594




