
苯甲醛是合成多种化工产品的重要中间体。目前,由甲苯氧化生产苯甲醛的工艺主要是采用乙酸为溶剂、羧酸钴为催化剂的均相催化氧化反应。该法的缺点是反应选择性低、设备易腐蚀以及催化剂难循环使用。因此,开发固体催化剂的甲苯液相氧化制苯甲醛的工作已引起广泛的关注。由于在反应过程中生成的苯甲醛容易被过度氧化成苯甲酸,造成苯甲醛的选择性普遍偏低。因此,开发甲苯氧化制苯甲醛的高选择性催化剂是个挑战性课题。
水滑石是一类具有层状结构的无机材料,在离子交换、吸附分离、催化和医药等领域均有广泛应用。层状双氢氧化物( Layered Double Hydroxides,LDHs) 包括水滑石( Hydrotalcite,HT) 和类水滑石化合物( Hydrotalcite-like compounds,HTLc) 2 种。其结构通式为: [M2 +1 - xM3 +x( OH)2]Am -x / m·nH2O,其中 M2 +和 M3 +为金属阳离子,存在于层板上的八面体的顶点位置。利用其阳离子的可变性,科研人员已合成了大量的水滑石化合物及其焙烧产物( LDOs) 并被应用作不同氧化反应的催化剂。但将此类催化剂用于甲苯选择性氧化制苯甲醛的报道较少,Velu 等采用过氧化氢叔丁醇( TBHP) 为氧化剂,研究了不同原子比的 Mg-Mn-Al 三元水滑石对甲苯选择性氧化合成苯甲醛的催化作用。在优化条件下,甲苯的转化率为14. 3%,苯甲酸的选择性为75%,苯甲醛的选择性为23. 9%。Genti 等以水滑石为前体制备了CoOx/ CoAl2O3混合氧化物,考察了甲苯气相氧化反应的性能,生成苯甲醛的选择性低于 20%。
本文制备了不同 Co/Al 比的 Co/Al-LDHs 及其焙烧氧化物 Co/Al-LDOs,考察了它们对甲苯液相氧化制苯甲醛的催化作用。
1、 实验部分
1. 1 试剂和仪器
Co( NO3)2·6H2O、Al( NO3)3·9H2O、NaOH、Na2CO3、乙腈、TBHP 和甲苯均为分析纯试剂,实验用水为蒸馏水。Vista-AX 型电感耦合等离子体光谱仪( ICP,美国 Varian 公司) ; ASAP2012C 型表面孔吸附仪( BET,美国 Micromeritics 公司) ,N2在 196 ℃测定; D/max 2500 PC 型 X 射线衍射仪( XRD,日本理学公司) ,使用 Cu-Kα( λ = 1. 5402 nm) 射线源,扫描速率 10 min- 1; PROTEGE 460 型傅里叶变换红红外光谱仪( FT-IR,美国 Nicolet 公司) ,固体 KBr 压片法制样,测试范围 4000 ~ 400 cm- 1; GCMS-2010 型气质联用仪( 日本 Shimadzu 公司) ; SUPRA55 型扫描电子显微镜( SEM,德国蔡司公司) ; Chem-BET-3000 型化学吸附仪( CO2-TDP,美国 Quantachrome 公司) ; GC9100 气相色谱仪 ( 科晓公司) ,SE-30 毛细管柱 ( 30 m ×0. 25 mm × 0. 25 μm) ,进样口温度 250 ℃ ,FID( 离子火焰) 检测器,温度 250 ℃ ,N2气为载气。
1. 2 催化剂的制备
按文献方法配制 Co( NO3)2和 Al( NO3)3的一定摩尔比例的混合溶液以及 NaOH 与 Na2CO3的混合溶液。在60 ℃水浴中,剧烈搅拌下同时滴加上述2 种溶液,控制溶液 pH 值恒定为8. 5,滴加完成后继续搅拌30 min,80 ℃陈化24 h,抽滤,用去离子水洗至中性,100 ℃干燥12 h 得产物记为 Cox/ Al-LDHs( x =2,3 和 4) 。上述水滑石在 650 ℃下焙烧 4 h 制备相应的焙烧氧化物,记为 Cox/ Al-LDOs( x = 2,3和 4) 。
1. 3 催化甲苯氧化制苯甲醛
在 100 mL 的四口烧瓶中,加入催化剂100 mg,甲苯0. 6 mL( 5. 43 mmol) ,乙腈 10 mL,磁力搅拌。体系温度为70 ℃下滴加 TBHP 2. 8 g( 70%,21. 7 mmol) ,反应过程中采用气相色谱跟踪反应进程。以正丁醇为内标,用气相色谱测定苯甲醛的产率和选择性。用气质联用仪 GC-MS 对产物进行定性分析。
2、 结果与讨论
2. 1 催化剂的表征
不同 Co/Al 比的水滑石及其焙烧产物的 BET 及 ICP 分析数据列于表 1。ICP 测定 Co/Al 原子比低于投入量,可能由于制备过程中混合物 pH 值较低,Co2 +离子沉淀不完全引起,但不同 Co/Al 原子比的Cox/Al-LDH 中 Co 的含量变化不大。可能因陈化过程中部分 Co2 +氧化成 Co3 +,使制备的水滑石颜色从玫红色变成了灰色。Leroux 等和 Ionescu 等的研究表明,低氧压的情况有利于陈化过程中的氧化。
从表 1 还可以看出,Co/Al-LDOs 的比表面积在焙烧后比 Co/Al-LDHs 有所增大,这主要归因于焙烧后水滑石层间 CO2 -3和表面吸附水的失去。
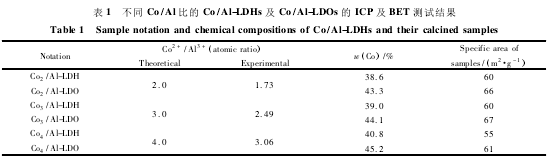
图 1 为不同 Co/Al 比的水滑石在焙烧前后的 XRD 图。从图 1 可以看出,焙烧前 3 种水滑石样品均在低角度出现了相对衍射较强( 003,006,110,113) 特征衍射峰,高角度出现了弱衍射峰( 009,015,018) 。表明 3 个样品均形成了晶相单一、晶体结构一致的水滑石。其 XRD 谱图基线低平,衍射峰峰型窄且尖,结晶度较好,表明 Co2 +被均匀的引入到水滑石结构中。
650 ℃ 焙烧后的 XRD 图( 图 1B) 表明水滑石的晶型被破坏,形成了混合金属氧化物。特征衍射峰显示焙烧后的样品形成了 Co3O4的尖晶石结构( JCPDS 421467) 且没有 Al2O3的特征峰。根据文献报道,XRD 图中的宽峰是由混合3 价金属氧化物: Co3O4、CoAl2O4( JCPDS 440160) 以及 Co2AlO4( JCP-DS 380814) 引起的。
SEM 照片( 图 2) 表明,Co4/ Al-LDHs 形成了片状的团聚晶体,具有明显金属层状化合物的特征。焙烧后的 Co4/ Al-LDO 未发生形貌上的变化,保持层状结构,与文献报道的结果一致。
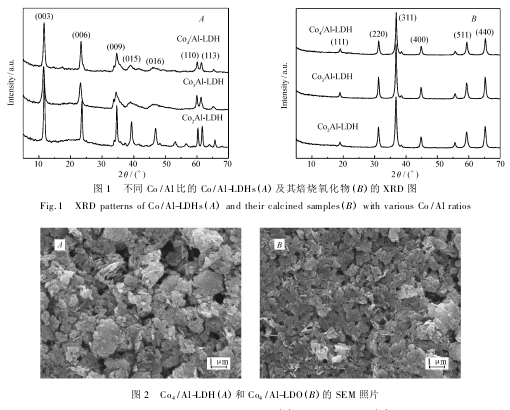
图 3 为 Co4/ Al-LDH 和 Co4/ Al-LDO 的 FT-IR 谱图。Co4/ Al-LDH 在 3498 ~ 3502 cm- 1有大而宽的羟基峰,属于水滑石层间水分子及与 Co、Al 键连的 O—H 振动。在 2800 和 3200 cm- 1之间观察到的肩峰可能是属于水和碳酸根离子之间的氢键。1630 cm- 1附近的宽峰属于层内水分子,这证明了层间水分子的存在。在 1358 cm- 1尖而大的峰是 LDHs 样品的中固定的 CO2 -3的伸缩振动峰。在 757 及 985 cm- 1附近的峰是 Al—OH 的振动吸收峰。由于 LDOs 的混合氧化物对水和二氧化碳敏感。在 1636 cm- 1附近的吸收属于氧化物表面吸附水的羟基氢键的伸缩振动,而在 1383 和 1025 cm- 1附近的弱宽峰是 LDOs表面 O—C—O 的振动。在 665 和 563 cm- 1附近的峰可能是 Al—O 和 Co—O 的振动峰。
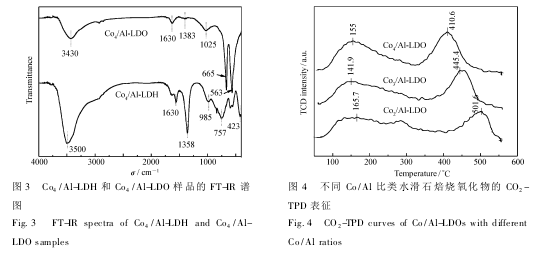
不同 Co/Al 比的 CoAl-LDOs 催化剂的 CO2-TPD 曲线见图 4。由图 4 可见,不同 Co / Al 比的 CoAl-LDOs 均显示了 2 个明显的 CO2脱附峰,分别位于 140 ~166 ℃和 410 ~502 ℃范围内。两个峰依次归属于催化剂表面的弱碱性位和强碱性位吸附的 CO2的脱附。从图 4 可见,随着 Co/Al 比的增加,催化剂的弱碱性位的强度和数量基本保持不变,而强碱性位的强度略有降低,碱位数量明显增加。
2. 2 Co /Al-LDHs 催化甲苯氧化制苯甲醛反应条件的选择以 TBHP 为氧化剂,分别考察了 Co/Al-LDHs 及其焙烧产物对甲苯氧化制苯甲醛的催化性能。GC-MS分析结果表明氧化产物主要为苯甲醛,主要副产物为苯甲醇和苯甲酸。由于在相同条件下不加催化剂甲苯不发生氧化反应,表明类水滑石是催化 TBHP 氧化甲苯的催化剂。
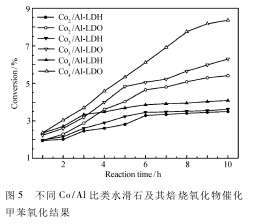
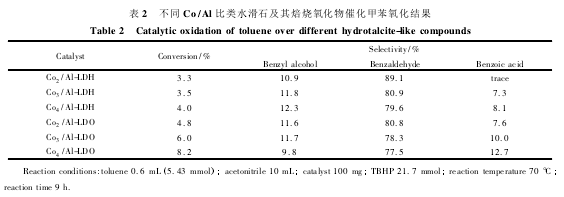
2. 2. 1 催化剂的选择 图 5 和表 2 总结了甲苯的氧化反应结果。从图 5 可以看出,在所选的催化剂条件下,生成苯甲醛的选择性为 75% ~ 85%,高于文献报道值。催化剂中 Co/Al 原子比对苯甲醛的产率和选择性有明显的影响,以 Co/Al-LDHs 和Co / Al-LDOs作为催化剂,随着 Co / Al 比从 2 增加至4,甲苯的转化率明显提高,而苯甲醛的选择性变化较小。这除了受钴含量影响外,可能还与催化剂表面的碱性有关。结合 CO2-TPD 测试结果推测,强碱性位数量的增加对甲苯氧化制苯甲醛反应具有促进作用。
层状结构的水滑石在 650 ℃下焙烧 4 h 后以氧化物的形式存在,焙烧后形成的 Co3O4和 CoAlOx混合物的催化活性明显提高。在相同反应条件下,甲苯的转化率由 4%提高至 8. 2%,而苯甲醛选择性下降不明显。说明甲苯的氧化反应受到其与催化剂表面 Co 物种接触的影响,Co/Al-LDHs 经焙烧后的水滑石的 Co 物种在催化剂表面暴露更充分,催化活性更强。因此,选择 Co/Al-LDOs 为甲苯氧化制苯甲醛的催化剂。
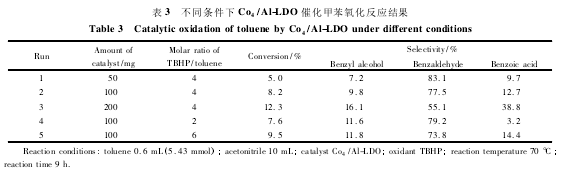
2. 2. 2 催化剂及氧化剂用量的选择 催化剂的用量从 50 mg 增加至 100 mg 时,甲苯的转化率从 5% 升高至 8. 2%,而选择性略有下降。催化剂用量增加至 200 mg 时,虽然甲苯的转化率升至 12. 3%,但苯甲醛的选择性从 77. 5%下降至 55. 1%,苯甲酸的选择性随着催化剂用量的增加显著增加( 表 3) 。故选择催化剂用量为 100 mg,氧化剂 TBHP 用量与甲苯的摩尔比为 4。
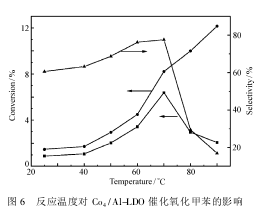
3、 结 论
通过共沉淀法制备了不同 Co/Al 比的类水滑石及其焙烧氧化物,考察了它们对液相催化甲苯氧化反应的性能。结果表明,Co/Al 比为 4 的催化剂在甲苯氧化反应中具有较高的苯甲醛选择性,焙烧后形成的 Co4/ Al-LDO 比不焙烧的 Co4/ Al-LDH 催化活性更高。在优化条件下,甲苯的转化率为 8. 2% ,苯甲醛的选择性达到 77. 5%。催化剂具有良好的重复使用性。
参 考 文 献:
[1]Meng Y,Liang B,Tang S W. A Study on the Liquid-phase Oxidation of Toluene in Ionic Liquids[J]. Appl Catal A: Gen,2012,439 /440: 1-7.
[2]Huang G,Xiang F,Li T M,et al. Selective Oxidation of Toluene over the New Catalyst Cobalt Tetra ( 4-hydroxyl)Phenylporphyrin Supported on Zinc Oxide[J]. Catal Commun,2011,12( 10) : 886-889.
[3]ZHANG Guiquan,ZHANG Xin,QI Min,et al. Superfine Fe-V-O Catalyst for Liquid-Phase Oxidation of Toluene toBenzaldehyde[J]. Chinese J Catal,2012,33( 5) : 870-877( in Chinese) .
张贵泉,张昕,祈敏,等. 超细 Fe-V-O 催化剂上甲苯液相氧化制苯甲醛[J]. 催化学报,2012,33( 5) : 870-877.
[4]LIU Yanxiu,SONG Hua,WANG Baohui. Recent Advances in Synthesis of Benzaldehyde by Oxidizing Toluene Directly[J]. Ind Catal,2005,2( 13) : 25-28( in Chinese) .
柳艳修,宋华,王宝辉. 甲苯直接氧化制苯甲醛研究进展[J]. 工业催化,2005,2( 13) : 25-28.
[5]Xue M W,Yu J N,Chen H,et al. Surface Acidic and Redox Properties of V-Ag-O/TiO2Catalysts for the Selective Oxida-tion of Toluene to Benzaldehyde[J]. Catal Lett,2009,128: 373-378.
[6]Demel J,Lang K. Layered Hydroxide-Porphyrin Hybrid Materials: Synthesis,Structure,and Properties[J]. Eur J InorgChem,2012,2012( 23) : 5154-5164.
[7]Zumreoglu-Karan B,Ay A N. Layered Double Hydroxides-multifunctional Nanomaterials[J]. Chem Pap,2012,66( 1) : 1-10[8]YU Hongli,HAN Caiyun,LI Hongying,et al. Research Progress of Hydrotalcite-like Compounds: Preparation,Characterization and Application[J]. Mater Rev,2013,27( 3) : 59-66( in Chinese) .
禹洪丽,韩彩云,李鸿颍,等. 类水滑石的合成、表征及应用进展[J]. 材料导报,2013,27( 3) : 59-66.
[9]Rives V,Prieto O,Dubey A,et al. Synergistic Effect in the Hydroxylation of Phenol over CoNiAl Ternary Hydrotalcites[J].J Catal,2003,220( 1) : 161-171.
[10]Chmielarz L,Wegrzyn A,Wojciechowska M,et al. Selective Catalytic Oxidation( SCO) of Ammonia to Nitrogen overHydrotalcite Originated Mg-Cu-Fe Mixed Metal Oxides[J]. Catal Lett,2011,141( 9) : 1345-1354.
[11]Zhang F Z,Xiang X,Li F,et al. Observation of Electron-Antineutrino Disappearance at Daya Bay[J]. Catal Surv Asia,2012,108( 17) : 253-260.
[12]Velu S,Shah N,Jyothi T M,et al. Effect of Manganse Substitution on the Physicochemical Properties and Catalytic TolueneOxidation Activities of Mg-Al Layered Double Hydroxide[J]. Micropor Mesopor Mater,1999,33: 61-75.
[13]Centi G,Lanzafame P,Perathoner S. Performances of Co-based Catalysts for the Selective Side Chain Oxidation of Toluenein the Gas Phase[J]. Catal Today,2005,99: 161-170.
[14]Gabrovska M,Edreva-Kardjieva R,Tenchev K,et al. Effect of Co-content on the Structure and Activity of Co-AlHydrotalcite-like Materials as Catalyst Precursors for CO Oxidation[J]. Appl Catal A: Gen,2011,399: 242-251.
[15]Leroux F,Moujahid E M,Taviot-Gu ho C,et al. Effect of Layer Charge Modification for Co Al Layered Double Hydroxides:Study by X-ray Absorption Spectroscopy[J]. Solid State Sci,2001,3: 81-92.
[16] Ionescu R,Pavel OD,Brjega R,et al. Epoxidation of Cyclohexene With H2O2and Acetonitrile Catalyzed by Mg-AlHydrotalcite and Cobalt Modified Hydrotalcites[J]. Catal Lett,2010,134: 309-317.
[17]Sanchez Valente J,Figueras F,Gravelle M,et al. Basic Properties of the Mixed Oxides Obtained by Thermal Decompositionof Hydrotalcites Containing Different Metallic Compositions[J]. J Catal,2000,189: 370-381.
[18]Rives V. Characterisation of Layered Double Hydroxides and Their Decomposition Products[J]. Mater Chem Phys,2002,75: 19-25.
[19]XIE Hui,JIAO Qingze,DUAN Xue. Synthesis of Hydrotalcite by Hydrothermal Method[J]. Chinese J Appl Chem,2001,18( 1) : 70-72( in Chinese) .
谢晖,矫庆泽,段雪. 镁铝型水滑石水热合成[J]. 应用化学,2001,18( 1) : 70-72.
[20]Dupin J C,Martinez H,Guimon C,et al. Intercalation Compounds of Mg-Al Layered Double Hydroxides with Dichlophenac:Different Methods of Preparation and Physicochemical Characterization[J]. Appl Clay Sci,2004,27: 95-106.
[21]Jing F L,Zhang Y Y,Luo S Z,et al. Nano-size MZnAl( M =Cu,Co,Ni) Metal Oxides Obtained by Combining HydrothermalSynthesis with Urea Homogeneous Precipitation Procedures[J]. Appl Clay Sci,2010,48: 203-207.
[22]Velu S,Suzuki K,Hashimoto S,et al. The Effect of Cobalt on the Structural Properties and Reducibility of CuCoZnAlLayered Double Hydroxides and Their Thermally Derived Mixed Oxides[J]. Mater Chem,2001,11: 2049-2060.
[23] Pérez-Ramirez J,Mul G,Kapteijn F,et al. On the Stability of the Thermally Decomposed Co-Al Hydrotalcite AgainstRetrotopotactic Transformation[J]. Mater Res Bull,2001,36( 10) : 1769-1775.
[24]Belló S,Medina F,Tichit D,et al. Study of Alkaline-Doping Agents on the Performance of Reconstructed Mg-AlHydrotalcites in Aldol Condensations[J]. Appl Catal A Gen,2005,281: 191-198.
[25]Greenwell H C,Holliman P J,Jones W,et al. Studies of the Effects of Synthetic Procedure on Base Catalysis UsingHydroxide-Intercalated Layer Double Double Hydroxides[J]. Catal Today,2006,114: 397-402.
[26]LIU Qingqing,LANG Chunyan,HUANG Junzuo,et al. Preparation of Hydrotalcite-Like Compound and Its Calcined Productfor Catalytic Oxidation of Benzene to Phenol[J]. Ind Catal,2012,4( 20) : 60-63( in Chinese) .
刘青青,郎春燕,黄军左,等. 类水滑石的制备及其焙烧产物催化笨制苯酚[J]. 工业催化,2012,4( 20) : 60-63.
[27]Li F,Zhang L H,Evans D G,et al. Structure and Surface Chemistry of Manganese-doped Copperbased Mixed Metal OxidesDerived from Layered Double Hydroxides[J]. Colloids Surf A: Phys Eng Aspects,2004,244: 169-177.
[28]Wang Z P,Shangguan W F,Su J X,et al. Catalytic Oxidation of Diesel Soot on Mixed Oxides Derived from Hydrotalcites[J]. Catal Lett,2006,112: 149-154.
[29]HUANG Dengtong,KE Guoliang,SU Shu,et al. Internal Standard Quantitative Characterization of Basic Sites on Mg-AlHydrotalcites by CO2-TPD-MS Technique[J]. Chinese J Appl Chem,2010,3( 27) : 338-341( in Chinese) .
黄登通; 柯国梁; 苏抒,等. 水滑石型固体碱碱性位的内标 CO2-程序升温脱附-MS 表征[J]. 应用化学,2010,3( 27) : 338-341.
[30] Tyagi B,Sharma U,Jasra R V. Epoxidation of Styrene with Molecular Oxygen over Binary Layered Double HydroxideCatalysts[J]. Appl Catal A: Gen,2011,408: 171-177.







