制药设备论文第七篇:乙酰氨基酚栓剂的生产设备清洁技术探析
摘要:目的 评估对乙酰氨基酚栓生产设备清洁操作完成后设备表面的清洗效果。方法 采用淋洗法、擦拭法进行取样。以目视检查法、化学残留、微生物、清洁剂残留来验证清洁的合理性与有效性。选取最难清洁的部位,清洁剂为50~60℃的0.25%的碳酸钠溶液,对连续3批对乙酰氨基酚栓取样。结果 目检无可见残留物,擦拭法和淋洗法化学残留量均<1.0μg/ml,擦拭法平均回收率为82.1%,RSD为7.6%;淋洗法平均回收率为99.0%,RSD为1.2%。微生物限度均<100 CFU/ml,无清洁剂残留。该清洁方法符合规定的清洁限度要求,不会对将生产的下批产品造成污染或交叉污染。结论 选取50~60℃0.25%的碳酸钠溶液作为清洁剂,适合于对乙酰氨基酚栓生产设备清洁。
关键词:清洁溶剂; 设备; 残留; 微生物限度;
Study on cleaning method of production equipment for paracetamol suppository
LI Min WANG Xiao-sheng FANG Yang-li
Quality Management Section of Zhejiang Jianfeng Pharmaceutical Co., Ltd. Jinhua People's Hospital
Abstract:Objective To evaluate the cleaning effect of the surface of the equipment after the cleaning operation of the acetaminophen suppository production equipment.Methods Sampling was carried out by rinsing method or wiping method. Verify the rationality and effectiveness of cleaning by visual inspection, chemical residues, microbes, and detergent residues. The most difficult to clean parts were selected. The cleaning agent was a 0.25% sodium carbonate solution at 50°C to 60°C, and three consecutive batches of acetaminophen plugs were sampled.Results No visible residue was observed by visual inspection. The chemical residues in the wiping method and the leaching method were all <1.0 μg/ml. The average recovery rate of the wiping method was 82.1%, the RSD was 7.6%, and the average recovery rate of the leaching method was 99.0%. RSD was 1.2%. The microbial limit was <100 CFU/ml, no detergent residue. The cleaning method meets the specified cleaning limit requirements and didn't not cause pollution or cross-contamination of the next batch of products to be produced.Conclusion 50°C to 60°C 0.25% sodium carbonate solution is selected as a cleaning agent, which is suitable for the cleaning of acetaminophen suppository production equipment. This cleaning method is very suitable for the cleaning of acetaminophen suppository production equipment.
对乙酰氨基酚栓用于婴幼儿普通感冒或流行性感冒引起的发热[1],也用于缓解轻至中度疼痛如头痛、关节痛、偏头痛、牙痛、肌肉痛、神经痛。其处方组成为:对乙酰氨基酚和硬脂。活性成分对乙酰氨基酚在热水或乙醇中易溶;硬脂在水或乙醇中几乎不溶,熔点约为34℃,在热水中熔融但不溶于水。其给药方式为直肠给药,已上市的有0.15、0.3、0.6 g规格的栓剂。根据GMP的要求,生产结束后,要对生产设备及操作间进行彻底清洁[2],以避免造成同一产品不同批号或不同品种产品之间的污染和交叉污染。每批生产结束后,对所有在生产中使用的生产设备及容器具进行清洁,清洁后取样检测化学残留及微生物限度。目前国内对栓剂生产过程中的清洁及操作方法有热水清洗法,本研究根据工作实际情况,结合相关法规和行业指导原则,对栓剂生产设备清洁方法做了探索,旨在为栓剂生产设备建立一种有效清洁方法。
1 材料与方法
1.1 仪器与试药
Agilent1260高效液相色谱仪(包括1260 Quat Pump VL溶剂输送泵、1260VWD 检测器、1260 ALS 自动进样器、1260TCC柱温箱、LC solution 色谱数据工作站及电脑);TX?715 型棉签(Texwipe Philippines 公司,批号180711)。对乙酰氨基酚对照品(中国食品药品检定研究院,批号: 100018-201610),水( 滤过纯化水) ,甲醇( Scharlab S.L.,批号:17394825,色谱纯),磷酸氢二钠、磷酸二氢钠,甲醇(国药集团化学试剂有限公司,批号:20170204,分析纯) ,乙醇(浙江汉诺化工科技有限公司,批号:20180101,分析纯)。
1.2 方法
1.2.1 色谱条件
色谱柱:C8,粒径5 μm,4.6 mm×250 mm,柱温:35℃,检测波长为245 nm,流速1.5 ml/min,进样量50 μl。
1.2.2 溶液配制
(1)对照品的配制。取对乙酰氨基酚对照品适量,置于250 ml容量瓶中,加20%乙醇溶解并稀释至刻度,浓度分别为0.989 2 μg/ml。(2)供试品的配制。擦拭法制备:将每个设备取样后的棉签置锥形瓶中,精密量入50 ml水,放置45℃水浴30 min过滤,即得;淋洗法制备:取淋洗水样,过滤,即得;空白棉签制备: 将空白棉签按供试品的配制方法处理。
1.2.3 棉签擦拭方法
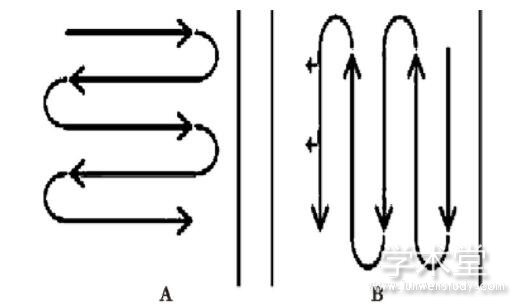
擦拭取样法对于较难清洗可拆卸且能接触到的部位为取样部位[3],通过适当的擦拭,能将清洗过程中溶解度小的成分擦下来。取1支棉签用纯化水浸湿,并将其靠在溶剂瓶上挤压以除去多余的纯化水,用一面按图1A所示,将其棉头按在25 cm2取样表面上,用力使其稍弯曲,平稳而缓慢地擦拭取样表面。在向前移动的同时,将其从一边到另一边,擦拭过程应覆盖整个表面,均匀擦拭10次。翻转棉签,用另一面按图1B所示擦拭,但与前次擦拭方向垂直[4],均匀擦拭10次。每个取样点取1份,取样面积为5 cm×5 cm=25 cm2。见图1。
图1 生产设备关键部位平面取样示例
1.2.4 圆筒形内壁取样擦拭法
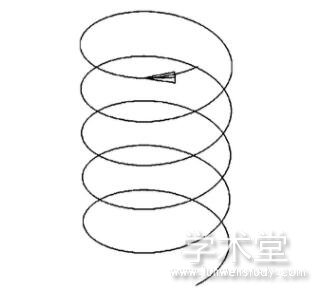
将棉签棉头按在圆筒内壁25 cm2取样表面上,按图2所示,用力使其稍弯曲,平稳而缓慢并呈模孔内表面,直至覆盖整个取样表面,确保完全采样,均匀擦拭10次。
图2 生产设备关键部位圆筒形内壁取样示例
1.2.5 配料罐-淋洗水取样法
淋洗水对于拆卸困难的设备取样,取样面积大,能补充擦拭取样法的缺点。考虑到均质头底部、均质头支柱转接处和配料罐内表面,采用棉签擦拭法取样可操作性不高,因此采用淋洗水法进行取样。取样至少涵盖配料罐的均质头、配料罐内折线处和出料口3个取样点。对均质机按清洗规程有效清洗后,用约54 L的50~60℃纯化水对均质机进行淋洗,收集所有淋洗水。取淋洗水目测:与同体积的纯化水比较,应澄清无色。取淋洗水约100 ml检测化学残留,取淋洗水约500 ml检测微生物。
1.2.6 自动栓剂灌封机加料桶、灌装模块-淋洗水取样法
考虑到灌封机加料桶的搅拌桨底部、桶内表面和出料口等很难采用棉签擦拭法取样,因此采用淋洗水法进行取样。取样至少涵盖加料桶的搅拌桨、加料桶内表面和出料口。对灌封机上的加料桶按清洗规程有效清洗后,用约20 L的50~60℃纯化水对加料桶进行淋洗,淋洗水通过灌装泵输料管后用清洁的不锈钢盆收集,最后将灌装模块装入不锈钢盆中,反复冲洗约2 min,收集所有淋洗水。取淋洗水目测:与同体积的纯化水比较,应澄清无色。取淋洗水约500 ml检测微生物。取淋洗水约100 ml检测化学残留。
2 结 果
2.1 进样精密度试验
取2.2对照溶液连续进样6针,计算平均峰面积擦拭RSD为0.43%,淋洗RSD为0.13%。
2.2 空白溶液干扰试验
将未涂抹对乙酰氨基酚的不锈钢板(约5 cm×5 cm)放入烧杯,加入纯化水100 ml,振摇5 min,制备空白溶液。取空白溶液50 μl注入液相色谱仪,空白溶液不干扰主峰测定。
2.3 线性试验
取对乙酰氨基酚对照品,用20%乙醇溶液分别配制对乙酰氨基酚残留限度(1.0 μg/ml)50%、80%、100%、120%、 150%浓度的对照品溶液,每个浓度平行进样2次,以峰面积为纵坐标,浓度为横坐标,进行线性回归,得回归方程y=136.5x+0.933,r=0.999 5。结果表明,对乙酰氨基酚在0.507 8~1.523 3 μg/m浓度范围内线性关系良好,其最低检测限为4.576 ng/ml,最低定量限为42 ng/ml。
2.4 最高可接受残留限度
化学残留可接受限度的计算方法有两种:生物活性限度(最低日治疗剂量的1/1 000)和浓度限度(10 PPm)[5],分别按两种方法计算对乙酰氨基酚残留限度。
2.4.1 生物活性限度 L1/1000=MTDa/1000×Nb/MDDb×Sb[其中:L1/1000:残留物限度,mg;MTDa:清洗前产品最小每日给药剂量中的活性成分含量,mg;Nb:清洗后产品的批量,mg;MDDb:清洗后产品的最大日给药剂量的活性成分含量,mg;Sb:清洗后产品活性成分含量的百分比(%,w/w)],用L1/1000除以设备表面积(cm2)可算出最大残留限度(μg/cm)。
表1L1/1000和相关参数数据
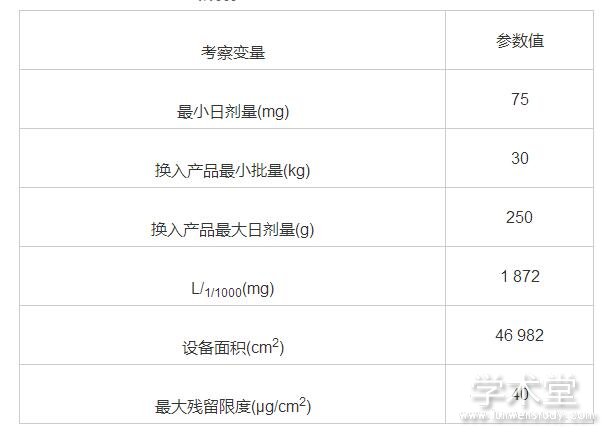
擦拭面积25 cm2,棉签提取溶液10 ml,故棉签擦拭提取溶液的最大允许浓度为100.0 μg /ml。
2.4.2 浓度限度(10PPm)?L=10×10?6×BE×F(10ΡΡm)?L=10×10-6×BE×F,从残留可能性以及限度最低考虑,选择75 mg规格对乙酰氨基酚栓作为清洗前产品,选择250 mg规格对乙酰氨基酚栓作为清洗后产品,清洗后产品的批量为30 kg,安全因子F=10,设备接触面积E=46 982 cm2。可算出浓度限度(10 PPm)为0.638 5 μg/cm2。擦拭面积25 cm2,棉签提取溶液10 ml,故棉签擦拭提取溶液的最大允许浓度为1.6 μg/ml。
比较两种化学残留可接受限度的计算方法可知最大允许浓度1.6 μg/ml。
2.5 微生物限度
按《中国药典》二部(2015年版)纯化水的标准[6],需氧菌总数不超过100 cfu/ml。
2.6 回收率试验
2.6.1 擦拭回收率
用棉签擦拭法取样。取不锈钢板1块(约20 cm×20 cm),与设备材质相同,画线,成若干个5 cm×5 cm方块,按设备清洁标准操作规程对试验材料进行清洁。用无水乙醇配制浓度10.0、20.0 μg/ml的对乙酰氨基酚溶液10 ml,用移液枪吸分别取1 ml,均匀涂抹至25 cm2的不锈钢板上,共涂10块,自然干燥或用冷风吹干不锈钢板。取2根棉签,按2.2项下棉签擦拭方法取样,剪下棉签头放入试管中,加入20%乙醇溶液10 ml,超声得样品。同法取得共6个样品。另取对乙酰氨基酚对照品用20%乙醇溶液稀释制成1.0、2.0 μg/ml的溶液10 ml为对照。1.0 μg/ml擦拭法平均回收率为82.1%,RSD为7.6%;2.0 μg/ml擦拭法平均回收率为81.2%,RSD为4.5%。回收率不低于70%。
2.6.2 淋洗法回收率
用无水乙醇配制浓度为100.0 μg/ml的含对乙酰氨基酚溶液50 ml,用移液枪分别吸取0.5、1.0、1.5 ml各3份,分别均匀涂抹至不锈钢板上,共涂9块,自然干燥或用冷风吹干不锈钢板。将不锈钢板放入烧杯,加入40℃水100 ml,置40℃水浴中振摇5 min,取溶液过滤作为供试品溶液。另取对乙酰氨基酚对照品,用20%乙醇溶液配制成含对乙酰氨基酚1.0 μg/ml的对照品溶液。1.0 μg/ml淋洗法平均回收率为99.0%,RSD为1.2%;0.5 μg/ml淋洗法平均回收率为98.6%,RSD为1.5%;1.5 μg/ml淋洗法平均回收率为96.4%,RSD为2.6%。回收率不低于70%。
2.7 清洁溶剂的选择[7]
在选择清洗溶剂时,不仅要考虑去除设备中残留的前一产品的能力,还要考虑去除生产中可能带入的其他杂质,而且清洗溶剂不得与设备材质本身不相容,不得对设备的材质产生破坏,清洗溶剂本身应安全、无毒、易于清除、经济实惠。因活性成分对乙酰氨基酚在热水或乙醇中易溶;硬脂在水或乙醇中几乎不溶,熔点约为34℃,在热水中熔融但不溶于水;碳酸钠溶液呈碱性,可用于油脂性物料的清洗,碳酸钠易溶于水,本身安全、无毒、经济实惠。因此选择50~60℃的0.25%的碳酸钠溶液作为清洁溶剂。
2.8 SJZ-300型均质机和GZS-9型全自动栓剂灌封机清洗结果
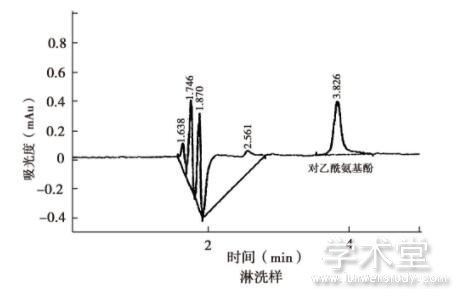
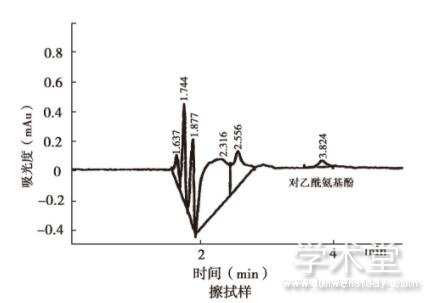
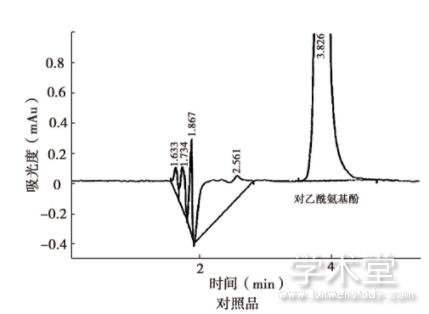
本研究针对对乙酰氨基酚栓片生产过程中涉及的2个设备,包括高效均质机、全自动灌封机。清洗剂为50~60℃的0.25%的碳酸钠溶液。通过对3批对乙酰氨基酚栓产品生产结束后取样检测化学残留、微生物限度、清洁剂残留。目检结果:清洗水与同体积的纯化水比较,澄清无色,符合要求。化学残留结果见图3擦拭样、淋洗样化学残留对乙酰氨基酚峰面积<1.0 μg/m对乙酰氨基酚对照品峰面积,符合要求。清洗剂残留结果:取10 ml淋洗水,加甲基红指示剂2滴,不显红色;另取10 ml,加溴麝香草酚蓝指示剂5滴,不显蓝色,无清洁剂残留。微生物限度结果<100 cfu/ml。
图3 对照品、擦拭样、淋洗样色谱图
3 讨 论
经过清洁验证证明现有的厂房、设施和设备的条件下,依照50~60℃0.25%的碳酸钠溶液作为清洁溶剂清场及清洁后,设备上的化学残留、微生物限度符合规定的清洁限度要求,无清洁剂残留,具有清洁步骤少,清洁方法稳定可靠,可保证再生产药品的疗效、质量和安全性。
欧盟关于公用设施生产不同药品的风险识别中使用的基于健康的暴露限度指南中提到PDE计算方法,此指南不是为了清洁验证而提出的,但其中提出了PDE而被清洁验证所采用,之所以提出PDE的概念,是因为传统的方法,最低日治疗剂量的1/1 000或者浓度限度(10 PPm),所制定的限度忽视了毒理学数据并且可能过于严格或不严格,在残留量确定过程中,现在的说法是指药理实验的半数致死量。半数致死量在一些抗癌药物(高活性的性激素和直接作用细胞的抗肿瘤药品,有非常低的PDE和相应擦拭或冲洗限度值)的使用上是常见的,而本文只生产单一品种对乙酰氨基酚栓,主要成分是对乙酰氨基酚和硬脂,低风险产品可以用1/1 000日剂量来计算,所以残留限度风险可控,10 PPm标准有数据支持,表面交叉污染角度来说能够使患者得到充分保护。清洁验证通常可采取前验证或同步验证形式进行,一般至少进行连续3轮验证来确认清洁程序的有效性是否符合预期[8]
关于清洁验证的分析方法,HPLC法分离效果好,检测灵敏度高,且设备较普及。由于栓剂产品中很多都是有机物,这就为TOC法提供了检测残留的基础。TOC检测具有灵敏度高,且快速便捷,与HPLC法结合能够进一步完善栓剂产品的清洁。
参考文献
[1] 丁柒伶,刘小平.对乙酰氨基酚栓对小儿高热的降温效果观察[J].基层医学论坛,2016,20(31):4409-4410.
[2] 程艳.制药企业工艺设备的清洁规程及清洁验证[J].中国药业,2006,15(9):19-20.
[3] 何国强.制药工艺验证实施手册[M].北京:化学工业出版社,2013:248-249.
[4] 梁毅,丁越.药品生产设备清洁验证关键点的研究[J].中国药房,2012,23(33):3073-3074.
[5] 马肖梦,黄丽敏,许汉林.关于设备清洁残留物限度验证的探讨[J].湖北中医杂志,2016,38(8):69.
[6] 国家药典委员会.中华人民共和国药典[M].四部.北京:中国医药科技出版社,2015:1105.
[7] 赵萌莹.固体制剂生产中的工艺设备及其清洁验证[J].化工管理,2017,33(29):30.
[8] European Medicines Agency.Guideline on processvalidation for finished products-information and data to beprovided in regulatory submissions [EB/OL].[2018-09-10].https://ec.europa.eu/health/sites/health/files/files/eudralex/vol-4/2015-10_annex15.pdf.
点击查看>>制药设备论文(精选范文8篇)其他文章