摘要:智能制造背景下,生物制药行业的MES系统首要实现的目标是如何确保生产合规,其次才是提高生产效率。针对生物制药的行业特点,围绕着如何解决生物制药行业的用户痛点,本文详细介绍了生物制药行业的MES系统设计方案,通过MES系统实现生物制药企业全过程的质量检测管理、贯穿全过程的条码/批号的物料流管理、生产线高度自动化、第三方机构实时监管与不合规操作视频识别判断以及构建药品质量的追溯体系,确保生物制药企业生产合规、生产数据全过程可追溯。
关键词:MES系统;电子批记录;物料追溯;物料族谱;生产合规;视频监控;
Abstract:Under the background of intelligent manufacturing, the first goal of MES system in biopharmaceutical industry is to ensure production compliance, and the second is to improve production efficiency. According to the characteristics of the biopharmaceutical industry, focusing on how to solve the pain points of the users in the biopharmaceutical industry, the design scheme of MES system in the biopharmaceutical industry is introduced in detail. Through the MES system, the whole process quality detection system of the biopharmaceutical enterprise, the material flow management of bar code and batch number throughout the whole process, the high automation of the production line, the thirdparty supervision in time and non-compliance video judgment, and the construction of drug quality traceability system are realized.It ensures the production compliance of Biopharmaceutical Enterprises and the traceability of the whole process of production data.
Keyword:MES system; Electronic batch record; Material traceability; Material genealogy; Production compliance; Video monitoring;
引言
随着国内对于药品生产的过程质量保证要求日趋严格,为确保制药企业持续稳定的生产出适用于预定用途、符合GMP注册批准要求和质量标准的药品,生产过程采用信息化和自动化系统已成为必不可少的有效手段。通过充分运用信息化和自动化,才能真正做到生产过程可控,过程数据真实、准确,批记录实时、可追溯。
《中华人民共和国药品管理法》和《中华人民共和国疫苗管理法》实施后,国家药品监管理局按照《药品生产质量管理规范(2010年修订)》第三百一十条规定,对《生物制品》附录进行了修订。其中附录第59条规定,企业采用实时采集数据的信息化系统记录数据的,因信息化建设需要一定周期,应在2022年7月1日前符合相关要求。因此,生物制品企业采用自动化和信息化手段,实现生产过程数据的电子化记录,建立全生产过程的药品信息追溯体系已经是迫在眉睫的事情。
1 整体解决方案概述
针对生物制药行业的特点以及用户的痛点,生物制药行业MES系统重点需要实现以下4个目标:
(1)医药必须符合药监局的基本思想,并用新技术加固管理方案,使得药品从原料、生产、流通等环节的管理更加刚性有效、可行、高效。
(2)如何利用信息化、物联网和工业互联网技术提高企业生产水平,在底层基础自动化基础上实现全流程监控和实时准确记录,保证质量一致性和均一性。
(3)通过全流程监控,如何通过大数据、互联网技术加强第三方机构监管的实时性、有效性和长期可执行性。
(4)如何实现药品的溯源和生命周期管控。
生物制药行业的MES系统重点解决以下问题:
(1)确保物料流转的准确性,提高生产的一次成功率。
(2)任何产品记录、工艺参数和设备的修改都要进行电子签名和审计跟踪,有效避免纸质记录修改不留痕的高风险行为。
(3)显着减少审查和放行时间,缩短产品到达市场的时间。
(4)生物制药生产区域存在B级(及以上)洁净区,操作人员戴口罩和穿双层洁净服进行电子签名不方便——采用戴口罩人脸识别的电子签名方式。
(5)在人工操作工序(如细胞传代制备)生产监控存在盲区——采用视频监控判断不合规操作行为的方式确保生产合规。
MES系统功能图如图1所示。

图1 MES系统功能图
2 系统架构图
服务器采用的超融合服务器。超融合服务器配置了6个虚拟服务,即MES/LIMS系统的测试环境,MES/LIMS系统的验证环境,MES系统的生产工作环境和生产冗余备用环境,LIMS系统的生产工作环境和生产冗余备用环境,MES系统和LIMS系统配置了测试、验证、和生产环境;确保生产数据的干净、完整和可靠。
整个MES网络由于与OA共用同一网络,采用了万兆核心交互机,与SCADA系统通过工业级网关防火墙进行物理隔离,保证了数据的网络安全。MES现场终端部署了符合洁净区要求的一体机和工业平板。考虑到洁净区的洁净要求,现场终端采用无线通信网络,通过接入交换机、POE交换机和网线AP部署了整个MES网络,保证了生产数据的安全。平板电脑用于现场的生产前检查、电子签名等操作。一体机用于称量配送站,实现物料扫描、称量和条码打印功能。图2为某生物制药企业MES系统架构图。
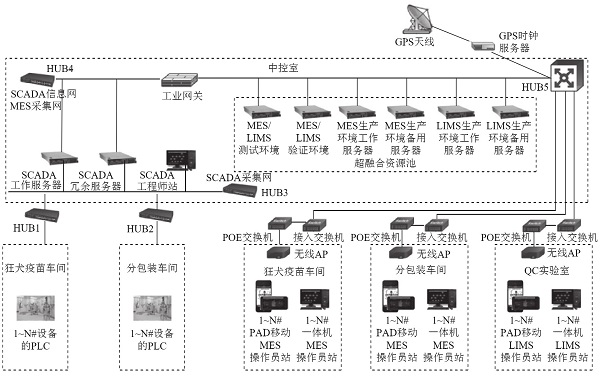
图2 生物制药企业MES系统架构图
3 方案内容
3.1 全过程的质量检测系统——LIMS实验室信息管理模块
原辅料采购、药品生产全过程等都要进行严格的质量管理和检验,原材料入库、半成品和成品生产完成后,LIMS系统自动生成取样和请检任务,自动触发并指导相关人员进行取样和检验,且生成相应的检验记录和检验报告。MES系统在扫描物料条码时,系统能够确保未经检验、检验未合格的物料不能在生产环节中使用;在产品放行时,MES系统能够确保未经检验、检验未合格的物料不能放行出库。实验室系统管理系统如图3所示。
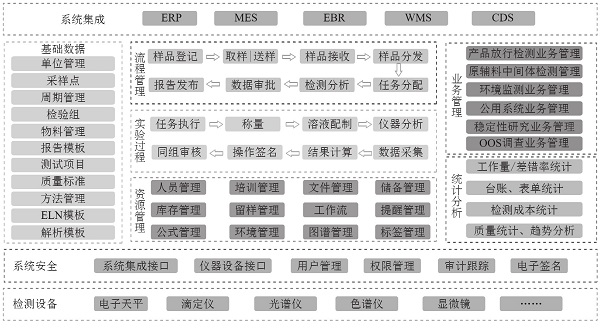
图3 实验室系统管理系统
3.2 贯穿全过程的条码、批号的物料流管理
制药企业通常分为原料仓库(冷库)、生产车间(上、下游工序)和产品仓库(冷库)。如何确保全过程的物料都有相应的条码,只需在仓库入库、称量配送和(半)成品声明3个环节做好物料标签条码打印(或关联IBC容器)即可。
针对原料仓库和成品仓库,按照GMP法规要求,系统实现了如何避免物料混淆存放和使用等(本文采用按件管理,物料盘点、上架、移位等操作采用PDA扫描确认,有效避免物料混淆和使用)。
针对生产车间(上、下游工序),按照GMP法规要求,系统能够确保操作人员严格按照SOP规程进行生产,并实时、准确地生成电子批记录;通过扫描枪扫描目标设备条码、待投物料标签条码可以确保物料流转的一次成功性。全过程物料流管理如图4所示。
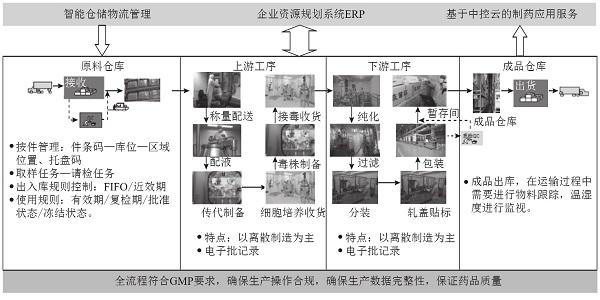
图4 全过程物料流管控
3.3 如何确保各个生产环节的质量均一——基础自动化
从根源杜绝生产数据造假,需要从根本上杜绝人工操作、人工记录,将原有的手动生产进行自动化升级改造,同时将手动检测升级为在线质量检测。自动化生产控制有助于提高药品的质量,保证药品质量的稳定输出、质量均一,如图5所示。
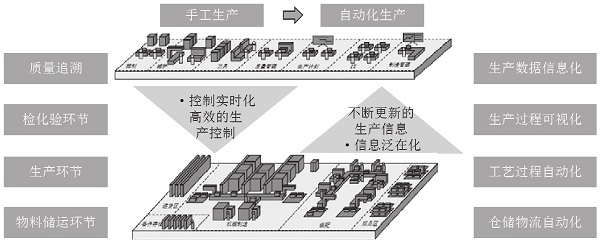
图5 生产全感知和过程自动化
生产车间基础自动化实现之后,DCS系统从MES系统获取工艺参数后,按照工艺参数的控制要求实现自动化控制,该工序生产结束后,MES系统自动记录该工序所需的电子批记录的相关事件数据(如生物反应器定周期获取pH值、溶氧度、温度、压力等),并实时、准确地生成电子批记录。
3.4 第三方监管的实时性与不合规操作视频判断
通过视频监控系统,实时远程监控操作人员是否按照生产规程进行合规化生产。所有的监控视频可长期保存,发生质量事故后可以直观的查看当时生产人员的操作状态。通过电子批记录系统,远程实时浏览各个批次疫苗的电子批记录和检验记录,提高监管的实时性,如图6所示。

图6 视频监控确保生产合规
针对疫苗车间的细胞(或病毒)传代制备工序等无法实现自动化生产的人工操作场合,MES系统在执行该工序生产任务的同时,自动触发该工序的摄像头定位到该工序的生产场所预制点,对该生产任务操作进行视频监控。同时,可以进行不合规生产操作的视频判断并记录,并将视频录像作为电子批记录的附件,以便随时查看。
3.5 构建药品质量的追溯体系(见图7)
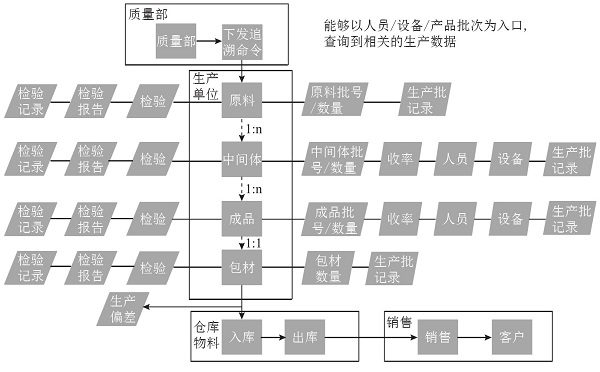
图7 质量追溯体系示意图
M ES系统EBR电子批记录模块的质量追溯功能,能够生成最终产品的物料族谱树、实现生产操作过程的追踪追溯。在药品发生质量问题时候,能够快速查找发生质量问题的原因,确定受影响的相关药品批次,确定快速召回问题药品的范围和影响的大小,实现快速处理应付;而且事后可追查问责到人,增加操作者的责任感,从根源上提升产品质量。安全。
4 结束语
中控技术的医药行业MES产品是符合GMP法规要求,符合cGMP、EU-GMP(ANNEX 11)、FDA 21CFR Part 11等标准规范的生产制造执行系统(MES)软件,以生产制造执行指导、质量管控、电子批记录为核心,对生产线的物料流转、生产过程进行集中管控。它能确保操作人员严格按照医药企业制定的SOP操作规程进行生产,确保药品生产的合规性,保证了药品的质量,保障了患者的安全。
参考文献
[1]李钧,李志宁.药品质量风险管理[M].中国医药科技出版社,2001.
[2]罗文华.药品生产质量管理[M]人民卫生出版社, 2009.
[3]张琪.探索中国物联网之路[M].北京:电子工业出版社,2012.
我国政府及其相关的部门必须要引起生物制药技术方面的重视, 加大支持的力度, 扩大财政资金支撑, 注重生物制药专业人才的培养力度, 为生物制药技术的发展以及成功药物的问世奠定坚实的基础。...
题目:我国生物制药业发展中的问题与对策目录摘要(详见正文)1我国生物产业的现状2我国生物制药业发展存在的问题2.1行业结构因素2.2研发创新不足,对国内知识产权和药品市场的冲击2.3研究停留在实验室且技术成果转化率低2.4政府的财政支持2.5完...
生物发酵制药是传统制药行业中的重要组成部分。随着生物技术和医药技术的发展,我国已成为全球最大的抗生素类药品的生产国与出口国,同时也是抗生素行业对环境造成污染最严重的国家之一。...
1研究背景生物制药是中国战略性新兴产业的重点选择,也是全球高技术产业竞争的焦点[1].目前生物制药企业之间的竞争已转变为供应链之间的竞争,而协同创新是提升供应链竞争能力的有效途径已在生物制药产业成为共识[2].因此,开发出能够加强产学研各关联主体...
随着社会的进步以及科学技术的发展, 人们对蛋白质的研究越来越多, 并且其研究已经发展到前沿领域, 受到了人们的广泛关注。无细胞蛋白表达体系也受到了人们的广泛关注。...
细胞工程为生物制药提供了更多的技术参考与发展空间,促进了我国医药品的研发,为部分疾病的治疗找到了新的治疗方法,提供了一些疾病的治疗效果。...
科学技术在我们如今的医疗方面也已经进行了广泛的运用,并且取得了良好的效果。我国的医学有着悠久的历史,我们五千多年的医学就已经非常的发达了,有很多的文字的记载说明了这一切,像是黄帝内经、本草纲目等等都是我们的瑰宝。手术的麻醉剂在我国很早的时候就...
制药企业加强成本管理是应对当前经济发展环境的重要手段,降低成本是有效扩大利润的行之有效的重要途径。良好的发展环境能扩大就业,增加政府财政收入,促进了社会和谐,稳定了国计民生。...
社会的不断发展、科学的持续进步,鞭策着医疗技术的不断提高。新时代下,国家提高了对生物制药注射剂安全问题的重视程度,提出要加强生物制药注射剂的检验方法,不能只按照是否含有活菌来检验、判断生物制药注射剂,要对其提出更高的、严格的要求,以保证生...
生命科学的快速发展,推动了生物制药的崛起,生物制药产业中包含非常多的技术,动物细胞培养技术即为其中之一,并在此行业中发挥着较大作用。细胞培养技术源于二十世纪初期,在世纪中期规模逐渐扩大,目前在生物制药领域被广泛应用,例如:利用此项技术生产...