摘要: 载体材料的选择对固定化酶的性能有着至关重要的影响。 纳米复合材料不仅具有纳米尺寸的特性,而且可以克服单一材料的不足,在固定化酶领域引起了广泛关注。 本文就目前在固定化酶领域使用的纳米复合载体分类进行了系统的阐述,重点介绍了目前在固定化酶研究领域运用较为广泛的硅基纳米复合材料、 碳基纳米复合材料和纳米纤维复合材料等材料的制备方法及不同材料对酶学性能的影响,并对这些纳米复合材料固定化酶发展前景进行了展望。
关键词: 纳米复合材料; 固定化酶; 硅基材料; 碳基材料。
Abstract: The choice of carrier material has a crucial influence on the performance of the immobilized enzyme.
Nanocomposites, which not only have the properties of nanoscale, but also overcome the shortcoming of a singlematerial, have attracted tremendous attention in the field of immobilized enzyme. In this paper, classifications ofnanocomposite carriers which are currently used in the field of immobilized enzyme are systematically elaborated;the preparation and the significantly enhanced enzymology properties of enzymes immobilized on Si-basednanocomposites, C-based nanocomposites and nanofibers composites are introduced. The outlook of enzymesimmobilized on these nanocomposites is also prospected.
Keywords: nanocomposites; immobilized enzyme; Si-based nanomaterials; C-based nanomaterials.
0引 言。
酶是一种可以高效控制特定化学反应的一种通用的生物催化剂,在实际应用中通常将酶作固定化处理。 固定化酶由于其高稳定性、可重用性、易分离等性质被广泛地应用于化学、生物、农业和医药等领域[1-3]. 酶固定化方法主要包括物理吸附法、共价结合法、包埋法和交联法。 制备固定化酶过程中所采用的固定化技术、载体、介质条件和所催化反应类别会在一定程度上导致酶失活、变性,从而使酶的催化性能或保留活性降低,其中载体所带来的分配效应、空间障碍效应和扩散限制效应是影响固定化酶催化效率的主要因素,因此探寻可行、有效的固定化载体来增强固定化酶的催化性能一直是固定化酶研究的热点[4-6].
纳米尺度的材料由于具有特殊的表面效应、体积效应、 量子尺寸效应和宏观量子隧道效应等,在声、光、电、磁、热性能方面呈现出了新的特性,在全球范围内引起了科学和产业界的极大关注[7]. 与传统大尺寸材料相比, 纳米材料还具有大比表面积、表面易于修饰、与酶分子尺寸相近等优点,作为一种新型的酶固定化载体在生物技术领域得到了广泛关注[8]. 纳米复合材料是由不同性能的纳米材料复合而成,可以有效解决单一纳米材料固定化酶所面临的问题,在保持酶活和增强酶的稳定性等方面有较为突出的表现[9]. 本文对近几年在固定化酶领域所采用的纳米复合材料进行了一个系统的分类,并阐述了纳米复合材料的结构和制备过程及其各组分对固定化酶性能产生的影响。
1硅基纳米复合材料固定化酶研究。
由于高比表面积、高化学纯度、高稳定性、化学惰性、 无毒和易于修饰等优良特性, 以二氧化硅(SiO2) 为代表的纳米硅基材料已经成为广泛使用的酶固定化材料[10].
1.1磁性硅基纳米复合材料固定化酶。
在空气或酸性环境下,磁性纳米粒子(MNPs)的氧化或溶解会大大限制其使用性能, 且由于 MNP之间存在的磁引力易于聚集而影响分散性能,将MNPs 导入硅基纳米材料和将硅基纳米材料覆盖在MNPs 表面形成核壳结构是当前广泛使用的保护方法。 其中核壳结构纳米复合材料具有核壳结构的结合功能和独特的磁性响应率、低毒性和可化学修饰的表面, 在固定化酶领域具有极大的应用潜力,引起了广泛关注[11].
介孔二氧化硅(mSiO2)作为已知发展最为成熟、研究最为透彻的介孔材料具有独特的孔道结构(2~50 nm),不仅有利于大尺寸分子和基团的进入,还因其具有大量纳米级孔道而具有纳米材料的特性。 同时,mSiO2材料如 MCM-41、MCM-48、SBA-15 和介孔泡沫(MCFs)可以增加酶固定化材料的比表面积、提高酶的稳定性和活性,越来越多的研究者将它作为复合材料的基体来制作酶固定化载体[12-13].
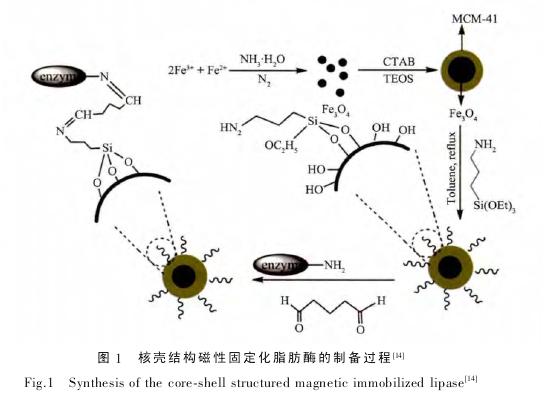
Xie 等[14]首先通过化学共沉淀法获得磁性纳米粒子 Fe3O4,再通过 stober 法在其表面形成介孔材料MCM-41, 从而获得
Fe3O4@MCM-41 核壳结构纳米复合材料(图 1), 然后引入氨基官能团并以戊二醛(GA)为交联剂共价固定褶皱假丝酵母脂肪酶(CRL)。通过透射电子显微镜(TEM)图像分析表明, 具有MCM-41 外壳的复合载体有效地克服了 Fe3O4粒子之间强磁偶极-偶极相互作用。 该法的固定化效率为 76%, 在油脂的 Sn-2 位酯交换反应中保持优良的催化活性和选择性, 催化效率达到 228.2 U·g-1;重复使用性有所提高,经过 5 次重复使用酶活基本保持不变,饱和磁化强度值为 26.3 emu·g-1,可以通过外加磁场达到简易分离。 类似的,Zhu 等[15]以羧基功能化 SiO2包裹的磁性纳米粒子(
Fe3O4@SiO2-NH2-COOH)为载体共价固定猪胰脂肪酶(PPL),用于脂肪酶抑制剂的筛选。 热重量分析法(TGA)和傅里叶变换红外光谱(FTIR)表征表明,载体成功羧基功能化且通过酰胺键共价固定 PPL 在其表面;振动样品磁强计(VSM)所得磁滞回线分析表明, 载体
Fe3O4@SiO2-NH2-COOH 和 固定化 PPL 拥有高饱和磁感应强度,分别达到 45.75 和 42.25 emu·g-1,相比未羧基化的
Fe3O4@SiO2(51.51 emu·g-1),磁感应强度略有下降。 固定化 PPL 与游离酶相比,酶活性、可重用性、热稳定性和储存稳定性都得到明显提升,其动力学参数 Km值 从 游 离 酶 的 0.29 mmol·L-1变 为 0.02mmol·L-1,Vmax也从 3.16 U·mg-1·min-1提高到 6.40U·mg-1·min-1, 说明固定化后酶与底物的亲和力和催化效率均得到提升。