摘 要: 2013年03月,中国部分城市出现了人感染H7N9禽流感病毒病例,随后H7N9禽流感感染疫情迅速暴发,进而引起全球高度关注,接种疫苗是预防H7N9禽流感病毒大流行最有效的措施。本文对H7N9禽流感疫苗临床前研究进展、临床研究概况及免疫原性评价方法等方面作一综述,旨在为H7N9禽流感疫苗的研发提供参考及借鉴。
关键词: H7N9禽流感病毒; 疫苗; 免疫原性; 临床试验; 评价方法;
Abstract: In March 2013,a novel avian-derived H7N9 influenza virus is emerged in cities of China,causing severe human disease. The rapid outbreak of the avian influenza H7N9 virus caused global concern. Vaccination is considered the most effective method to combat an H7N9 influenza pandemic. This paper mainly reviews the research progress in preclinical development,clinical trials and evaluation criteria of immunogenicity of H7N9 vaccine candidates in order to provide references for the further development.
Keyword: Avian influenza H7N9 virus; Vaccine; Immunogenicity; Clinical trial; Evaluation criteria;
来自猪、禽类等非人宿主的新型流感病毒重配株可能会引起人类感染,对公共健康造成潜在大流行威胁[1]。2013年3月,中国安徽省和上海市的3位市民首次感染多源病毒重配的新型H7N9病毒,并引起严重甚至致命的呼吸道疾病,3~4月达到首次感染高峰。自此,每年的冬春交替季节发生H7N9病毒感染疫情,目前已发生5次H7N9流感大流行疫情[2]。调查发现,大部分患者有明确的活禽市场接触史,活禽市场、多种家禽及小动物混杂圈养环境是导致人群感染的主要来源。虽然已经有药物及相应的诊疗方案用于应对H7N9禽流感疫情,但接种疫苗是防控疫情最有效的措施[1]。本文主要对新型H7N9禽流感疫苗的研究进展作一综述。
1 、新型H7N9禽流感疫苗临床前研究进展
1.1 、传统疫苗
传统疫苗主要包括减毒活疫苗和灭活疫苗。H7N9禽流感传统疫苗以鸡胚或细胞为基质培养流感病毒,经超滤、灭活或裂解等工艺处理制备而成。候选疫苗病毒株,如NIBRG-268、IDCDC-RG32A、IDCDC-RG56B、NIBRG-375等,是以A/Anhui/1/2013、A/Shanghai/2/2013、A/Hong Kong/125/2017、A/Guangdong/17SF003/2016野生H7N9病毒为原型,采用反向遗传学技术构建而成,安全性和有效性已通过WHO评价,能够在BSL-2级别环境使用[3]。个别公司通过培养野生型H7N9禽流感病毒(A/Anhui/1/2013)制备灭活疫苗,HA含量低至0.03μg即可保护小鼠抵御野生型流感病毒侵袭[4],多数H7N9禽流感传统疫苗,采用病毒重配株[5],该重配株包含H7N9禽流感HA、NA基因及另外来自鸡胚适应株A/PR/8/34(H1N1)病毒的6个基因。
1.2 、重组蛋白疫苗
多种表达系统可用于表达流感病毒抗原蛋白,目前主要在昆虫细胞和E.coli中表达全长H7 HA、嵌合HA、HA2亚基或HA1-2球状头部区抗原,以制备重组蛋白候选疫苗[5]。

在Sf9细胞中表达A/Anhui/1/2013(H7N9)株全长、重组H7蛋白(rH7),形成寡聚多形状亚病毒颗粒(subviral particle,SVP),直径约29 nm,具有凝集红细胞能力[6]。5μg rH7 SVP免疫小鼠后,1/5的免疫小鼠产生HI抗体,配伍单磷酸类脂A(monophosphoryl lipid A,MPL)使用,显着增加免疫应答和抗体滴度,100%保护免疫小鼠抵御10倍半数致死量(median lethal dose,MLD50)H7N9病毒(A/Anhui/1/2013)侵袭;15μg rH7 SVP(无佐剂配伍)经肌肉注射方式免疫雪貂3针后,产生高滴度HI抗体,且血清与H9存在交叉反应[6]。
有研究人员将H7胞外区序列与GCN4序列[7]、折叠序列(Foldon)[8]和His标签相融合,并在昆虫细胞中表达、制备嵌合HA抗原,以小鼠为动物模型,评价该嵌合抗原特异性免疫应答和保护效力,结果表明,疫苗候选物具有高度免疫原性,在不使用佐剂的情况下,诱导特异性保护性免疫和长效体液免疫应答[7]。配伍维甲酸诱导蛋白Ⅰ(retinoic acidinducible protein,RIG-I)配体使用,显着增强免疫应答和抗体滴度[9]。
此外,基于H7N9流感病毒HA2亚基的重组疫苗在小鼠体内同样具有免疫效应[10],无佐剂配伍的25μg重组蛋白免疫动物后,与配伍咪喹莫特佐剂组产生一致水平的HA2特异性IgG抗体。
重组蛋白技术的优势之一是可以将病毒HA免疫优势区与佐剂相融合制备嵌合抗原。如将A/chicken/Jiangsu/CZT4/2013(H7N9)病毒HA1-2球状头部区62~284氨基酸分子和沙门菌鞭毛蛋白相融合,制备嵌合H7抗原(HA1-2-fli C),C3H/HeJ小鼠模型试验结果表明,该嵌合抗原诱导高滴度HA1-2特异性IgG和HI抗体[11]。进一步研究结果表明,HA1-2-Flic诱导的免疫保护效应和以聚乙烯亚胺(polyethyleneimine,PEI)佐剂配伍的HA1-2蛋白试验组产生的免疫效果一致[12]。
1.3、 VLP疫苗
1.3.1、 基于杆状病毒/昆虫细胞表达系统的VLP
2013年,H7N9禽流感疫情暴发后,SMITH等[13]研究人员快速制备了整合A/Anhui/1/2013(H7N9)病毒株全长HA、NA基因及A/Indonesia/05/2005(H5N1)病毒株M1基因的重组杆状病毒,进一步表达、纯化,制备了首例H7N9病毒VLP候选疫苗。小鼠动物模型试验结果表明,该候选疫苗具有高度的免疫效应,可以抵御致死剂量的野生型H7N9病毒侵袭。在此基础上,放大生产规模,探索规模化生产工艺,制备符合GMP法规的H7N9病毒VLP疫苗,进行了第1例临床试验[14]。2015年,以雪貂为试验动物,进一步扩大免疫原性评价试验范围,结果表明,该VLP单独使用即具有免疫效果,配伍皂素(ISCOMATRIX)或MatrixM1TM佐剂,显着增强免疫原性、提高抗野生型H7N9病毒侵袭能力,两种佐剂发挥相近的免疫效应[15]。
多数的H7N9 VLP疫苗需要添加佐剂,以诱导高水平的保护应答[5,15],然而,基于HA蛋白(A/Shanghai/1/13或A/Anhui/1/13)和基质蛋白M1[A/Udorn/307/72(H3N2)]的H7N9病毒VLP,不配伍佐剂使用,低剂量抗原(0.03μg HA)单次免疫小鼠,就能保护动物免受致死剂量H7N9病毒侵袭,推测杆状病毒发挥了类似佐剂效应[16]。
此外,有研究人员采用杆状病毒表达系统,共表达H5、H7、H9和H10亚型禽流感病毒HA蛋白、H5N1流感病毒N1蛋白及牛免疫缺陷病毒gag蛋白,制备了H5/H7/H9/H10四价VLP,并以雪貂为动物模型,证实多价VLP具有良好的免疫原性[17,18]。
1.3.2、 基于植物表达系统的VLP
加拿大默迪卡哥(Medicago)制药公司研究人员,以农杆菌渗入法,将携带H7N9流感(A/Hangzhou/1/2013)HA基因的质粒导入本氏烟叶片,表达H7 HA蛋白,进一步收获烟叶并精纯,19 d制备出H7 VLP候选疫苗。小鼠和雪貂动物试验结果表明,未配伍佐剂时,以2针次免疫程序接种小鼠,诱导的体液免疫应答显着增强,产生100%保护率,同时明显降低呼吸道感染的相关症状;以铝佐剂配伍的H7 VLP疫苗,单次免疫雪貂,诱导强烈的体液免疫应答和细胞介导免疫应答,激活抗原特异性的CD3+T细胞,保护雪貂免受致死剂量病毒侵袭[19]。
1.3.3 、基于哺乳动物细胞表达系统的VLP
哺乳动物细胞表达系统具备多种蛋白翻译后修饰功能,可用于制备VLP。将全长流感病毒HA、NA和M1基因[A/Wuxi/1/2013(H7N9)]克隆至pCDNA5.1FRT载体,在293T细胞中共转染重组质粒,经蔗糖密度梯度离心法纯化,制备H7N9流感VLP,并以BALB/c小鼠为实验动物评价免疫原性。ELISA结果表明,小鼠血清具有高水平的特异性IgG;酶联免疫斑点试验(enzyme-linked immunospot assay,ELISPOT)表明,VLP诱导记忆性细胞免疫应答[20]。
1.3.4、 基于原核表达系统的嵌合VLP
为了克服杆状病毒表达系统和哺乳动物细胞表达系统制备方法繁琐、周期长及成本高等缺陷,将H7N9病毒HA基因保守的长α螺旋区(long alpha-helix,LAH)插入乙型肝炎病毒核心蛋白(hepatitis B virus core protein,HBc)载体,进一步在E.coli中表达,制备了嵌合型LAH-HBc VLP。配伍壳聚糖或霍乱毒素B亚单位(CTB)佐剂,经鼻腔免疫小鼠,结果表明,LAH-HBc VLP有效诱导体液免疫和细胞免疫应答,完全保护小鼠免受致死剂量的同源H7N9病毒或异源H3N2病毒侵袭,部分保护异源H1N1病毒侵袭,这为新型H7N9流感疫苗的研发提供了思路[21]。
1.4、 核酸疫苗
核酸疫苗包括DNA疫苗、病毒载体疫苗及RNA疫苗,临床试验证实了DNA疫苗和病毒载体疫苗的安全性、耐受性和免疫原性[22]。
1.4.1 、DNA疫苗
H7N9病毒DNA疫苗介导强烈的特异性保护免疫应答,诱导产生高滴度抗H7N9病毒HI抗体;诱导强烈的多功能CD4和CD8 T细胞记忆应答,免疫DNA疫苗的BALB/c小鼠可抵御H7N9禽流感病毒侵袭且不表现相关症状[23]。CHOI等[24]进一步以BALB/c小鼠为研究对象,采用多种免疫剂量和免疫方式,深入研究H7N9 DNA疫苗免疫原性,HI试验和IFNγELISPOT结果显示,可以有效诱导产生抗体、引起IFNγ应答,抗体几何平均滴度随免疫次数增加而升高,免疫小鼠显示100%保护率和血清转换率。
此外,一项关于H7 DNA疫苗和H7N9灭活疫苗的临床试验[25](见表1)结果证实,DNA疫苗是一种有效预防H7N9禽流感疫情暴发的候选疫苗。
1.4.2、 RNA疫苗
RNA疫苗包括mRNA和自我扩增的RNA复制子(self-amplifying mRNA,SAM)疫苗[22]。通过全球流感共享数据库(global initiative on sharing all influenza data,GISAID)获得H7N9基因组序列后,采用SAM技术,8 d内可完成H7N9禽流感候选疫苗制备[5,26]。
以脂质纳米颗粒(lipid nanoparticles,LNP)传递系统包裹的SAM疫苗(H7/LNP),首次免疫小鼠2周后,6/7的免疫动物发生血清转换阳性,产生H7特异性HI滴度,HI滴度随时间延长而增加[26]。另一科研团队发现,内入核蛋白(nucleoprotein,NP)和M1基因的SAM疫苗制剂,诱导广谱CD8和CD4 T细胞,为H7N9禽流感病毒新型疫苗开发提供了借鉴方法[27]。
BAHI等[28]制备了编码H7N9(A/Anhui/1/2013)HA的mRNA疫苗。HI及微量中和(microneutralization,MN)试验结果表明,H7N9 mRNA疫苗在小鼠、雪貂及非人灵长类动物体内,产生快速强烈的免疫应答。单次免疫H7N9 mRNA可保护小鼠免受致死剂量流感病毒侵袭,使雪貂肺部H7N9病毒滴度降低。
1.4.3 、病毒载体疫苗
当前,已成功研制一系列基于各种病毒载体的H7N9病毒载体候选疫苗[5]。基于改良型痘苗病毒安卡拉株(modified vaccinia virus Ankara,MVA)载体的H7N9禽流感疫苗(MVA-H7-Sh2),单次免疫雪貂可产生免疫应答。经气管注射流感病毒A/Anhui/1/2013,免疫动物未显示严重疾病,而未免疫MVA-H7-Sh2的试验对照组动物,则表现出以特征性肺泡炎为症状的间质性肺炎,同时伴有食欲不振、体重下降、呼吸困难等症状[29]。WANG等[30]将H7N9病毒HA基因克隆至黑猩猩源腺病毒载体AdC68,制备了预防H7N9病毒的重组腺病毒载体疫苗,小鼠和豚鼠的动物试验结果表明,该疫苗完全保护免疫动物抵御野生型H7N9流感病毒侵袭。
此外,有些研究团队以新城疫病毒[31]、副流感病毒5型[32]、水泡性口炎病毒等为载体,制备了预防H7N9流感的病毒载体疫苗。
2、 新型H7N9禽流感疫苗临床研究概况
尽管研究人员开发了多种H7N9禽流感疫苗,且在动物试验中取得了一定的预期结果,但仅有少数候选疫苗进入临床阶段,其中包括病毒样颗粒疫苗(virus like particle,VLP)、流感病毒减毒活疫苗(live-attenuated influenza vaccines,LAIV)、流感病毒灭活疫苗(inactivated influenza vaccine,IIV)、裂解疫苗等,详细信息见表1(数据整理自Clinicaltrials.com)。
3 、新型H7N9禽流感疫苗免疫原性评价
传统的HI及病毒中和(virus neutralization,VN)试验检测方法是在动物模型或临床试验中常用的评价流感病毒免疫原性方法,但基于HI和VN试验的检测结果显示,H7N9流感疫苗的免疫原性偏低[33]。
一项最近的研究表明,无佐剂配伍的灭活H7N7、H7N2、H7N9、H1N1和H3N2抗原免疫BALB/c小鼠后,H7亚型的HI抗体和VN抗体滴度显着低于H1和H3亚型,而ELISA结果却显示相对一致水平的IgG滴度。若以IgG抗体水平评价免疫原性,H7亚型病毒和季节性流感病毒具有一致水平的免疫原性,但H7抗原诱导的HI和VN抗体在总量IgG中,显着低于季节性流感病毒,这说明存在大量的非中和抗体,而非中和抗体同样具有抗病毒侵袭作用[34,35]。产生大量非中和抗体的原因之一是H7N9病毒HA抗原表位的改变,另外一个影响H7N9疫苗免疫原性的因素是HA存在调节性T细胞(Treg)表位,H7N9禽流感病毒通过免疫“伪装”和激活Treg应答,可能导致HA蛋白免疫应答逃避[33]。
表1 新型H7N9禽流感疫苗的临床研究
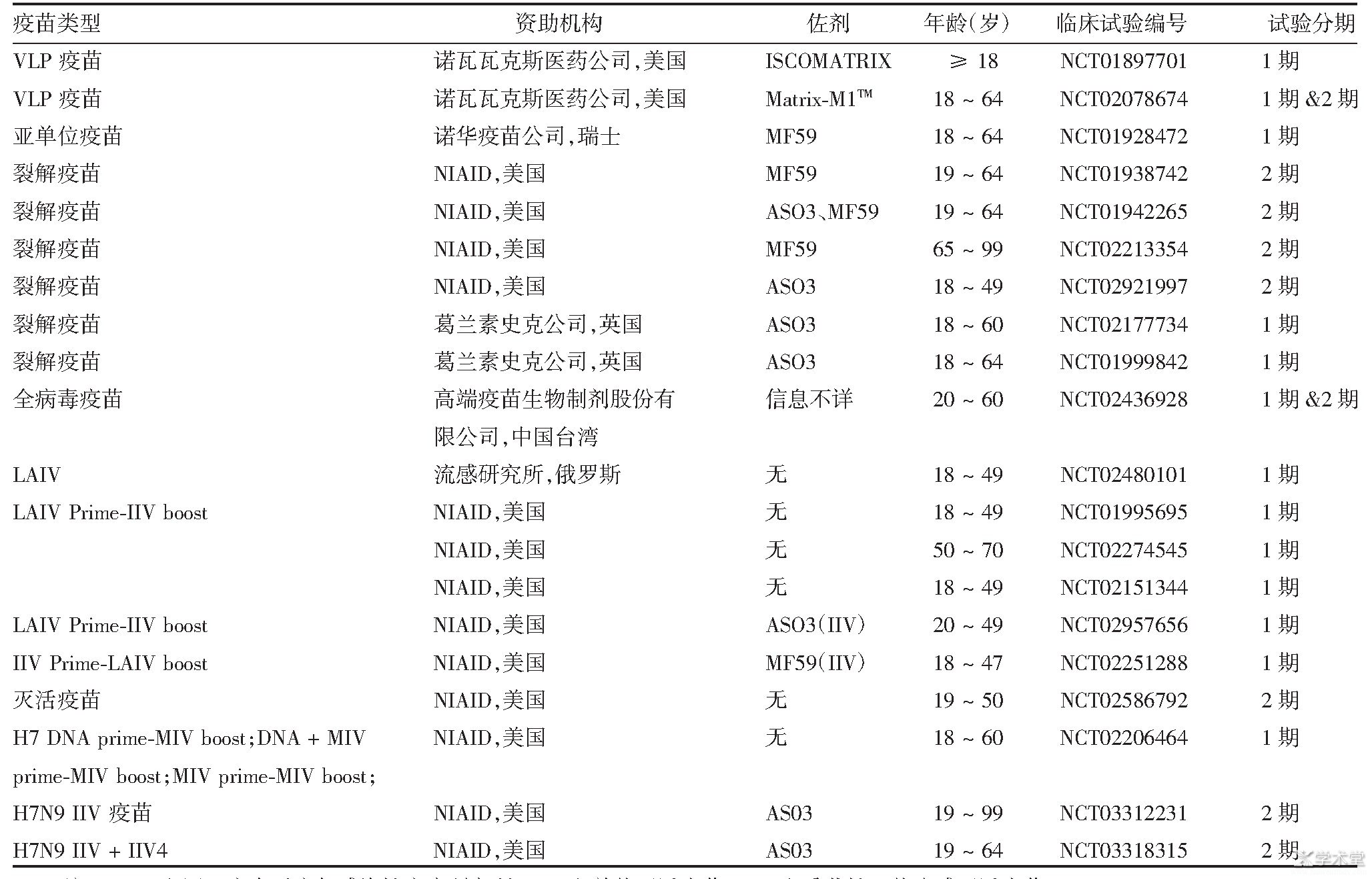
注:NIAID即国立变态反应与感染性疾病研究所;MIV即单价灭活疫苗;IIV4即季节性四价流感灭活疫苗。
4 、总结及展望
H7N9禽流感病毒不能以人传人的模式传播,但鉴于其存在潜在大流行的风险,对H7N9禽流感疫苗的深入、持续研究亟待加强。当前以多种方法和技术开发的H7N9禽流感疫苗,具有相应的优势及劣势,VLP疫苗以其独特的安全性、有效性等特征,在预防H7N9禽流感疫情方面有着更为广阔的发展前景。在设计H7N9禽流感疫苗时,需要重点关注H7N9病毒诱导的非中和抗体的分子机制、免疫程序及如何进一步提高免疫原性等方面。此外,还要考虑佐剂对H7N9禽流感病毒疫苗免疫原性的重要性,除了铝佐剂、ASO3、Matrix-M1TM、MF59等当前正在使用的佐剂,可以使用粒细胞-巨噬细胞集落刺激因子(granulocyte macrophage colony factor,GM-CSF)、鞭毛蛋白等新型分子佐剂,以及将其以膜锚定的形式嵌入VLP,使其深入发挥效应[36,37]。相信随着对H7N9病原学研究的持续深入、新型研究技术在疫苗开发中的广泛运用及国内外科研人员和疾控人员协力合作程度的不断加深[38],人类一定可以快速、有效防控H7N9禽流感病毒疫情。
参考文献
[1]YOO S J,KWON T,LYOO Y S.Challenges of influenza Aviruses in humans and animals and current animal vaccines as an effective control measure[J].Clin Exp Vaccine Res,2018,7(1):1-15.
[2]SU S,GU M,LIU D,et al.Epidemiology,evolution,and pathogenesis of H7N9 influenza viruses in five epidemic waves since 2013 in China[J].Trends Microbiol,2017,25(9):713-728.
[3]WHO.Summary of status of development and availability of avian influenza A(H7N9)candidate vaccine viruses and potency testing reagents[OL].(2018-11-08)[2018-11-08].https://www.who.int/influenza/vaccines/virus/candidates_reagents/summary_a_h7n9_cvv_20181108.pdf?ua=1.
[4]WODAL W,SCHWENDINGER M G,SAVIDIS-DACHO H,et al.Immunogenicity and protective efficacy of a Vero cell culturederived whole-virus H7N9 vaccine in mice and guinea pigs[J].PLoS One,2015,10(2):e0113963.
[5]ISAKOVA-SIVAK I,RUDENKO L.Tackling a novel lethal virus:a focus on H7N9 vaccine development[J].Expert Rev Vaccin,2017,16(7):1-13.
[6]PUSHKO P,PUJANAUSKI L M,SUN X,et al.Recombinant H7 hemagglutinin forms subviral particles that protect mice and ferrets from challenge with H7N9 influenza virus[J].Vaccine,2015,33(38):4975-4982.
[7]WANG L,CHANG T Z,HE Y,et al.Coated protein nanoclusters from influenza H7N9 HA are highly immunogenic and induce robust protective immunity[J].Nanomedicine,2017,13(1):253-262.
[8]YANG H,CARNEY P J,CHANG J C,et al.Structural analysis of the hemagglutinin from the recent 2013 H7N9influenza virus[J].J Virol,2013,87(22):12433-12446.
[9]CAO W,LIEPKALNS J S,KAMAL R P,et al.RIG-I ligand enhances the immunogenicity of recombinant H7HA protein[J].Cell Immunol,2016(304-305):55-58.
[10]TO K K,ZHANG A J,CHAN A S,et al.Recombinant influenza A virus hemagglutinin HA2 subunit protects mice against influenza A(H7N9)virus infection[J].Arch Virol,2015,160(3):777-786.
[11]SONG L,XIONG D,KANG X,et al.An avian influenza A(H7N9)virus vaccine candidate based on the fusion protein of hemagglutinin globular head and Salmonella typhimurium flagellin[J].BMC Biotechnol,2015,15:79.
[12]SONG L,XIONG D,SONG H,et al.Mucosal and systemic immune responses to influenza H7N9 antigen HA1-2 codelivered intranasally with flagellin or polyethyleneimine in mice and chickens[J].Front Immunol,2017,8:326.
[13]SMITH G E,FLYER D C,RAGHUNANDAN R,et al.Development of influenza H7N9 virus like particle(VLP)vaccine:homologous A/Anhui/1/2013(H7N9)protection and heterologous A/chicken/Jalisco/CPA1/2012(H7N3)crossprotection in vaccinated mice challenged with H7N9 virus[J].Vaccine,2013,31(40):4305-4313.
[14]FRIES L F,SMITH G E,GLENN G M.A recombinant viruslike particle influenza A(H7N9)vaccine[J].N Engl J Med,2013,369(26):2564-2566.
[15]LIU Y V,MASSARE M J,PEARCE M B,et al.Recombinant virus-like particles elicit protective immunity against avian influenza A(H7N9)virus infection in ferrets[J].Vaccine,2015,33(18):2152-2158.
[16]KLAUSBERGER M,WILDE M,PALMBERGER D,et al.One-shot vaccination with an insect cell-derived low-dose influenza A H7 virus-like particle preparation protects mice against H7N9 challenge[J].Vaccine,2014,32(3):355-362.
[17]TTRETYAKOVA I,HIDAJAT R,HAMILTON G,et al.Preparation of quadri-subtype influenza virus-like particles using bovine immunodeficiency virus gag protein[J].Virology,2016,487:163-171.
[18]PUSHKO P,SUN X,TRETYAKOVA I,et al.Mono-and quadri-subtype virus-like particles(VLPs)containing H10subtype elicit protective immunity to H10 influenza in a ferret challenge model[J].Vaccine,2016,34(44):5235-5242.
[19]PILLET S,RACINE T,NFON C,et al.Plant-derived H7 VLPvaccine elicits protective immune response against H7N9influenza virus in mice and ferrets[J].Vaccine,2015,33(46):6282-6289.
[20]ZHANG L,LU J,CHEN Y,et al.Characterization of humoral responses induced by an H7N9 influenza virus-like particle vaccine in BALB/C mice[J].Viruses,2015,7(8):4369-4384.
[21]ZHENG D,CHEN S,QU D,et al.Influenza H7N9 LAH-HBc virus-like particle vaccine with adjuvant protects mice against homologous and heterologous influenza viruses[J].Vaccine,201634(51):6464-6471.
[22]ULMER J B,MASON P W,GEALL A,et al.RNA-based vaccines[J].Vaccine,2012,30(30):4414-4418.
[23]YAN J,VILLARREAL D O,RACINE T,et al.Protective immunity to H7N9 influenza viruses elicited by synthetic DNAvaccine[J].Vaccine,2014,32(24):2833-2842.
[24]CHOI E J,LEE H S,NOH J Y,et al.Humoral and cellular immunogenicity induced by avian influenza A(H7N9)DNAvaccine in mice[J].Infect Chemother,2017,49(2):117-122.
[25]DEZURE A D,COATES E E,HU Z,et al.An avian influenza H7 DNA priming vaccine is safe and immunogenic in a randomized phase I clinical trial[J].NPJ Vaccin,2017,2:15.
[26]HEKELE A,BERTHOLET S,ARCHER J,et al.Rapidly produced SAM((R))vaccine against H7N9 influenza is immunogenic in mice[J].Emerg Microbes Infect,2013,2(8):e52.
[27]MAGINI D,GIOVANI C,MANGIAVACCHI S,et al.Selfamplifying m RNA vaccines expressing multiple conserved influenza antigens confer protection against homologous and heterosubtypic viral challenge[J].PLoS One,2016,11(8):e0161193.
[28]BAHL K,SENN J J,YUZHAKOV O,et al.Preclinical and clinical demonstration of immunogenicity by mRNA vaccines against H10N8 and H7N9 influenza viruses[J].Mol Ther,2017,25(6):1316-1327.
[29]KREIJTZ J H,WIERSMA L C,DE GRUYTER H L,et al.Asingle immunization with modified vaccinia virus Ankara-based influenza virus H7 vaccine affords protection in the influenza A(H7N9)pneumonia ferret model[J].J Infect Dis,2015,211(5):791-800.
[30]WANG X,FU W,YUAN S,et al.Both haemagglutininspecific antibody and T cell responses induced by a chimpanzee adenoviral vaccine confer protection against influenza H7N9viral challenge[J].Sci Rep,2017,7(1):1854.
[31]LIU Q,MENA I,MA J,et al.Newcastle disease virusvectored H7 and H5 live vaccines protect chickens from challenge with H7N9 or H5N1 avian influenza viruses[J].J Virol,2015,89(14):7401-7408.
[32]LI Z,GABBARD J D,JOHNSON S,et al.Efficacy of a parainfluenza virus 5(PIV5)-based H7N9 vaccine in mice and guinea pigs:antibody titer towards HA was not a good indicator for protection[J].PLoS One,2015,10(3):e0120355.
[33]HU Z,JIAO X,LIU X.Antibody immunity induced by H7N9avian influenza vaccines:Evaluation criteria,affecting factors,and implications for rational vaccine design[J].Front Microbiol,2017,8:198.
[34]KAMAL R P,BLANCHFIELD K,BELSER J A,et al.Inactivated H7 influenza virus vaccines protect mice despite inducing only low levels of neutralizing antibodies[J].J Virol,2017,91(20):1202-1217.
[35]HENRY DUNAND C J,LEON P E,HUANG M,et al.Both neutralizing and non-neutralizing human H7N9 influenza vaccine-induced monoclonal antibodies confer protection[J].Cell Host Microbe,2016,19(6):800-813.
[36]LIU W C,LIU Y Y,CHEN T H,et al.Multi-subtype influenza virus-like particles incorporated with flagellin and granulocyte-macrophage colony-stimulating factor for vaccine design[J].Antiviral Res,2016,133:110-118.
[37]LIU J,REN Z,WANG H,et al.Influenza virus-like particles composed of conserved influenza proteins and GPI-anchored CCL28/GM-CSF fusion proteins enhance protective immunity against homologous and heterologous viruses[J].Int Immunopharmacol,2018,63:119-128.
[38]GAO G F.From“A”IV to“Z”IKV:Attacks from emerging and re-emerging pathogens[J].Cell,2018,172(6):1157-1159.
布氏菌病(Brucellosis,简称布病)是布氏菌引起的能够在人和动物中传播的一类人兽共患...
在全球女性恶性肿瘤中,宫颈癌发病率位居第二位,仅次于乳腺癌;尖锐湿疣是国内排名第三的性传播疾...
脊髓灰质炎(简称脊灰)是由1、2、3型脊髓灰质炎病毒感染引起的急性传染病,好发于婴幼儿,具有一定的致死率和肢体麻痹后遗症,被医学界称为威胁儿童生命和健康的最大杀手.脊灰病毒通过污染的食物和水传播,并在肠道中增殖,最终侵袭神经系统,导致出现发...
自1998年肠道病毒71型在中国台湾地区引起手足口病暴发以来,HFMD在世界范围呈流行态势,特别在西太平洋地区呈持续高流行态势[1-5].中国2008年-2014年11月,累积报告HFMD11748976例,死亡3210例,其中约90%的重症及死亡病例由EV71引起...
衣原体是一类专一细胞内寄生、不能合成ATP且具有独特发育周期的革兰氏阴性杆菌。它是人兽共患病病原体, 引起的人类疾病相当广泛[1]。它还是一些致病原的辅助因子, 例如可以使Ⅰ型人类免疫缺陷病毒的传播变得更加容易。...
核酸疫苗(nucleicacidvaccine)是一种新型的基因工程疫苗,它将含有编码一种或几种抗原蛋白基因序列的重组质粒导入机体的细胞内,然后在宿主细胞内转录表达抗原蛋白,诱导机体生成相应的细胞免疫应答与体液免疫,接种的机体因此得到了其提供的免疫保护...
布氏菌病(Brucellosis,简称布病)是布氏菌引起的能够在人和动物中传播的一类人兽共患...
PspA作为在各型肺炎链球菌中广泛表达且免疫原性最强的免疫原被广泛应用于融合蛋白疫苗中。...
黄热病是由黄热病毒(yellow fever virus,YFV)引起,主要通过伊蚊叮咬传播的自然疫源性传染病,以高热、头痛、黄疸、蛋白尿和出血等为主要临床表现。全球约有45个非洲和南美洲国家总计超过9亿人口处于黄热病疫区内,每年黄热病病例估计有20万。...
疟疾是以疟原虫为病原体并通过按蚊叮咬传播的寄生虫病,是世界上分布和流行最广的寄生虫性疾病之一,世界上约有20亿人口生活在疫区[1].在我国,疟疾也是一种严重危害人类生命健康的疾...