
衰老现象在自然界中广泛存在,它是一种内源的逐渐发生的并会对发生个体产生持续性损害的过程.在关于衰老发生的理论假说中,衰老的自由基假说(the free radical theory of aging)自 20 世纪 50年代提出伊始,便受到广泛关注,与端粒酶假说、细胞分裂极限假说等成为推动衰老基础研究的重要假说之一.该假说认为过多的氧化还原活性自由基能够造成生物大分子的氧化损伤,导致衰老.研究发现,伴随衰老的发生发展,线粒体产生的过氧化氢增多,机体氧化损伤增加,而过表达抗氧化酶的转基因果蝇寿命延长,这些结果都支持了衰老的自由基假说.在最近发表的关于衰老标志的综述中,作者列举了基因组不稳定、端粒缩短、表观遗传改变、蛋白质稳态异常、营养感受异常、线粒体功能紊乱、细胞衰老、干细胞耗竭、细胞通讯障碍九个方面的衰老标志,其中基因组不稳定及线粒体功能紊乱与活性氧有直接关系,其他方面也存在间接调控.因此,细胞的氧化还原调控是衰老研究中的重要问题,衰老过程中氧化还原调控机制的研究对揭示衰老机制和延缓衰老及健康衰老具有重要意义.
1、细胞氧化还原平衡调控与衰老
细胞内有一套完整的氧化系统和还原系统,氧化系统主要包括活性氧 / 活性氮 (ROS/RNS:reactive oxygen/nitrogen species)两大 “家族”, 其中活性氧 (ROS)包括 O2·,HO·,HO2·,H2O2,1O2,RO·,ROO·(R 表示烷基)等,活性氮(RNS)包括NO,ONOO-,NO+,N2O3等.主要产生自线粒体、过氧化物酶体、NADPH 氧化酶、 细胞色素 P450、黄嘌呤氧化还原酶系统等,外源主要与紫外线、电离辐射、环境毒素等有关.而还原系统主要包括大分子抗氧化酶类(如:超氧化物歧化酶、过氧化氢酶、谷胱甘肽过氧化物酶等)和小分子抗氧化剂(如:谷胱甘肽、维生素 C、维生素 E 等).硫氧还蛋白系统和谷氧还蛋白系统是重要的內源抗氧化系统.二硫键异构酶 PDI 及热休克蛋白也在氧化还原平衡调控中有重要作用.正常情况下,氧化系统与还原系统处于有机平衡,细胞功能正常.一旦氧化系统与还原系统失去平衡,细胞氧化还原环境受到破坏,表现出应激和功能异常,持续不平衡将导致衰老及相关疾病,如:动脉硬化、糖尿病、癌症、神经退行性疾病等都与氧化还原失衡密切相关.尤其是氧化损伤占主导时,生物大分子功能受到破坏,导致衰老发生,即自由基衰老学说的核心思想 (图 1).
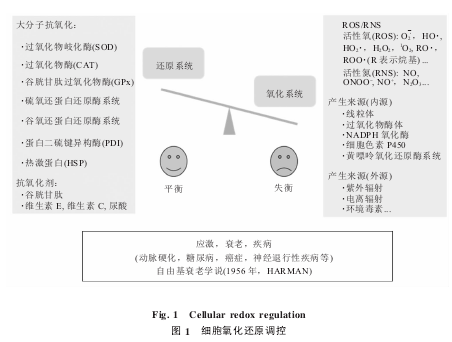
氧化还原平衡调控与衰老密切相关.超氧化物歧化酶 SOD 对于细胞氧化还原平衡的维持至关重要,过表达 SOD 能够延长果蝇寿命; SOD2 敲除的 MEF 细胞及小鼠皮肤较之野生型细胞更易发生损伤与老化.过氧化氢酶(catalase,CAT)作用于SOD下游,是细胞应对氧化应激的重要抗氧化酶之一.CAT 在内皮细胞的病理进程中起重要作用,针对法国人群的研究表明 CAT 能够延缓动脉衰老.
另一类重要的自由基清除蛋白是谷胱甘肽过氧化酶(glutathione peroxidase,GPx),除了能够清除胞内的过氧化氢之外,GPx 还能够清除过氧化的脂质物质,有研究表明其与心血管疾病的发生存在联系.硫氧还蛋白(thioredoxin,TRX)是一个氧化还原酶家族,能够可逆地还原二硫键;通过去除过氧化氢,硫氧还蛋白能够帮助降低细胞氧化应激水平,提高细胞抗氧化能力.氧化后的 TRX 通过硫氧还蛋白还原酶(thioredoxin reductase,TRXR)进行还原再生,TRXR 是一种含硒蛋白,它对 TRX 的还原依赖于 NADPH.同时,硫氧还蛋白结合蛋白2(trx-binding protein-2,TBP-2)能够调控 TRX 的活性.TBP-2 的缺失则会导致脂质代谢失常,这些过程均与衰老过程密切相关.研究发现,参与 GSH生物合成的关键限速酶 GCL 活性会随年龄增长降低,在果蝇中过表达 GCL 能够延长寿命 50%.针对酵母衰老时程的研究表明,在衰老过程早期胞内NADPH急剧减少,继而引发 NADPH 依赖的氧化还原酶(如 TRXR、GR 等)氧化失活,造成氧化还原严重失衡,导致含巯基蛋白的大量氧化,氧化还原严重失衡.
2、氧化还原与信号转导
随着细胞分子生物学的快速发展,人们发现活性氧、活性氮等在细胞信号转导中发挥重要作用,如精原干细胞的自我更新就需要活性氧.一氧化氮自由基(NO)作为气体信号分子,在免疫系统、心脑血管系统和神经系统发挥重要作用.近年研究表明:NO 能够对蛋白质半胱氨酸自由巯基修饰,将—SH 转变为—SNO,即蛋白质巯基亚硝基化修饰. 因此,关于细胞氧化还原调控在生命中的作用及在衰老中的作用需要重新和全面认识.这里以一氧化氮为例阐述其如何通过对蛋白质自由巯基亚硝基化修饰(S-nitrosylation,S-nitrosation)调控蛋白质的功能和信号转导(图 2).
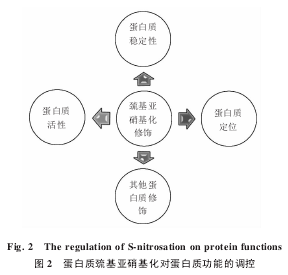
2.1巯基亚硝基化对蛋白质活性的调控
在巯基亚硝基化的早期研究中,很多代谢相关的酶被鉴定为亚硝基化的靶点,这些酶大多具有活性半胱氨酸残基,在亚硝基化的修饰作用下,活性位点受到影响,活性也受到影响,如 GAPDH 的Cys194、谷胱甘肽还原酶(glutathione reductase,GR)的 Cys63、肌酸激酶(creatine kinase, CK) 的Cys283,代谢酶活性的改变导致代谢反应失常.后来越来越多的研究发现,巯基亚硝基化修饰不仅仅影响代谢酶类,许多激酶与磷酸酶、膜受体与离子通道、转录因子的活性也都受到巯基亚硝基化的影响.激酶与磷酸酶的亚硝基化后活性的改变直接影响了磷酸化信号的传递,如JNK、蛋白激酶C (PKC)、蛋白酪氨酸磷酸酶 1B (PTP1B)、PTEN等;膜受体与离子通道的亚硝基化可能会影响信号向下游的传递,如NMDA 受体(NMDAR)亚硝基化后活性降低,抑制了下游信号通路、雷诺定受体(RyR)亚硝基化后活性升高,激活了下游信号通路;亚硝基化能够通过影响转录因子与DNA 的结合来调控其转录活性,如 AP-1、NF-κB的亚硝基化均抑制了其与 DNA 的结合能力.
2.2巯基亚硝基化对蛋白质定位的调控
关于巯基亚硝基化影响蛋白质定位的研究较少,就目前的报道来看,巯基亚硝基化能够影响一些蛋白质在细胞质与细胞核之间的转运.原本定位于细胞质内的代谢酶 GAPDH 亚硝基化之后与Siah1 蛋白结合能力增强,后者的核输入信号导致二者共同向细胞核内转运,巯基亚硝基化解释了不具备核输入信号的GAPDH 入核的机制.巯基亚硝基化对蛋白质定位的调控也是本课题组近年来关注的科学问题,我们的研究发现:NO 通过亚硝基化修饰 93 位以及 310 位半胱氨酸调控 DNA 修复蛋白APE1的核输出,同时破坏了 importin 介导的核输入系统导致 APE1 在核内全部清空;NO 通过对核输出受体蛋白(CRM1)的亚硝基化修饰,削弱了其与核输出信号 NES 的结合,导致对经典核输出通路的抑制.前者是巯基亚硝基化对蛋白质本身定位的影响,后者是巯基亚硝基化通过对核转运蛋白的调控影响其他蛋白质的定位.
2.3巯基亚硝基化对蛋白质稳定性的调控
蛋白质的泛素化途径是调控其稳定性的主要机制之一.巯基亚硝基化修饰可通过影响泛素化途径来调控蛋白质的稳定性.这包括两个层次的意义:
首先,巯基亚硝基化可影响单个蛋白质的泛素化,对于不同的蛋白质,巯基亚硝基化可能促进其泛素化水平,降低蛋白质稳定性,如 FLICE 样抑制蛋白(FLIP),也可能降低其泛素化水平,从而维持该蛋白的稳定性,如缺氧诱导因子 1 (HIF-1)、Bcl-2;其次,泛素化系统中关键酶的巯基亚硝基化会影响其底物的稳定性,如巯基亚硝基化抑制了泛素 E3 连接酶 Parkin 的活性,造成其底物蛋白质的降解受到抑制,α-synuclein (α突触核蛋白)、synphilin-1等的大量聚集引起多巴胺能神经元的大量凋亡.
2.4巯基亚硝基化对蛋白质-蛋白质相互作用的调控
生物体细胞内的蛋白质相互作用网络是信号转导和一切生理病理过程发生的基础,巯基亚硝基化对蛋白质相互作用的调控也是亚硝基化行使功能的重要机制之一.GAPDH 由细胞质向细胞核转位之前,巯基亚硝基化增强其与Siah 的相互作用就是亚硝基化影响蛋白质相互作用的例证之一.此外,N- 乙基马来酰亚胺敏感因子(NSF)的亚硝基化能够增强其与AMDA 受体(AMDAR) GluR2 亚基的结合,从而调控 AMDAR 下游信号通路.p53的77位半胱氨酸残基的亚硝基化能够抑制其与泛素E3连接酶 HDM2 结合,避免其被降解.
2.5巯基亚硝基化对蛋白质发生其他类型翻译后修饰的调控
巯基亚硝基化影响其他类型翻译后修饰的情况也普遍存在.巯基亚硝基化通过对激酶或磷酸酶活性的影响,调控其底物的磷酸化水平,造成某种生理或病理上的效应,如在胰岛素抵抗过程中,胰岛素受体、胰岛素受体底物以及 Akt 的酪氨酸磷酸化水平的降低与其亚硝基化水平的升高相关.蛋白质氧化修饰也受到巯基亚硝基化修饰的影响,有报道指出,蛋白质巯基亚硝基化能够抑制其受到不可逆氧化修饰的影响,防止其受到氧化应激的损伤,从而起到保护的作用,如巯基亚硝基化对硫氧还蛋白和 PTP1B的保护作用.此外,组蛋白去乙酰化酶 HDAC2 的巯基亚硝基化能促使其从染色质上解离,增强组蛋白的乙酰化,调控转录,Sumo 化 E3 连接酶 Pias3 的巯基亚硝基化促使其经泛素途径降解,导致细胞 sumo 化整体水平的降低.
巯基亚硝基化对蛋白质其他类型翻译后修饰的调控是信号通路之间发生交互作用(crosstalk)的重要机制.
3、生物大分子氧化损伤与衰老
3.1 DNA的氧化损伤与修复
氧化还原失衡,尤其是当羟自由基这样强氧化的自由基过多时,会造成 DNA 断裂、突变等氧化损伤,8- 羟基 -2′- 脱氧鸟嘌呤核苷(8-hydroxy-2′-deoxyguanosine,8-OHdG)是 DNA 氧化损伤的最主要产物和标记物.细胞具有多种 DNA 损伤响应机制,能够及时感知这些损伤,并启动相应的修复通路进行修复.但是,当这些损伤超出了细胞的修复能力,DNA 突变逐渐积累,细胞基因组稳定性下降.基因组不稳定是衰老过程中的重要标志.另一方面,线粒体作为内源自由基的主要来源之一,线粒体DNA 极易受到氧化损伤.对于多个物种、多个组织的研究均表明,伴随衰老进程,线粒体DNA (mtDNA)突变累积.伴随衰老过程线粒体ROS 增加,细胞氧化应激水平升高,氧化还原敏感的碱基切除修复(base excision repair,BER)关键酶APE-1 由细胞质向细胞核及线粒体转位,以便有效清除DNA 氧化损伤,而过度的氧化损伤可能影响相关修复系统的正常功能,导致 DNA氧化损伤不能及时修复,加速衰老及相关疾病的发展.
3.2蛋白质的氧化损伤与堆积
蛋白质中半胱氨酸、色氨酸、酪氨酸等对氧化还原比较敏感,成为 ROS/RNS 的主要作用靶点,发生多种形式的氧化修饰,一方面直接影响蛋白质的正常功能,另一方面,造成没有功能的蛋白质堆积,导致细胞损伤和死亡.研究较早的是蛋白质羰基化修饰,不饱和醛反应或蛋白质自身氧化导致的蛋白质不可逆羰基化直接影响蛋白质折叠和降解.
从线虫到人类,伴随衰老羰基化蛋白质的水平是增加的.在过氧化亚硝基作用下蛋白质发生酪氨酸硝化,产生 3- 硝基酪氨酸(3-nitrotyrosine,3-NT),也是一种不可逆的氧化损伤.蛋白质巯基不同程度的氧化及磺酸化都可能导致蛋白质堆积和细胞功能异常.研究发现衰老过程中蛋白质降解能力降低、多种酶的催化活性降低.此外,蛋白质氧化的另一个重要来源是脂质过氧化:不饱和脂肪酸受到活性氧和活性氮的攻击产生反应活性高寿命长的脂类自由基以及不饱和醛类,进一步与蛋白质反应损伤细胞的功能.上述蛋白质的异常氧化修饰导致了蛋白质稳态异常,是衰老的重要标志之一.4延缓衰老和健康衰老的氧化还原调控新策略。
延缓衰老和健康衰老一直是人们追求的目标.鉴于氧化还原调控在衰老过程中的重要作用,提出以下几个方面作为新的策略参考:
a.氧化还原平衡的维持.活性氧和活性氮的氧化还原调控是一个“双刃剑”,一方面在有机体中广泛参与细胞的信号转导和生命过程,另一方面能造成生物大分子氧化损伤,影响大分子功能,从而导致衰老及相关疾病的发生.要保持细胞正常的生理功能,重要的是如何保持细胞内的氧化还原平衡,既不能有过度氧化损伤,也不能过度抗氧化而影响正常的氧化还原依赖的信号转导,这在延缓衰老过程中同样重要.
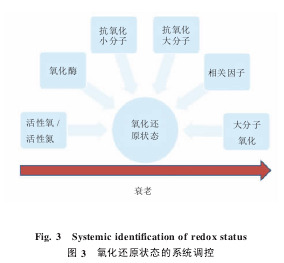
b.氧化还原平衡的系统调控.细胞的氧化还原状态是一个系统调控,而不是单一哪一个指标就能代表的,比如,活性氧活性氮是经常检测的氧化还原水平的指标,但生物大分子的氧化可能更有功能相关性.经典的氧化酶直接影响氧化还原活性物质的产生,但过渡金属、环境的 pH 值和氧浓度等相关因子也会显著影响细胞的氧化还原水平.小分子抗氧化看起来作用直接,但大分子抗氧化可能更有效率.因此,首要的问题是建立细胞氧化还原状态的定量的系统描述,研究在衰老过程中这些不同参数的变化规律,进而在此基础上系统调控机体的氧化还原平衡,否则,很可能顾此失彼 (图 3).【图3】
c.氧化还原调控的个体化.衰老本身是一个个体化的事件,而每个人的氧化还原状态也是各不相同,衰老过程的氧化还原变化因人而异,因此,衰老过程的氧化还原调控只有实现个体化才能真正对症下药.这方面的工作任重而道远.5、结 语。
细胞的氧化还原平衡为胞内各种生物大分子行使正常功能提供了稳定的微环境,氧化还原状态变化将直接影响蛋白质的功能,特别是氧化还原敏感的含巯基蛋白质的功能.因此,细胞氧化还原调控与衰老机制不再是简单的“自由基衰老学说”,也不再是简单的抗氧化延缓衰老,氧化还原活性小分子与生物大分子的交互作用(crosstalk)是揭示衰老机制的国际前沿,关键蛋白质的氧化还原修饰异常可能是衰老的重要机制.衰老过程中氧化还原平衡的维持、氧化还原相关基因的调控机制、氧化还原依赖的蛋白质巯基修饰与信号转导、生物大分子氧化损伤的累积与清除、氧化还原平衡的系统调控及氧化还原状态的个体化表征是细胞氧化还原研究的重要内容,将为揭示衰老机制提供重要依据,为延缓衰老和健康衰老提供新的策略.
中性粒细胞在抵抗感染性炎症方面具有重要地位,其中中性粒细胞分泌的丝氨酸蛋白酶(neutrophilserineproteases,NSPs)在清除病原体方面发挥重要作用。蛋白酶3(proteinase3,PR3)是中性粒细胞分泌的主要丝氨酸蛋白酶之一[1],是继人中性...
目前,国内外研究中,基于细胞壁相关酶(几丁质酶、β-1,3葡聚糖酶)活性研究抑制作用的报道较多,但其他酶类研究报道较少,有待进一步研究,从而能更全面、更有力地论证抑菌物质对病原菌的抑制机制。...
绝大多数真核生物的生命活动都离不开氧气,氧气与高等生物体的能量代谢等过程密切相关。氧气分子在代谢中间体、酶和辐射作用下产生活性氧(Reactive oxygen species,ROS),其在正常生理条件下对细胞代谢的调控发挥着至关重要的作用。...
目的研究Rab29在细胞内的分布以及对甲状旁腺激素受体(PTHR)胞内转运的调控作用。方法采用免疫荧光技术观察Rab29在细胞内的分布;细胞内分别转染野生型Rab29和Rab29两种突变型,免疫荧光技术观察3种Rab29在细胞内的分布;细胞内共转染PTHR和Rab29,免疫荧光技...
黄嘌呤氧化酶(xanthineoxidase,XOD),属黄素蛋白酶类,可将次黄嘌呤氧化为黄嘌呤,继续氧化黄嘌呤为尿酸,并产生过氧化氢及超氧化物,是嘌呤代谢的关建酶。可用于检测血清无机磷、血清超氧化物岐化酶活力及胞外黄嘌呤、次黄嘌呤水平。在核苷类药物的合...
前言心肌缺血再灌注损伤(Myocardialischemiareperfusionin-jury,MIRI)是指心肌缺血/缺氧一段时间,当重新恢复血流或血氧供应后,心肌细胞功能代谢障碍及结构破坏反而较缺血/缺氧时进一步加重、心功能进一步恶化的病理生理过程。细胞内既有活性氧等氧...
1铜蓝蛋白的研究概况铜蓝蛋白(EC1.16.3.)又称铜氧化酶,是Holmberg和Laurell于1948年首先从人血清a2-球蛋白中纯化出的一种外观呈蓝色的含铜糖蛋白,命名为铜蓝蛋白(Ceruloplasmin,Cp)[1],随后人们陆续在其他哺乳动物和鱼类中发现了Cp...
细胞内代谢过程除以碳骨架结构改变为主的物质转化外,通常还伴随辅因子介导的能量转移。物质转化和能量转移高度耦合,显着增加了代谢系统的复杂度。氧化还原辅因子通过在氧化态和还原态之间循环再生传递电子,将物质转化途径关联成复杂的代谢网络[1]....
肿瘤已经成为危害人类生命的一种常见疾病,随着磁疗在临床应用的广泛开展,有关磁场对生物机体抗肿瘤细胞的研究也日益增多.但磁场对生物的影响比较复杂,在不同的磁场强度、温度、照射时间等条件下,生物效应会有所不同.通常较强的磁场会抑制生物的生长,而弱磁...