摘 要: 布南色林是一种新型非典型抗精神病药物,是高选择性多巴胺D2/D3及5-羟色胺2A(5-HT2A)受体拮抗剂。该药对精神分裂症疗效明显,不良反应较少,能有效改善精神分裂症患者的阳性、阴性症状和认知缺损症状。本文就布南色林治疗精神分裂症的药理特点和适应证、临床疗效、不良反应及其处理、临床使用原则与方法等方面的研究进展进行综述。
关键词: 布南色林; 精神分裂症; 治疗结果; 安全;
Abstract: Blonanserin, a new atypical antipsychotic drug, is a highly selective dopamine D2/D3 and 5-HT2A receptor antagonist. The drug has obvious curative effect on schizophrenia with fewer adverse reactions. It can effectively improve the positive and negative symptoms and cognitive impairment symptoms of the patients with schizophrenia. This review focused on the pharmacological characteristics, indications, clinical efficacy, adverse reactions and management, principles and methods of clinical use of blonanserin in the treatment of schizophrenia.
Keyword: blonanserin; schizophrenia; treatment outcome; safety;
精神分裂症(schizophrenia)是一种具有较高患病率、显着致残率和沉重社会负担等特点的重大精神疾病[1],其病因及发病机制尚不明确,以阳性症状、阴性症状、情感症状及认知症状为临床特征,主要使用抗精神病药物治疗,绝大多数患者需要终身服药,对个人、家庭和社会造成了极大的负担。自从1952年第一种抗精神病药物氯丙嗪(chlorpromazine)问世,目前全世界已有50多种抗精神病药物用于治疗精神分裂症等精神障碍[2],包括以氯丙嗪为代表的经典抗精神病药物(第一代) 和以氯氮平(clozapine)为代表的非典型抗精神病药物(第二代) 。对两代抗精神病药物荟萃分析发现,4种第二代抗精神病药物[氨磺必利(amisulpride)、氯氮平、奥氮平(olanzapine)和利培酮(risperidone)]对精神分裂症患者症状总体变化、阳性症状及阴性症状比第一代药物更有效[3]。同时,短期和长期临床研究证明显示使用第一代和第二代抗精神病药物均可能损害身体多种系统,包括锥体外系运动系统、糖脂代谢、心血管系统和性功能等[4]。因此仍需要研发新的抗精神病药物,以改善阴性症状和认知症状并提高安全性。布南色林(blonanserin)作为一种有着不同的药理作用机制的新型非典型抗精神病药物,能有效改善精神分裂症患者的阳性、阴性症状和认知症状,成为治疗精神分裂症的新选择。本文基于循证证据综述布南色林治疗精神分裂症的疗效和安全性,规范布南色林临床应用,希冀更多患者获益。
一、药理特点和适应证
布南色林由日本住友制药有限公司开发,已经在日本(2008年)、韩国(2009年)及中国(2017年)获准用于治疗精神分裂症[5]。化学名为2-(4-乙基-1-哌嗪基)-4-(4-氟苯基)-5,6,7,8,9,10-六氢-环辛[b]吡啶,是一种高选择性多巴胺D2/D3及5-羟色胺2A(5-HT2A)受体拮抗剂,对多巴胺D1、D4、D5,5-HT1A、5-HT 2B、 5-HT 2C、5-HT 3~7,肾上腺素α1、α2、β,组胺H1以及毒蕈碱M1受体的亲和力很低[6]。研究表明,布南色林对D2受体的亲和力比氟哌啶醇(haloperidol)高20倍,比利培酮高94倍,对肾上腺素α1受体的体外亲和力比氟哌啶醇低3倍,比利培酮低40倍[6],这也能部分解释布南色林比利培酮较少引起直立性低血压的原因。其活性代谢产物N-去甲基布南色林(N-deethylated blonanserin)对大部分受体的亲和力与布南色林相似。与大多数其他非典型抗精神病药相比,布南色林对D2受体亲和力比5-HT2A受体高好几倍;而与利培酮、奥氮平或阿立哌唑(aripiprazole)相比,布南色林在大鼠体内的D2和D3受体占有率最高,分别为91.5%和76.8%[7],提示其对阴性症状、认知症状或有更好的治疗效果。正电子发射计算机断层显像(PET)提示布南色林给药剂量为12.9~22.1 mg·d-1时,纹状体D2受体占有率为70%~80%[8],另一项PET研究提示布南色林单次给药12 mg时,纹状体D3受体平均占有率为60.8%[9]。

二、治疗精神分裂症临床疗效
1. 急性期治疗
GARCIA等[10]在高加索人群中开展了一项比较布南色林、氟哌啶醇或安慰剂治疗急性期加重的精神分裂症患者(patients with an acute exacerbation of their schizophrenia)疗效研究。共307位患者被随机分为5组,分别接受布南色林2.5 mg·d-1(n=61)、布南色林5 mg·d-1(n=58)、布南色林10 mg·d-1(n=64)、氟哌啶醇10 mg·d-1(n=60)及安慰剂(n=64)治疗。结果显示,治疗6周后,布南色林组阳性与阴性症状量表(PANSS)总评分、临床总体印象评分-严重程度(CGI-S)评分及简明精神病评定量表(BPRS)总评分的改善均显着优于安慰剂组,布南色林可显着改善急性期患者阳性和阴性症状,且起效更快,对阴性症状的改善显着优于氟哌啶醇。与阿立哌唑对照的研究显示布南色林在改善急性期患者精神病症状方面与阿立哌唑相当[11]。一项日本研究纳入43例急性期精神分裂症患者,结果显示布南色林单药治疗可显着改善BPRS评分[12]。另一项日本研究纳入了70例急性期精神分裂症患者,结果显示布南色林治疗8周可改善急性期患者各维度症状,8周时的治疗有效率是75.4%[13]。两项日本上市后的临床真实世界研究分别纳入1 144例急性期患者和152例首发的急性期患者,结果显示布南色林治疗12周可显着降低BPRS评分[14,15]。李华芳等[16]在中国人群中开展了一项随机、双盲、为期8周的临床研究,比较布南色林与利培酮治疗急性期精神分裂症患者的疗效。267位患者随机接受布南色林8~24 mg·d-1(n=131)或利培酮2~6 mg·d-1(n=136)。重复测量的混合效应模型(MMRM)分析结果显示,治疗8周后布南色林组和利培酮组的PANSS总评分、PANSS症状评分、CGI-S评分均显着降低,布南色林在改善中国精神分裂症患者阳性症状与阴性症状方面均与利培酮相当。
2. 巩固维持期治疗
MURASAKI[17]和MIURA[18]在日本开展的两项随机双盲对照研究显示,布南色林可显着改善稳定期精神分裂症患者的精神病症状,疗效与氟哌啶醇或利培酮相当,对于阴性症状的改善显着优于氟哌啶醇。日本多中心真实世界研究以及长期研究均显示布南色林治疗可明显改善稳定期患者阳性和阴性症状,且该改善可一直保持[19,20,21,22],其中MURASAKI[20]开展的长达56周的多中心研究结果显示,治疗52~56周后总体改善率为87%,PANSS总评分及阳性、阴性症状和一般精神病理学评分均有显着改善;其中OSADA等[22]的研究显示布南色林治疗1年的继续服药率为81%,治疗320周的继续服药率为47.6%,患者BPRS评分和一般精神病理学评分均有明显改善。NAKAMURA等[23]总结布南色林在日本7家医院使用经验显示,38例由其他抗精神病药换为布南色林治疗2周后,BPRS总评分显着降低。日本开展的上市后研究显示布南色林治疗1年后,患者BPRS评分有显着改善[24]。KISHI等[25]对布南色林治疗精神分裂症的Meta分析显示,布南色林对阳性症状的改善与利培酮或氟哌啶醇相当,对阴性症状的改善显着优于氟哌啶醇。
3、 改善精神分裂症认知症状
认知症状是精神分裂症核心症状群之一,导致显着的社会功能缺陷和生活质量下降,目前尚无有效治疗认知症状的药物。布南色林对D3受体具有高度亲和力,提示可能可以改善认知症状[7]。动物实验发现,对氯胺酮(ketamine)诱导的13只有执行功能缺陷的狨猴使用布南色林,可逆转D3特异性受体激动剂对执行功能的进一步损害[26]。HUANG等[27]研究发现布南色林通过对D3受体的拮抗作用,增加皮质DA和乙酰胆碱释放,从而改善大鼠的新事物识别功能,改善精神分裂症认知损害。另外,BABA等[7]报道布南色林作为一种D3受体强效拮抗剂在甲基苯丙胺(methamphetamine)诱导的大鼠运动亢进模型中显示出抗精神病疗效。HIDA等[28]报道布南色林可通过抑制D3受体改善苯环己哌啶诱导的小鼠视觉认知记忆损伤。
HORI等[29]评估了不同抗精神病药物对日本急性精神分裂症患者认知功能及社会功能的改善情况,39例患者分别接受布南色林(n=20)或利培酮(n=19)治疗,用简明精神分裂症认知功能测验评价认知功能,用精神疾病患者生活评估量表评价社会功能。结果显示,布南色林治疗后“言语流畅性”及“执行功能”显着改善,利培酮治疗后仅“言语流畅性”有显着改善;布南色林组“日常生活”及“工作技能”评分均显着改善,利培酮组则仅“工作技能”评分显着改善。MIYAKE等[30]评估了布南色林治疗日本精神分裂症患者的认知功能,22例精神分裂症患者随机接受布南色林(n=12)或利培酮(n=10)治疗8周,结果显示接受布南色林治疗的患者言语性记忆(修订版Wechsler记忆量表)和注意处理能力(WAIS-R数字符号评估)均有显着改善。
综上所述,从临床循证证据分析,布南色林适用于急性期(包括精神症状恶化)的精神分裂症患者,尤其是存在有明显阴性症状及认知症状的患者,同样,也适用精神分裂症的维持期治疗。
三、不良反应及其处理
布南色林的常见不良反应为静坐不能、高泌乳素血症、失眠、嗜睡和震颤,很少引发迟发性运动障碍,对于代谢及实验室参数的影响较小[14]。日本真实世界研究显示,布南色林绝大部分不良事件都发生在用药12周以内[24]。长期研究显示,因不良事件中止用药的比例仅为5%[31]。
1、 锥体外系症状
相较于氟哌啶醇,布南色林治疗中锥体外系症状发生率显着较低(75.0% vs. 52.7%,P<0.001)[17]。另外两项分别在日本[18]和韩国[32]进行的研究表明布南色林锥体外系症状的发生率与利培酮相当。
2、对泌乳素的影响
中国[16]、韩国[32]和日本[18]的研究一致显示,相比利培酮,布南色林较少引起泌乳素升高现象。KISHI等[25]进行的Meta分析显示,布南色林组高泌乳素血症风险较低,泌乳素水平显着低于利培酮+帕利哌酮组(SMD=-0.587,95% CI:-0.854~-0.320,P<0.001,I2=0%)。
3 、对代谢的影响
纳入11种抗精神病药及安慰剂(n=3 446)的Meta分析显示,布南色林、氟哌啶醇、安慰剂及利培酮对体重的影响显着优于奥氮平,其中布南色林引发体重增加的风险最低,对糖脂代谢的影响也较小[33]。在中国患者中开展的研究显示布南色林治疗4周对体重的影响显着低于利培酮[16]。
四、临床使用原则与方法
临床使用布南色林,原则上以单一治疗为主,治疗过程中根据患者的病情和身体状况滴定与调整至合适的剂量。
1、 急性期治疗
首发患者原则上以单剂量,从小剂量开始。日本开展的真实世界上市后重点监测发现,首发患者初次用药每日给药剂量为(7.1±3.1)mg·d-1,最终给药剂量为(11.3±5.8)mg·d-1,最高给药剂量为(13.7±6) mg·d-1[15]。据日本的使用经验,首发患者建议以2~4 mg·d-1开始用药,每1~2周增加2 mg·d-1,缓慢增量[34],通常有效剂量范围为8~24 mg·d-1,每日剂量不应超过24 mg[34]。复发患者建议起始剂量为4~8 mg·d-1,每周增加4 mg,有效剂量范围一般为8~24 mg·d-1,每日剂量不应超过24 mg。对于幻觉妄想症状明显的急性期患者,建议的每日用量为16~24 mg。此外,使用布南色林后,可能出现失眠和兴奋,因此可考虑处方顿服安眠药或苯二氮?类药物,晚上发作时可妥善对应,也可消除家属的顾虑。
2、 巩固期及维持期治疗
巩固期治疗仍以急性期治疗有效的剂量继续治疗,疗程至少3~6个月。维持期治疗根据个体及所用药物情况,使用有效的治疗剂量,继续治疗3~5年。日本长达一年的真实世界研究显示布南色林的平均最终治疗剂量是12.8 mg·d-1,且剂量并不随着时间而增加[20]。另一项日本长期研究显示,布南色林的最终治疗剂量为(14.2±6.3) mg·d-1[22]。
3、 换药
临床上经一种抗精神病药足量足疗程治疗而疗效差或不能耐受时需换用另一种药物。对于以下患者可考虑换用布南色林:(1)目前正在使用典型抗精神病药或非典型抗精神病药,但受过度镇静、体重增加、直立性低血压和QTc延长等不良反应困扰的患者;(2)目前使用的药物对阳性症状或认知症状改善不佳的患者;(3)以改善社会功能为目标的患者;(4)尝试更换药物的患者。
根据布南色林在日本使用的临床经验[34],不同药物换用布南色林的方法建议如下:(1)从利培酮或氟哌啶醇等高效价抗精神病药改用布南色林时,建议采用追加后剂量渐减法或剂量渐减/渐增法(图1A);(2)从奥氮平和喹硫平等多受体作用的抗精神病药改用布南色林时,建议采用平台换药法(图1B);(3)从D2受体部分激动剂阿立哌唑改用布南色林的方法是采用追加后剂量渐减法或剂量渐减/渐增法(图1),也有专家认为可采用快速中断渐增法(图1C)。从日本临床使用统计结果来看,从阿立哌唑改用布南色林的方法支持顺序是剂量渐减/渐增法(43%)、追加后剂量渐减法(34%)、快速中断渐增法(23%)。布南色林的镇静作用较弱,因此从已处方多种药物或强镇静作用药物改用布南色林时,需注意撤药反应。此时,应减缓更换速度或追加抗焦虑药,且心理社会支持也很重要。伴有激烈精神运动性兴奋的病例和严重失眠的病例,由有强镇静作用的抗精神病药换用布南色林时,有可能出现失眠和兴奋、以及阳性症状一过性加剧等。此时,最好短期合用苯二氮?类抗焦虑药或丙戊酸钠等具有安定作用的辅助药物进行处置。
图1 布南色林的给药方法
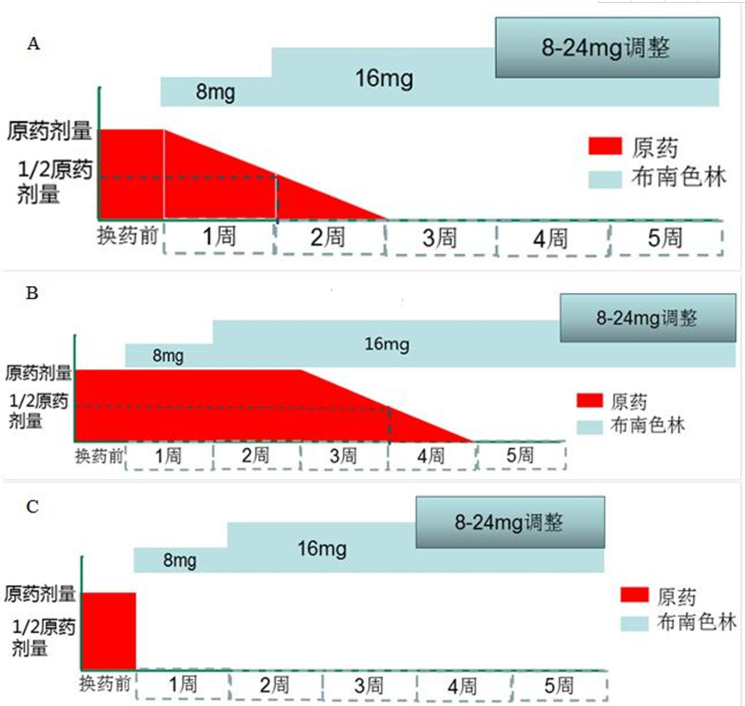
A: 渐减渐增法, B: 平台换药法, C: 快速中断渐增法
五、小结
布南色林具有独特的药理作用机制,为高选择性D2/D3及5-HT2A受体拮抗剂,与其他非典型抗精神病药物比较,其有更高的D2/D3 受体亲和力。临床研究表明布南色林可有效治疗精神分裂症,改善认知功能,且较少引起体重增加、糖脂代谢障碍等抗精神病药常见不良反应。然而,目前布南色林临床应用不够广泛,主要在日本和韩国用于精神分裂症的治疗,在中国人群中的临床研究较少,仅有李华芳等[16]开展了一项比较布南色林与利培酮治疗精神分裂症患者疗效与安全性的研究,其余为布南色林在健康志愿者中药动学方面的研究[35,36]。因此,布南色林对中国精神分裂症患者的疗效、耐受性及安全性有待于进一步深入研究,尤其需要基于大样本的真实世界的研究进行验证。
参考文献
[1]OWEN MJ, SAWA A, MORTENSEN PB. Schizophrenia[J]. Lancet, 2016, 388(10039): 86-97.
[2]GEORGE M, AMRUTHESHWAR R, RAJKUMAR RP, et al. Newer antipsychotics and upcoming molecules for schizophrenia[J]. Eur J Clin Pharmacol, 2013, 69(8): 1497-1509.
[3]LEUCHT S, CORVES C, ARBTER D, et al. Second-generation versus first-generation antipsychotic drugs for schizophrenia: a meta-analysis[J]. Lancet, 2009,373(9657): 31-41.
[4]MOORE TJ, FURBERG CD. The harms of antipsychotic drugs: evidence from key studies[J]. Drug Saf, 2017, 40(1): 3-14.
[5]KISHI T, MATSUI Y, MATSUDA Y, et al. Efficacy, tolerability, and safety of blonanserin in schizophrenia: an updated and extended systematic review and meta-analysis of randomized controlled trials[J]. Pharmacopsychiatry, 2019, 52(2):52-62.
[6]DEEKS ED, KEATING GM. Blonanserin: a review of its use in the management of schizophrenia[J]. CNS Drugs, 2010, 24(1): 65-84.
[7]BABA S, ENOMOTO T, HORISAWA T, et al. Blonanserin extensively occupies rat dopamine D3 receptors at antipsychotic dose range[J]. J pharmacol Sci, 2015, 127(3):326-331.
[8]TATENO A, ARAKAWA R, OKUMURA M, et al. Striatal and extrastriatal dopamine D2 receptor occupancy by a novel antipsychotic, blonanserin: a PET study with [11C]raclopride and [11C]FLB 457 in schizophrenia[J]. J Clin Psychopharmacol, 2013, 33(2):162-169.
[9]TATENO A, SAKAYORI T, KIM WC, et al. Comparison of dopamine D3 and D2 receptor occupancies by a single dose of blonanserin in healthy subjects: a positron emission tomography study with [11C]-(+)-PHNO[J]. Int J Neuropsychopharmacol, 2018, 21(6):522-527.
[10]GARCIA E, ROBERT M, PERIS F, et al. The efficacy and safety of blonanserin compared with haloperidol in acute-phase schizophrenia: a randomized, double-blind, placebo-controlled, multicentre study[J]. CNS drugs, 2009, 23(7):615-625.
[11]KISHI T, MATSUDA Y, MATSUNAGA S, et al. A randomized trial of aripiprazole vs blonanserin for the treatment of acute schizophrenia and related disorders[J]. Neuropsychiatr Dis Treat, 2016,12:3041-3049.
[12]WATANABE H, , SHIMIZU Y, HATA H, et al. Effectiveness of blonanserin in 43 cases of acute phase schizophrenia patients in psychiatric hospitals[J]. Jpn J Clin Psychopharmacol, 2013,16(3):403-414.
[13]TSUTSUMI Y, KASUGA Y, IASKA Y, et al. Effectiveness of blonanserin(BNS) in 70 in-patients with acute phase schizophrenia[J]. Jpn J Clin Psychopharmacol, 2011,14(9):1523-1540.
[14]TSUCHIMORI K, MATSUURA A, KAWAGUCHI N, et al. Results of post-marketing surveillance study of blonanserin in acute exacerbation phase schizophrenic patients—safety and efficacy of blonanserin under administration in daily clinical practice[J]. Jpn J Clin Psychopharmacol, 2017,20(11):1311-1334.
[15]KAWAGUCHI N, NOSAKA T, TANI S, et al. Results of post-marketing surveillance study of blonanserin in antipsychotic-na?ve patients with first-episode schizophrenia—safety and efficacy of blonanserin administered for 12 weeks in daily clinical practice[J]. Jpn J Clin Psychopharmacol, 2016,19(4):471-482.
[16]LI H, YAO C, SHI J, et al. Comparative study of the efficacy and safety between blonanserin and risperidone for the treatment of schizophrenia in Chinese patients: a double-blind, parallel-group multicenter randomized trial[J]. J Psychiatr Res, 2015,69:102-109.
[17]MURASAKI M. Clinical evaluation of blonanserin for schizophrenia: a double-blind trial comparing blonanserin with haloperidol[J]. Jpn J Clin Psychopharmacol,2007,10(11):2059-2079.
[18]MIURA S. Clinical evaluation of blonanserin for schizophrenia: a randomized controlled study comparing blonanserin with risperidone[J]. Jpn J Clin Psychopharmacol, 2008,11(2):297-314.
[19]ISHIGAKI T, AOYAMA H, KNMATA T, et al. Blonanserin: clinical efficacy and safety in schizophrenia, a multicenter naturalistic study[J]. Jpn J Clin Psychopharmacol, 2010,13(12): 2315-2327.
[20]MURASAKI M. Long-term clinical study of blonanserin for schizophrenia: a multicenter open study to determine safety and effectiveness in schizophrenic patients[J]. Jpn J Clin Psychopharmacol, 2007,10(12): 2241-2257.
[21]KINOSHITA T. Long-term clinical study of blonanserin for schizophrenia: a multicenter open study to determine safety and effectiveness in schizophrenic patients(Japan-wide study) [J]. Jpn J Clin Psychopharmacol, 2008,11(1): 135-153.
[22]OSADA K, MIYAMOTO S, MARUTA S, et al. Long-term study of blonanserin for schizophrenia:a multicenter open study to assess the safety and efficacy in patients with schizophrenia[J]. Jpn J Clin Psychopharmacol, 2009,12(11): 2337-2351.
[23]NAKAMURA Y, KAMEI M, KUMA H, et al. Experience with our use of blonanserin, a new antipsychotic drug for schizophrenia in muti-center[J]. Jpn Psychiatr, 2010, 16(6):588-596.
[24]NAGAO M, KAWAGUCHI N, SONODA J, et al. One-year follow-up of a blonanserin post-marketing surveillance study in schizophrenia patients[J]. Jpn J Clin Psychopharmacol, 2016, 19(5):617-631.
[25]KISHI T, MATSUI Y, MATSUDA Y, et al. Efficacy, tolerability, and safety of blonanserin in schizophrenia: an updated and extended systematic review and meta anlysis of randomized controlled trials[J]. Pharmacopsychiatry, 2019, 52(2):52-62.
[26]KOTANI M, ENOMOTO T, MURAI T, et al. The atypical antipsychotic blonanserin reverses (+)-PD-128907- and ketamine-induced deficit in executive function in common marmosets[J]. Behav Brain Res, 2016, 305:212-217.
[27]HUANG M, KWON S, OYAMADA Y, et al. Dopamine D3 receptor antagonism contributes to blonanserin-induced cortical dopamine and acetylcholine efflux and cognitive improvement[J]. Pharmacol Biochem Behav, 2015, 138:49-57.
[28]HIDA H, MOURI A, MORI K, et al. Blonanserin ameliorates phencyclidine-induced visual-recognition memory deficits: the complex mechanism of blonanserin action involving D3-5-HT2A and D1-NMDA receptors in the mPFC[J]. Neuropsychopharmacology, 2015, 40(3):601-613.
[29]HORI H, YAMADA K, KAMADA D, et al. Effect of blonanserin on cognitive and social function in acute phase Japanese schizophrenia compared with risperidone[J]. Neuropsychiatr Dis Treat, 2014, 10:527-533.
[30]MIYAKE N, MIYAMOTO S, TAKEUCHI A. Effect of new-generation antipsychotic blonanserin on cognitive impairment in schizophrenia: a randomized double-blind comparison with risperidone[J]. Jpn J Clin Psychopharmacol, 2008,11(2):315-326.
[31]ISHIGAKI T, SUMIYOSHI A, AOYAMA H, et al. Rates of continuation and safety on long-term clinical study of blonanserin:a multicenter naturalistic study in 40 patients of schizophrenia[J]. Jpn J Clin Psychopharmacol, 2013,16(1): 83-94.
[32]YANG J, BAHK WM, CHO HS, et al. Efficacy and tolerability of blonanserin in the patients with schizophrenia: a randomized, double-blind, risperidone-compared trial[J]. Clin Neuropharmacol, 2010, 33(4):169-175.
[33]KISHI T, IKUTA T, MATSUNAGA S, et al. Comparative efficacy and safety of antipsychotics in the treatment of schizophrenia: a network meta-analysis in a Japanese population[J]. Neuropsychiatr Dis Treat, 2017, 13:1281-1302.
[34] 中村 纯. 抗精神病薬完全マスター[M]. 日本东京都:株式会社 医学书院,2012:160-167.
[35]CHEN X, WANG H, JIANG J, et al. The pharmacokinetic and safety profiles of blonanserin in healthy Chinese volunteers after single fasting doses and single and multiple postprandial doses[J]. Clin Drug Investig, 2014, 34(3):213-222.
[36] 倪晓佳,胡海棠,张 明,等. 布南色林片在中国健康志愿者体内的药代动力学[J]. 中国药科大学学报, 2013, 44(6): 540-542.
有研究表明,选择性的5-羟色胺(5-HT)再摄取抑制剂(SSRIS)等新一代的抗抑郁药物可改善精神分裂症患者的阴性症状.本研究应用舍曲林合并原有抗精神病药物治疗以阴性症状为主的精神分裂症患者。现将研究结果报告如下。1对象与方法1.1对象选自2012-02-01...
精神障碍性疾病是指各种生物学、心理学以及社会环境因素影响下, 造成中枢神经系统功能失调或紊乱, 进而导致出现以认知、情感、意志和行为等各种精神活动异常作为主要临床表现的一类疾病的总称。...
精神分裂症是一组病因未明,以精神活动和环境不协调为特征的精神疾...
氨磺必利因为具有独特的药理作用,对精神分裂症患者的阴性症状和阳性症状都有治疗效果,近几年在临床上使用增多。但虽为新型抗精神病药物,氨磺必利对催乳素水平却有明显升高作用,而高催乳素血症可导致男性性欲下降、阳痿等性功能障碍。国内外目前对经典抗...
精神分裂症归属于精神疾病范畴,在正常人群中患有精神分裂症的几率为1%左右。精神分裂症患者以认知功能障碍为主,临床上主要以药物治疗与心理疏导作为主要治疗方案。...
齐拉西酮与喹硫平作为新型抗精神病药物,在治疗精神分裂症的临床疗效上二者均已获得大家的公认,今将齐拉西酮和喹硫平治疗早期精神分裂症的临床疗效及其不良反应比较报告如下。1、资料与方法1.1、一般资料沈阳市精神卫生中心2013年1月~2014年1月...
难治性精神分裂症患者顽固的阴性症状是长期以来最困扰临床医生、最使患者家属觉得痛苦和无力的难题。患者情感淡漠、动机兴趣缺乏、行为意志退缩,导致家人照顾患者困难,也使患者生活自理能力低下,回归家庭和社会不易。在现有药物体系中,氯氮平是临床医生...
精神分裂症临床表现为症状各异的综合征,涉及思维、情感、感知、行为等多方面的障碍及精神活动的不协调,多在青壮年缓慢或亚急性起病,病程一般迁延且呈反复发作、加重或恶化。药物治疗是精神分裂症治疗的首选方案,相关研究指出,第二代抗精神病药物比...
在社区居住的精神分裂症患者大都存在一些社会功能的损害,如人际交往能力缺陷,兴趣爱好缺乏,生活和工作能力减退等。通过对精神分裂症患者进行绘画艺术训练,鼓励他们运用创造的表达方式,使他们学会如何绘画,激发他们的创造性,以此建立起患者的自信心。艺术治疗...
精神分裂症是危害人类健康最常见的重性精神疾病之一,其终身患病率约为1%,且发病率、复发率和致残率均较高,给社会和家庭带来了沉重的负担。临床上将经过急性期治疗,处于缓解期和巩固期的患者统称为恢复期患者。此期患者常存在疾病知识认知不足、社会功能缺陷...