
1、 实验设计的构想
1.1 设计背景
要培养新型军事人才,能力素质的培养是重中之重。而在传统的化学实验过程中,学员按照教员所讲、教材所写进行实验,实验内容枯燥,实验过程按部就班,最终提交的实验报告也是大同小异。没有了展示自我的舞台,学员的动手积极性自然不高。本次实验让学员做教学过程中的主角,自行组成创新小组,发挥相互协作的团队精神,通过查阅文献资料,自主设计实验流程,在教员的指导下确定合理的实验方案。
1.2 实验的理论依据和研究背景
吡唑类衍生物是天然产物的结构单元,具有广泛的生物活性和药理活性,对各种吡唑类衍生物的合成已成为有机合成的热点之一。而取代的吡唑和稠合吡唑也是重要的药物制品和生物可降解的农用化学品。该类化合物传统的合成方法一般实验过程复杂、实验时间长、后处理不便、产品产率低。本实验尝试将 KF-蒙脱土作为催化剂应用于该类杂环化合物的合成,取得了较好的效果。
蒙脱土结构蓬松,遇热膨胀,可以进行层间离子交换,层与层之间可以插入多种金属配合物,也可以吸附多种化学试剂,对取代、加成、氧化、重排、和还原等反应具有良好的催化性能。目前大多数蒙脱土类催化剂催化的化学反应,一般都在酸性条件下进行,本文探讨将蒙脱土与 KF 交换制成KF-蒙脱土,并将其作为碱性催化剂应用于有机合成,为吡唑类衍生物的合成提供了一种新的快速、简便的方法。
2、 实验设计
2.1 仪器和试剂
XT-5 型显微熔点仪(温度计未校正);双光束红外光谱仪,KBr 压片;Inova-400 MHz 核磁共振仪,DMSO-d6为溶剂,TMS 为内标;所用试剂均为分析纯试剂,KF-蒙脱土按文献制备。
2.2 实验过程
在 50 mL 单口烧瓶中加入取代肉桂腈(1)(2mmol),3-甲基-1-苯基-2-吡唑啉-5-酮(2)(2mmol),KF-蒙脱土(0.25 g)和 DMF(15 mL),在80 ℃下,搅拌 4~6 h,用薄层色谱法跟踪反应,反应结束后,趁热将反应液倒出,过滤,滤液倒入冷水中,沉降,抽滤。滤饼自然风干后,用浓度 95%乙醇重结晶,即得产品 3。吡唑类衍生物的合成过程见图 1。
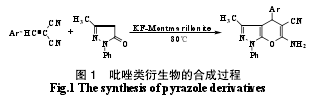
2.3 实验结果与讨论
该反应以 DMF 为溶剂,在温度 80 ℃下,恒温搅拌 4~6 h,生成一系列 1,4-二氢吡喃[2,3-c]吡唑衍生物,产物通过简单的减压抽滤即可分离,反应时间、产率和熔点见表 1。该方法操作简便、产品收率高,为吡唑衍生物的合成提供了一条新的合成途径。

产物的结构经红外光谱、核磁共振氢谱确证。
在红外光谱中在 3 400 cm-1和 3 300 cm-1附近出现NH2的特征吸收峰,同时在 2 200 cm-1附近出现尖而强的特征吸收峰,推测为 CN 吸收峰。在1HNMR 中,在 4.6~5.2 范围内出现共振信号,推测为 C4-H 的特征峰,在 7.20 左右出现特征峰,推测为-NH2的吸收峰,其它核磁共振吸收峰也与产物的结构相符。
产物3a: m.p.: 174-176 °C (Lit.: 173~175 °C);1HNMR (DMSO-d6, δ, 10-6): 1.78 (3H, s, CH3), 3.74 (3H, s,CH3O), 4.63 (1H, s, C4-H), 6.90 (2H, d, J = 8.4 Hz,ArH), 7.16~7.17 (4H, m, NH2+ArH), 7.30~7.34 (1H, m,ArH), 7.47~7.51 (2H, m, ArH), 7.78 (2H, d, J = 8.8 Hz,ArH); IR (KBr, ν, cm-1): 3391, 3322, 2192, 1660, 1596,1514, 1456, 1394, 1250, 1173, 1128, 1073, 1027, 813,759, 692。
产物 3b: m.p.: 199~200 °C (Lit.:198~201°C);1HNMR (DMSO-d6, δ, 10-6): 1.81 (3H, s, CH3), 4.98 (1H, s,C4-H), 7.32~7.52 (5H, m, NH2+ArH), 7.66~7.70 (1H, m,ArH), 7.77~7.81 (3H, m, ArH), 8.15 (2H, d, J = 4.0 Hz,ArH); IR (KBr, ν, cm-1): 3460, 3350, 2194, 1665, 1640,1591, 1580, 1495, 1452, 1387, 1354, 839, 820, 776,746。
产物3c: m.p.: 191~192 °C;1H NMR (DMSO-d6, δ,10-6): 1.79 (3H, s, CH3), 4.73 (1H, s, C4-H), 7.15~7.20(2H, m, ArH), 7.22 (2H, s, NH2), 7.29~7.35 (3H, m,ArH), 7.48~7.52(2H, m, ArH), 7.77~7.80(2H, m, ArH);IR (KBr, ν, cm-1): 3454, 3329, 2203, 1665, 1596, 1518,1494, 1444, 1390, 1264, 1226, 1126, 1068, 1027, 812,753, 685。
产物 3d: m.p.: 193~194 °C(Lit.: 193~195 °C);1H NMR (DMSO-d6, δ, 10-6): 1.83 (3H, s, CH3), 3.73(6H, s, 2×CH3), 4.64 (1H, s, C4-H), 6.75~6.93 (3H, m,ArH), 7.15 (2H, s, NH2), 7.31~7.33 (1H, m, ArH),7.47~7.51 (2H, m, ArH), 7.80 (2H, d, J = 8.0 Hz, ArH);IR (KBr, ν, cm-1): 3450, 3320, 3200, 2965, 2200, 1660,1598, 1510, 1450, 1390, 1261, 1150, 1135, 1035, 810,795, 760。
产物 3e: m.p.: 170~172 ℃ (Lit.: 167~168 ℃);1H NMR(DMSO-d6) δ: 1.78(s, 3H, CH3), 4.72(s, 1H,C4-H), 7.15~7.19(m, 2H, ArH), 7.22(s, 2H, NH2),7.29~7.34(m, 3H, ArH), 7.47~7.51(m, 2H, ArH), 7.78(d,J=8Hz, 2H, ArH); IR(KBr) ν: 3454, 3329, 2203, 1666,1597, 1519, 1445, 1390, 1264, 1226, 1158, 1126, 1096,1068, 1027, 812, 753, 685cm-1。
产物 3f: m.p.: 207~208 °C;1H NMR (DMSO-d6, δ,10-6): 1.80 (3H, s, CH3), 4.72 (1H, s, C4-H), 7.23~7.25(4H, m, NH2+ArH), 7.31~7.35 (1H, m, ArH), 7.48~7.56(4H, m, ArH), 7.78~7.80 (2H, m, ArH); IR (KBr, ν,cm-1): 3450, 3324, 2199, 1660, 1594, 1518, 1488, 1391,1127, 1126, 1070, 1010, 752。
产物 3g: m.p.: 185~186 °C (Lit.: 182~184℃);1HNMR (DMSO-d6, δ, 10-6): 1.78 (3H, s, CH3), 5.16 (1H, s,C4-H), 7.31~7.44 (5H, m, NH2+ArH), 7.48~7.52 (2H, m,ArH), 7.62 (1H, s, ArH), 7.78 (2H, d, J = 8.0 Hz, ArH);IR (KBr, ν, cm-1): 3458, 3325, 2198, 1660, 1583, 1560,1520, 1493, 1470, 1457, 1392, 1269, 1182, 1126, 1102,1072, 906, 836, 815, 758, 691。
产物 3h: m.p. 180~181 °C (Lit.177~178 °C);1HNMR (DMSO-d6, δ, 10-6): 1.79 (3H, s, CH3), 4.73 (1H, s,C4-H), 7.25 (2H, s, NH2), 7.29~7.34 (3H, m, ArH), 7.41(2H, d, J = 8.0 Hz, ArH), 7.47~7.51(2H, m, ArH),7.78(2H, d, J = 8.0 Hz, ArH); IR (KBr, ν, cm-1): 3459,3325, 2202, 1661, 1594, 1518, 1491, 1444, 1391, 1262,1127, 1089, 1066, 1015, 831, 804, 751, 686。
3、 实验小结
本次实验设计打破传统的纯粹验证型、演示型的实验模式,引导学员展开研究性学习和创造性实验研究。
在实验的设计环节,学员收获的不仅仅是实验结果,还有学习的态度和方法的转变。在确定实验设计方案的过程中,需要查阅大量文献,了解该方向的最新发展动态,学员们不满足于国内的研究成果,利用各种数据库,接触到大量的外文文献,极大的激发了他们的求知欲,调动了他们的动手积极性。充分为学员创造提供良好的实验环境、条件,让他们自主的发挥他们的创造力,最大限度的培养学员创新精神和创新能力,充分实现人的发展。
参考文献:
[1]刘晓宇,明霞,王洪来. 浅论大学化学教学中的创新教育[J]. 教学研究与改革,2004(5): 66-67.
全球经济增长引起的化石能源危机及日趋严重的环境污染问题是21世纪人们所面临的重大挑战,因此,清洁的可替代能源也成为本世纪的研究热点。氢是最轻且质量能量密度最大的燃料,它的燃烧产物为水,对环境无污染,因而被公认为未来可替代石油类化石燃料的能...
呋喃是是重要的化工原料,其市场需求正逐年增加。而传统的呋喃制备方法有糠酸脱羧法,糠醛氧化法和石油法(丁二烯氧化法)等。其中前两种方法应工艺落后,催化剂活性不好,污染严重等原因已被淘汰,而石油法却因石油储量逐年减少,价格也逐年增加等原因,市场...
金属和有机小分子催化的硫醚的不对称氧化反应得到了长足的发展,而生物催化硫醚的不对称氧化由于环境友好、反应条件温和、反应体系较为简单等优点,近年来引起了研究人员的广泛关注[1].生物催化剂的来源主要有自然来源的微生物的筛...
烯烃的双官能团化反应能够在烯烃的两端添加两个不同的官能团从而完成化合物种类的转变,通常同时具有原子经济性和步骤经济性等优点,所以格外受到化学合成工作者的青睐。...
木材干馏、粮食发酵等是早期获取醇类的主要途径,产量较小,仅被用作医疗、饮食、香料、染料等日用品的生产原料或溶剂。1923年,德国BASF公司最早开发了以CO和H2为原料,在10~30MPa压力和ZnO-CrO3催化体系作用下生产甲醇的工艺技术[1].目前,合成气制甲醇是...
四氧化三铁纳米颗粒(IONPs)具有独特的超顺磁特性,被广泛应用在污水处理、分析检测、生物大分子及细胞分离、药物靶向运输及可控释放、肿瘤磁热治疗、磁共振成像等领域[1~5].2007年中国科学院生物物理研究所阎锡蕴教授课题组[6]发现IONPs能够模拟辣根过氧化...
二氯化锡是一种重要的还原剂,同时也是一种良好的催化剂,具有较高的反应活性和选择性,可以有效的促进多官能团化合物的分子内及分子间的还原环化反应。而杂环化合物是一类非常重要的有机化合物,它们不仅存在于许多具有重要生理活性的天然产物中,而且也会...
酚类衍生物是生物质木质素的模型化合物,也是煤焦油中的重要馏分和废水中的有害物质,通过酚类衍生物催化加氢可以制备环己酮和环己醇,产物环己酮和环己醇(KA油)是合成纤维尼龙6及尼龙66的单体己内酰胺和己二酸的重要原料,同时也是医药、染料等精细...
甲醇是新的能源和基础化工原料,在我国正处于快速发展时期。从1996年至今,我国甲醇产量年平均增长率高达15%。随着甲醇产能的快速增长,甲醇下游产品的开发也得到了越来越多的重视。甲醇的下游产品主要有:二甲醚、低碳烯烃、甲醛、甲缩醛(DMM)、甲基叔丁...
有机小分子催化具有催化条件温和、催化效率高、对环境友好等优点,并且有机小分子催化剂可以应用到很多金属催化剂不能够涉猎的催化领域,因此引起了广泛的关注,成为近十年来不对称合成研究的热点领域.各种重要的不对称合成反应如D-A反应、Adol反应、Mann...