2.3.2 FF vs. FF/VI.
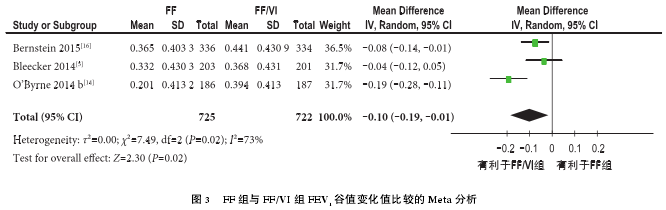
2.3.2.1 FEV1谷值变化值 共纳入 3 个 RCT[5,14,16],各研究之间有统计学异质性(I2=73%,P=0.02),故采用随机效应模型进行 Meta 分析。结果显示,FF组的 FEV1谷值变化值明显小于 FF/VI 组,且差异有统计学意义[MD=–0.10,95%CI(–0.19,–0.01),P=0.02](图 3)。剔除 O'Byrne 2014-b[14]研究进行敏感性分析,结果显示 FF 组的 FEV1谷值变化值仍小于 FF/VI 组,且差异有统计学意义[MD=–0.06,95%CI(–0.11,–0.01),P=0.02].
2.3.2.2 0~24小时wmFEV1变化值 共纳入 3 个RCT[5,14,16],各研究之间无统计学异质性(I2=0%,P=0.93),故采用固定效应模型进行 Meta 分析。结果显示,FF 组的 0~24 小时 wmFEV1变化值明显小于FF/VI,且差异有统计学意[MD=–0.11,95%CI(–0.16,–0.06),P<0.000 1].
2.3.2.3 24小时无需使用缓解药物率变化值 共纳入 3 个RCT[5,14,16],各研究之间无统计学异质性(I2=0%,P=0.93),故采用固定效应模型进行 Meta 分析。结果显示,FF 组的 24 小时无需使用缓解药物率变化值明显小于 FF/VI 组,且差异有统计学意义[MD=–11.57,95%CI(–14.98,–8.15),P<0.000 01].
2.3.2.4 24小时无症状率变化值 共纳入 3 个RCT[5,14,16],各研究之间无统计学异质性(I2=0%,P=0.52),故采用固定效应模型进行 Meta 分析。结果显示,FF 组的 24 小时无症状率变化值明显小于FF/VI 组,且差异有统计学意义[MD=–9.21,95%CI(–12.43,–5.98),P<0.000 01].
2.3.2.5 治疗相关不良事件发生率 共纳入 3 个RCT[5,14,16],各研究之间有统计学异质性(I2=0%,P=0.61),故采用固定效应模型进行 Meta 分析。结果显示,FF 组与 FF/VI 组的治疗相关不良事件发生率差异无统计学意义[OR=–1.05,95%CI(–1.39,–0.80),P=0.72].
2.3.3 FF vs. FP.
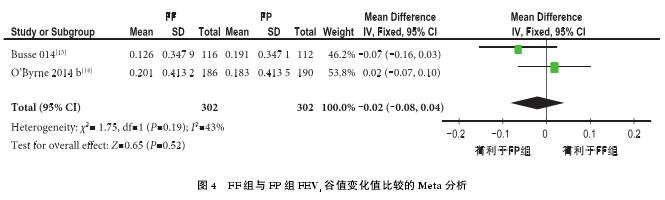
2.3.3.1 FEV1谷值变化值 共纳入 2 个 RCT[13,14]各研究之间无统计学异质性(I2=43%,P=0.19),故采用固定效应模型进行 Meta 分析。结果显示,FF组与FP组的FEV1谷值变化值差异无统计学意义[MD=–0.02,95%CI(–0.08,0.04),P=0.52](图 4)。
2.3.3.2 24小时无需使用缓解药物率变化值 共纳入 2 个 RCT[13,14],各研究之间无统计学异质性(I2=0%,P=0.65),故采用固定效应模型进行 Meta 分析。结果显示,FF 组与 FP 组的 24 小时无需使用缓解药物率变化值差异无统计学意义[MD=–4.44,95%CI(–9.63,0.75),P=0.09].
2.3.3.3 治疗相关不良事件发生率 共纳入 2 个RCT[13,14],各研究之间无统计学异质性(I2=0%,P=0.42),故采用固定效应模型进行 Meta 分析。结果显示,FF 组与 FP 组的治疗相关不良事件发生率差异无统计学意义[OR=1.62,95%CI(0.77,3.40),P=0.20].
3 讨论。
支气管哮喘是常见的呼吸系统疾病,发病的本质原因是气道的慢性炎症,气道炎症存在于哮喘的所有时段,是临床症状和气道高反应性的基础,患者在受寒或接触过敏原等刺激后易诱发支气管痉挛,出现反复发作性喘息、气急、胸闷、咳嗽等,而反复发作患者随着病程的延长,可产生气道重塑,引发呼吸衰竭,甚至出现多器官功能衰竭,影响患者的工作和生活质量,危及生命[17,18].随着我国工业化的进展,哮喘患病率呈明显上升的趋势,据流行病学调查显示,我国总体哮喘患病率为 1.24%,目前约有 2 000 万人罹患哮喘,由此造成的医疗费用约为 600 亿元/年[19],不仅严重威胁人类的健康,同时给患者带来沉重的经济负担,因此规范化的诊断和治疗,特别是长期管理对提高哮喘的控制水平,改善患者生命质量有重要作用。全球哮喘防治创议用药指南推荐吸入型糖皮质激素是控制哮喘病情最有效的药物,可显着改善哮喘患者症状,改善肺功能,减低气道高反应性,但其治疗依从性差会导致哮喘症状复发和控制不佳,因此提高支气管哮喘患者吸入糖皮质激素治疗依从性,可有效提高哮喘控制水平[2,20-24].
本系统评价结果显示,糠酸氟替卡松较安慰剂可显着增加一秒用力呼气量谷值、24 小时无需使用缓解药物率变化值、24 小时无症状率变化值,提示糠酸氟替卡松可显着改善患者肺功能、控制哮喘症状;糠酸氟替卡松较丙酸氟替卡松一秒用力呼气量谷值、24 小时无需使用缓解药物率变化值没有显着差异;糠酸氟替卡松/维兰特罗较糠酸氟替卡松可显着增加一秒用力呼气量谷值、0~24 小时加权平均一秒用力呼气量变化值、24 小时无需使用缓解药物率变化值、24 小时无症状率变化值,提示糠酸氟替卡松/维兰特罗复方制剂较单用糠酸氟替卡松更有助于改善患者肺功能、控制哮喘症状;有关安全性研究发现,糠酸氟替卡松与安慰剂、糠酸氟替卡松/维兰特罗、丙酸氟替卡松分别比较,治疗相关不良反应发生率没有显着差异,安全性较高。糠酸氟替卡松是一种脂溶性的氟化糖皮质激素,由于17-a 糠酸盐酯的结构存在,与其他糖皮质激素相比,糠酸氟替卡松显示出更强的肺组织亲和力;同时糠酸氟替卡松对糖皮质激素受体活性较高,从糖皮质激素受体转移到细胞核的速度更快,核内滞留时间更长,对糖皮质激素受体的选择性超过其他糖皮质激素,与肺组织的结合更为持久[9,25,26].已有文献显示,对于低剂量糖皮质激素不能控制的哮喘患者,糠酸氟替卡松100~400 μg每天晚上一次的剂量均是有效的,且不良反应少、耐受性好,BleecKer等[27]针对 12 岁以上的中度哮喘患者进行的一项双盲、安慰剂对照的剂量范围研究,纳入的 622 例患者随机分成糠酸氟替卡松(100~400 μg)每天晚上一次组、丙酸氟替卡松 250 μg 每天两次组及安慰剂组,经过 8 周的治疗,糠酸氟替卡松每晚一次一秒用力呼气量谷值的改善相等或优于丙酸氟替卡松组;与安慰剂组相比,各组一秒用力呼气量谷值均改善(>200 mL),且差异具有统计学意义(P<0.001),同时 100 μg 和 200 μg 考虑是最合适的使用剂量。另有文献显示,糠酸氟替卡松是一种新型的糖皮质激素,每天一次给药用于哮喘的治疗,更能提高患者的依从性,有利于改善哮喘的总体控制水平[28,29].本研究结果显示,糠酸氟替卡松每日一次用于哮喘患者的治疗,能有效改善肺功能、控制哮喘症状,是一种相对安全的治疗方法,总体上与上述研究结果[27-29]一致,在临床上有广阔的应用前景。
虽然本系统评价纳入的 6 个 RCT 均有明确的纳入标准与排除标准,各研究都对干预前年龄、性别、病情程度等因素进行了基线一致性分析,干预组和对照组具有可比性,但纳入研究仍存在以下局限性:虽然 6 个 RCT[5,12-16]均描述了具体的随机方法及隐蔽分组情况,但有 4 个RCT[5,12,15,16]只提到双盲,但未具体描述如何实施,因此纳入研究存在实施及测量偏倚的低度可能性;4个RCT[5,12,15,16]的退出率较高,为10%~15%,2 个RCT[13,14]的退出大于 15%,存在减员偏倚的中度可能。这些局限性均可能对Meta 分析结果产生影响,从而降低本 Meta 分析结论的可靠性。
综上所述,当前证据显示,糠酸氟替卡松较安慰剂可显着改善患者肺功能、控制哮喘症状,糠酸氟替卡松与维兰特罗联用比单用糠酸氟替卡松疗效更好,且不增加不良反应发生率。糠酸氟替卡松与丙酸氟替卡松两者疗效相当,但前者用法更简便,能很大程度上提高患者的依从性。受纳入研究数量和质量所限,上述结论可能存在偏倚,需开展更多高质量研究予以验证。
参考文献:
1 Asthma Committee, Respiratory Society, Chinese Medical Associ-ation. China Guideline on the Prevention and Treatment of Asth-ma. Chin J Tubere Respir Dis, 2013, 36(5): 3331-336.
2 Bateman ED, Hurd SS, Barnes PJ, et al. Global strategy for asthmamanagement and prevention: GINA executive summary. EurRespir J, 2008, 31(1): 143-178.
3 Price D, Robertson A, Bullen K, et al. Improved adherence withonce-daily versus twice-daily dosing of mometasone furoateadministered via a dry powder inhaler: a randomized open-labelstudy. BMC Pulm Med, 2010, 10: 1.
4 Bateman ED, Bleecker ER, Lotvall J, et al. Dose effect of once-dailyfluticasone furoate in persistent asthma: a randomized trial. RespirMed, 2012, 106(5): 642-650.
5 Bleecker ER, Lotvall J, O'Byrne PM, et al. Fluticasone furoate-vilanterol 100-25 mcg compared with fluticasone furoate 100 mcgin asthma: a randomized trial. J Allergy Clin Immunol Pract, 2014,2(5): 553-561.
6 Busse WW, Bleecker ER, Bateman ED, et al. Fluticasone furoatedemonstrates efficacy in patients with asthma symptomatic onmedium doses of inhaled corticosteroid therapy: an 8-week,randomised, placebo-controlled trial. Thorax, 2012, 67(1): 35-41.
7 Woodcock A, Bleecker ER, Busse WW, et al. Fluticasone furoate:once-daily evening treatment versus twice-daily treatment inmoderate asthma. Respir Res, 2011, 12: 160.
8 Woodcock A, Bateman ED, Busse WW, et al. Efficacy in asthma ofonce-daily treatment with fluticasone furoate: a randomized,placebo-controlled trial. Respir Res, 2011, 12: 132.
9 Rossios C, To Y, To M, et al. Long-acting fluticasone furoate has asuperior pharmacological profile to fluticasone propionate inhuman respiratory cells. Eur J Pharmacol, 2011, 670(1): 244-251.
10 Allen A, Bareille PJ, Rousell VM. Fluticasone furoate, a novelinhaled corticosteroid, demonstrates prolonged lung absorptionkinetics in man compared with inhaled fluticasone propionate.Clin Pharmacokinet, 2013, 52(1): 37-42.
11 National AE, Prevention P. Expert Panel Report 3(EPR-3):Guidelines for the Diagnosis and Management of Asthma-Summary Report 2007. J Allergy Clin Immunol, 2007, 120(5Suppl): S94-138.
12 O'Byrne PM, Woodcock A, Bleecker ER, et al. Efficacy and safetyof once-daily fluticasone furoate 50 mcg in adults with persistentasthma: a 12-week randomized trial. Respir Res, 2014, 15: 88.
13 Busse WW, Bateman ED, O'Byrne PM, et al. Once-dailyfluticasone furoate 50 mcg in mild-to-moderate asthma: a 24-weekplacebo-controlled randomized trial. Allergy, 2014, 69(11): 1522-1530.
14 O'Byrne PM, Bleecker ER, Bateman ED, et al. Once-dailyfluticasone furoate alone or combined with vilanterol in persistentasthma. Eur Respir J, 2014, 43(3): 773-782.
15 Bateman ED, O'Byrne PM, Busse WW, et al. Once-dailyfluticasone furoate (FF)/vilanterol reduces risk of severeexacerbations in asthma versus FF alone. Thorax, 2014, 69(4): 312-319.
16 Bernstein DI, Bateman ED, Woodcock A, et al. Fluticasone furoate1persistent asthma. J Asthma, 2015, 52(10): 1073-1083.
17 Denner DR, Doeing DC, Hogarth DK, et al. Airway Inflammationafter Bronchial Thermoplasty for Severe Asthma. Ann Am ThoracSoc, 2015, 12(9): 1302-1309.
18 Rodrigo GJ, Castro-Rodriguez JA. Tiotropium for the treatment ofadolescents with moderate to severe symptomatic asthma: asystematic review with meta-analysis. Ann Allergy Asthma18Immunol, 2015, 115(3): 211-216.
19 冯晓凯。 我国支气管哮喘患病情况及相关危险因素的流行病学调查。 北京: 北京协和医学院, 2014.
20 Finkelstein Y, Bournissen FG, Hutson JR, et al. Polymorphism ofthe ADRB2 gene and response to inhaled beta- agonists in childrenwith asthma: a meta-analysis. J Asthma, 2009, 46(9): 900-905.
21 Wenzel SE, Balzar S, Ampleford E, et al. IL4R alpha mutations areassociated with asthma exacerbations and mast cell/IgE expression.Am J Respir Crit Care Med, 2007, 175(6): 570-576.
22 Loza MJ, Chang BL. Association between Q551R IL4R geneticvariants and atopic asthma risk demonstrated by meta-analysis. JAllergy Clin Immunol, 2007, 120(3): 578-585.
23 程江华。 支气管哮喘患者吸入糖皮质激素治疗依从性的研究。 中国实用医药, 2016, 11(11): 195-196
24 谢先茂。 支气管哮喘患者治疗依从性与疾病控制的关联性研究。中国当代医药, 2016, 23(26): 31-33.
25 Biggadike K, Bledsoe RK, Hassell AM, et al. X-ray crystal structureof the novel enhanced-affinity glucocorticoid agonist fluticasonefuroate in the glucocorticoid receptor-ligand binding domain. JMed Chem, 2008, 51(12): 3349-3352.
26 Salter M, Biggadike K, Matthews JL, et al. Pharmacologicalproperties of the enhanced-affinity glucocorticoid fluticasonefuroate in vitro and in an in vivo model of respiratoryinflammatory disease. Am J Physiol Lung Cell Mol Physiol, 2007,293(3): L660-667.
27 Bleecker ER, Bateman ED, Busse WW, et al. Once-daily fluticasonefuroate is efficacious in patients with symptomatic asthma on low-dose inhaled corticosteroids. Ann Allergy Asthma Immunol, 2012,109(5): 353-358.
28 Richter A, Anton SF, Koch P, et al. The impact of reducing dosefrequency on health outcomes. Clin Ther, 2003, 25(8): 2307-2335.
29 Guest JF, Davie AM, Ruiz FJ, et al. Switching asthma patients to aonce-daily inhaled steroid improves compliance and reduceshealthcare costs. Prim Care Respir J, 2005, 14(2): 88-98.