
肌联蛋白(titin)是一个肌小节蛋白,发现相对较晚,但功能重要.Titin是哺乳动物体内分子量最大的蛋白,随亚型结构不同分子量达2970-3700kDa.Titin的N-C末端跨越半个肌小节,N末端与肌动蛋白相互作用固定于Z线,C末端附着在M线的肌球蛋白上。
Titin的发现是对滑行肌丝模型理论(sliding filament model)的重要补充,是肌原纤维中的“第三肌丝”.其结构特点有利于维持肌原纤维的完整性和稳定性,为粗肌丝装配的模版蛋白.并且,titin的I带部分具有高度折叠的弹簧样分子结构,是心肌细胞执行舒张功能的重要结构基础.Titin在 心 肌 细 胞 中 同 时 表 达N2B和N2BA两种亚型,N2B更短更僵硬,N2BA更长更有弹性,在不同的种属、不同的发育阶段和病理状态下,N2B/N2BA比值变化,可导致心脏僵硬度发生明显的改变.为研究titin的生理病理功能,需对titin及其亚型进行有效的电泳分离。
SDS-聚丙烯酰胺凝胶电泳(SDS-polyacrylamide gel electropho-resis,SDS-PAGE)是分离鉴别蛋白的重要实验方法,但该方法不能有效地分离大于500KDa的大分子量蛋白,对于超大分子量的titin而言需要特殊的电泳技术.本试验为能同时有效地分离肌小节内的超大分子量蛋白titin各亚型和中分子量的肌球蛋白重链(Myosin heavy chain,MHC),增强titin研究的可行性和科学性,对其电泳方法进行了改良。
采用大面积垂直电泳,在电泳板上层以SDS-琼脂糖胶(SDS-agarose gel electrophoresis,SDS-VAGE)方法分离titin各亚型,下层以SDS-PAGE电泳分离MHC,建立了能够同时分离、检测分子量跨越范围大的多个蛋白的一步法电泳。
材料和方法
1.材料
1.1 仪器与试剂
DYY-60型电泳仪;16cm×18cm垂直凝胶电泳槽(Bio-rad,美国);凝胶成像系统(KODAK,美国);琼脂糖(SeaKem Gold AGAROSE,Sigma,美国);四甲基乙二铵(Sigma,美国);丙烯酰胺、硝酸银、硅钨酸、冰醋 酸、甲 醛、甘 油、甘 氨 酸、十 二 烷 基 苯 磺 酸 钠(SDS)、三羟甲基氨酸甲烷(Tris)、过硫酸铵(Aps)等。
1.2 实验材料
实验兔和小鼠,均于麻醉后迅速摘取心脏,用冰生理盐水冲洗,沿房室环剪去左右心房及右室游离壁,然后切取左心,心尖至心底连线中点处游离壁心肌组织,置液氮保存后转移至-80℃低温冰箱以备做。同样方法留取兔腓肠肌组织。
2.方法
2.1总蛋白提取
取少量的上述的兔心肌组织、小鼠心肌组织,兔腓肠肌组织。将各组标本分别置于预冷的研钵中,在液氮浸泡下将组织块研磨成粉状。将粉状组织分装入EP管中,并按1∶40移入裂解液。60℃加热10min.涡旋后,在13 200r/min离心5min,取上清即行电泳。
2.2 垂直凝胶板的制备
将两块16cm×18cm的垂直电泳玻板和齿梳洗净后,再用酒精擦拭,晾干,安装在配胶架上。
2.2.1 配制PAGE胶
先配制15ml 6 %的PAGE胶,配方如下:30%丙烯酰胺溶液3ml、2mol/L Tis(pH 8.8)5.7ml、甘油0.15 ml、Aps 0.15 ml、去离子水6 ml、TEMED 0.012ml、SDS 0.15ml.配置后立即混匀,迅速将配置好的PAGE胶灌注到两块玻璃板中间的间隙中,小心地用双蒸水覆盖,室温垂直放置1h使之凝固。PAGE胶高度约占整片垂直电泳胶的1/3,主要起到分离中分子蛋白MHC的作用,同时可防止在垂直电泳中上层VAGE胶从底部脱落。待PAGE胶聚合完成后,倒掉覆盖层,尽可能排去凝胶上的液体,用吸水纸吸干。并将带有PAGE胶的垂直电泳槽置于60℃烤箱中预热约15min.
2.2.2 配制VAGE胶
VAGE胶灌注在PAGE胶上方,约占整片垂直电泳胶的2/3,主要起到分离巨大分子titin亚型的作用。按照下述方法配制50ml 1 %的VAGE胶:100%甘油15ml,5#buffer(0.25mol/L Tris,1.92mol/L甘氨酸,0.5% SDS)10ml,去离子水定容至50ml.秤取琼脂糖0.5g,将上述50ml溶液溶解琼脂糖。反复煮沸,使琼脂糖充分溶解。其后将琼脂糖液置入60℃烤箱10min,以排除液体中的气泡。将1% VAGE胶直接灌注到已预热的垂直电泳槽中,灌注后再次放入60℃烤箱5-10min,使液状胶体中的气泡能上升至液面。取出已灌注的垂直电泳槽,排除气泡后,立即在其中插入一块干净的齿梳。室温冷却后置于4℃冰箱制冷,至少放置30min后方能行电泳。也可于4℃冰箱中放置不超过2d.
2.3 点样
待VAGE胶聚合冷却后,小心移去齿梳。将凝胶固定在电泳装置上,分别在上下电泳槽加入蛋白质电泳缓冲液,缓冲液配方:50mmol/L Tris,0.384mol/L甘氨酸,0.1% SDS,上槽中需添加0.08%2-巯基乙醇。排除气泡后按照预定顺序每个样品上样10μl,不用上样的空孔加入等体积的2×SDS凝胶上样缓冲液。
2.4 电泳
在恒温4℃下进行电泳。接通电源,设定电压为200-250v,恒 定 电 流15 mA.当 溴 酚 蓝 到 达 下 层PAGE胶体底部时,可停止电泳,约需持续电泳5h.卸下玻板,在缓和的流水中轻轻撬开,取出凝胶。小心分离出下层的PAGE胶和上层的VAGE胶。
2.5 染色
PAGE胶使用考马斯亮蓝染色法:用至少5倍体积的考马斯亮蓝R250染色液浸泡PAGE胶,室温下置于摇床上平缓摇动1h.将凝胶移入脱色液中,室温平缓摇动4-8h,其间更换脱色液2-3次;VAGE胶使 用 银 染 法:使 用100 ml固 定 液 浸 泡VAGE胶,室温下置于摇床上平缓摇动1h.弃除固定液后,置胶片于37℃118-20h,使胶片中水分减少,胶片变薄可降低银染时背景对结果观察的影响。蒸馏水摇晃洗涤20min×3次。2 %亚铁氰化钾浸泡5min后,蒸馏水摇晃洗涤5 min×3次。100ml新鲜配制的银染液染色,待蛋白条带出现即倒掉银染液,予1%冰乙酸液洗胶,中和停止银染反应。
2.6 上述凝胶均于染色后 即扫描 记录,使用Bandscan分析软件对目标条带行蛋白定量。
结果
Titin为 动 物 体 内 分 子 量 最 大 的 蛋 白,使 用SDS-VAGE电泳并银染可见titin的蛋白条带处于胶片的最顶端。Titin具有数个亚型,亚型的数量比例在不同的物种中差别甚远。因为兔腓肠肌titin基本为N2A亚型,鼠心肌titin 99 %为N2B亚型,所以可使用这两种组织的titin电泳条带作为tit-inN2A和N2B亚型的标记.蛋白电泳结果显示:采用改良后的电泳方法,上层SDS-VAGE胶能成功分离titin,银染后可清晰显示titin各亚型及其分解产物T2.使用兔腓肠肌作为titin N2A标记,鼠心肌作为titin N2B标记,可确定兔心肌细胞分离出N2B和N2BA亚型,titin各亚型相应条带所处位置与其分子量大小一一对应(图1).

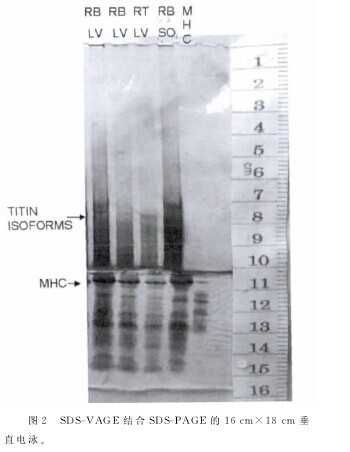
上层SDS-VAGE胶经银染处理后明显变薄并收缩,可减少银染时背景染色过深导致条带分析困难。上层的VAGE胶与下层的PAGE胶连接良好(图2)。与标记蛋白对照,可见下层SDS-PAGE胶能清晰地分离出MHC.根据以往文献报道,使用银染法能提高titin蛋白条带的检出率。本实验发现如同时使用银染法标记MHC其条带染色弥散,背景较深,影响电泳图像分析。故对SDS-PAGE胶使用考马斯蓝染色,结果显示MHC条带显示清晰(图2).
讨论
SDS-PAGE是分析生物体蛋白常用的方法,其基本原理在于:使用化学物消除蛋白的电荷差,由蛋白分子量的大小决定电泳迁移率,实现蛋白分离。不同浓度的聚丙烯酰胺凝胶形成不同凝胶孔径,与相应的蛋白质分子大小接近,可提高对蛋白的分辨能力。大部分的生物体蛋白可通过SDS-PAGE被分离、鉴定和纯化,但对于大分子量的蛋白,使用常规的电泳分离效果差。大分子量蛋白,需要低浓度的聚丙烯酰胺凝胶,低浓度的凝胶接近液态状,机械强度低,不利于实验操作,同时在固定与染色阶段容易出现胶体的断裂和破碎,影响实验效果。
Titin分子量巨大,其蛋白电泳方法是研究的难点,同时也导致了titin研究受到限制。既往使用的分离titin的电泳方法是用低浓度或2%-9.5%浓度渐变SDS-PAGE胶进行电泳.但这些方法均不能克服低浓度的PAGE胶带来的实验困难,如:胶片制作困难;实验操作中胶片容易破损;titin亚型的分离效果欠佳;转膜效率低而难以行下一步的western blot检测。至2003年Warren等使用1%SDS-琼脂 糖 胶 (SDS-agarose gel electrophoresis,SDS-VAGE)垂直电泳可清晰地分离titin的各种亚型,并证实该电泳系统可应用于大分子量蛋白(≥220kDa)的分离.
根据上述方法进行改良的垂直电泳方法,电泳胶片分为两大部分:上2/3使用SDS-VAGE胶对titin进行分离及银染;下1/3采用SDS-PAGE胶对MHC进 行 分 离 并 予 考 马 斯 蓝 染 色。在 上 部 的VAGE胶中因为琼脂糖形成的孔径大,对于超大分子量的titin蛋白而言是良好的电泳介质。
Titin在SDS-VAGE胶中缓慢移动,电泳约5小时可实现亚型的 分 离。对 中 小 分 子 量 的 蛋 白 而 言,上 层 的VAGE胶相当于不连续电泳系统中的低浓度的浓缩胶。中小分子量的蛋白在SDS-VAGE胶中电迁移速度快,有利于这些蛋白从最初的样品溶液中浓缩出来,进而在下部的SDS-PAGE胶中实现电泳分离。一步法的垂直电泳方法有助于在实验中实现一次电泳同时分离多个分子量差距大的蛋白,提高实验效率。此方法也有利于titin的研究,因为titin极易出现降解,无法制备相关的独立标记蛋白,故使用内参的方法对titin进行定量检测更为准确.在本实验中可以MHC作 为内 参,总titin=N2B+N2BA+T2,titin总量可表达为总titin/MHC.
此外,使用上述两种胶体结合的大面积垂直电泳也有助于提高蛋白含量测定的精确性。因为蛋白电泳作为一种操作技术,在试验过程中有多方面的因素可能影响实验结果,如:标本的准备方法;凝胶的组成和浓度;电泳分离参数和染色条件等。总体而言,蛋白定量检测过程中应注意使用同等条件准备标本、进行电泳及分析。本实验采用的垂直电泳板面积为16cm×18cm,共有21个点样孔,允许多个标本同时电泳。并可根据实验目的选择相应胶体进行组合,一次电泳即可检测出标本中的多个目标蛋白,减少分次电泳中存在的不可控误差,提高了结果比较和分析的可靠性。
参考文献
[1]Trombitas K,Jin JP,Granzier H.The mechanically ac-tive domain of titin in cardiac muscle.Circ Res,1995,77:856-861
[2]Linke WA,Rudy DE,Centner T,et al.I-band titin incardiac muscle is a three-element molecular spring and iscritical for maintaining thin filament structure.J Cell Bi-ol,1999,146:631-644
[3]Maruyama K,Connectin.An elastic protein from myofi-brils.J Biochem(Tokyo),1976,80:405-407
[4]Horowits R.The physiological role of titin in striatedmuscle.Rev Phydiol Biochem Pharmacol,1999,138:57-96
[5]Gregorio CC,Granzier H,Sorimachi H,et al.Muscleassembly:a titanic achievementCurr Opin Cell Biol,1999,11:18-25
[6]Cazorla O,Freiburg A,Helmes M,et al.Differentialexpression of cardiac titin isoforms and modulation ofcellular stiffness.Circ Res,2000,86:59-67
蛋白质组学研究的主要内容包括在蛋白质水平上大规模地分析组织细胞的蛋白质表达水平、翻译后修饰、蛋白质间的相互作用等,从而揭示蛋白质的功能,已在疫苗筛选、指导治疗、临床药物开发及预后判断等领域发挥了重要作用。...
甘油三酯(triglyceride,TG)是人体内含量最多的脂类,是体内能量的主要来源.TG检测是一项重要的临床血脂常规测定指标.血清甘油酯测定方法可分为化学法、酶标板法和色谱法3大类.化学法因操作步骤繁多、技术要求高而不适于常规工作应用.核素稀释/气相色谱...
在自然环境下,两栖动物受到紫外线、病原微生物的伤害及捕食者的威胁.面对恶劣的自然环境,两栖动物体表进化出许多特殊的腺体,这些腺体能够分泌丰富多样的生物活性肽,如抗氧化肽、抗菌肽、抗病毒多肽等,其中的抗菌肽研究已取得诸多进展.有研究者仅从...
近年来,分子生物学技术发展迅速,尤其是基于PCR衍生出的一系列技术,因其具有操作简单、快速准确、特异性强且灵敏度高的特点,已被广泛应用于各种检测领域。...
绝大多数真核生物的生命活动都离不开氧气,氧气与高等生物体的能量代谢等过程密切相关。氧气分子在代谢中间体、酶和辐射作用下产生活性氧(Reactive oxygen species,ROS),其在正常生理条件下对细胞代谢的调控发挥着至关重要的作用。...
蛋白质组是指一种细胞、组织乃至一种生物所表达的全部蛋白质。相较于传统的蛋白质研究,蛋白质组学可以在大规模水平上一次性鉴定成千上万种蛋白质的表达水平、修饰水平相互作用等,从而揭示蛋白质参与生命活动的作用。...
LAMP技术已经广泛用于植物病害的检测,其灵敏度远高于普通PCR技术,且对于样品的纯度、用量要求更低,结合显色指示剂能够实现可视化检测,操作更加简单快速,可满足田间现场的检测要求,有利于对田间病害的早期快速诊断治理。...
多重PCR又称复合PCR,是在常规PCR基础上改进并发展起来的一种新型PCR扩增技术,即在同一个反应体系中加入两对以上引物,同时在同一模板或不同模板之间进行多个核酸片段的扩增。...
0前言在所有的环境污染物种类当中,铅是一种较为常见的元素,其不仅会对人体产生一定的毒害作用,更会直接危害到动植物的健康与生态环境的平衡。传统的检测方式则更是多种多样,包括光谱检测、电泳仪、液相色谱检测法和双硫腙对比法等等,尽管传统的检测方...
硒是人体所必需的一种微量元素,它能提高人体的免疫力,并能预防许多种疾病,在机体中它有重要的生理作用[1-3],硒是谷胱甘肽过氧化酶、5.-脱碘酶的必需组成部分,同时又是体内许多蛋白质的组成成分,对动物机体抗氧化、抗应激、提高免疫力等起着重要的作用...